Сколько лет положено тестировать вакцину
Обновлено: 04.07.2024
Есть три этапа испытаний. Только вакцина, прошедшая тестовую фазу, может перейти на следующий уровень испытаний. Если вакцина на каком-то этапе не соответствует требованиям, ее испытания прекращаются.
В фазе 1 испытаний проводится проверка безопасности вакцины.
Обычно вакциной-кандидатом вакцинируется порядка ста здоровых молодых людей, после чего описываются и анализируются ее побочные эффекты, чтобы определить, достаточно ли безопасна вакцина при введении людям. Эта фаза продолжается от нескольких недель до месяцев.
В фазе 2 испытаний определяется необходимая доза вакцины.
Несколько сотен людей из разных возрастных групп получают повышенные дозы вакцины, чтобы определить дозу, при которой они вырабатывают достаточное количество антител в крови. Также определяется, сколько раз требуется введение вакцины, и с каким интервалом, для выработки напряженного иммунитета. Продолжительность этого этапа составляет от нескольких месяцев до года.
И, наконец, в фазу 3 проводится тестирование эффективности вакцины. В этой фазе вакцинируется несколько тысяч человек из всех возрастных групп. Кроме того, контрольная группа получает плацебо. Исследователи проводят наблюдения чтобы выяснить, защищает ли вакцина от инфекции. Если заболеваемость в группе субъектов, вакцинированных вакциной-кандидатом значительно ниже, чем у испытуемых, вакцинированных плацебо, значит, вакцина-кандидат эффективна. Этот этап испытаний в среднем длится от одного года до полутора лет.
Исследования на группах добровольцев могут частично заменить трудоемкие и дорогостоящие исследования фазы 3.
В разных странах некоторыми исследователями и разработчиками вакцин периодически предлагается пропустить эксперименты на животных и немедленно протестировать вакцины-кандидаты на людях. Однако большинство фармацевтических компаний не склонно исключать какие-либо этапы исследований, чтобы сэкономить время. Профиль безопасности вакцины ставиться на первое место.
На сегодняшний день во всем мире университетами и фармацевтическим компаниями разрабатываются более 123 вакцин-кандидатов, причем новые вакцины появляются чуть не каждую неделю. Большинство вакцин находятся на стадии лабораторных экспериментов или экспериментов на животных. Малая часть проходит испытания на людях.
Все эти вакцины работают по одному и тому же принципу. Они подвергают организм воздействию одного или нескольких вирусных компонентов, которые сами по себе не вызывают заболевания, но позволяют нашей иммунной системе распознавать вирус и быстро и эффективно уничтожить его при попадании в организм.
При создании вакцины могут использоваться разные способы. Например, может использоваться убитый температурой или определенными химическими веществами вирус SARS-CoV-2. Преимущества таких вакцин заключается в том, что с технической точки зрения их довольно легко производить. Недостатком таких вакцин является то, что для их производства необходимо культивировать большое количество вируса, и полностью уничтожить каждую вирусную частицу. С помощью этой техники производятся вакцина против гепатита А, а также вакцина против гриппа.
Также для создания вакцины может использоваться генетически ослабленный, но живой вирус SARS-CoV-2. Генетический код вируса изменяют в лаборатории, так что он больше не вызывает заболевание, а создает иммунитет. Такие вакцины приводят к формированию устойчивого иммунитета, однако, хоть и очень редко, ослабленный вирус может снова превратиться в свой опасный вариант. С помощью этой техники созданы вакцины от эпидемического паротита, кори, краснухи, желтой лихорадки.
Также для создания вакцины можно использовать другой, безвредный вирус в качестве переносчика для встроенных в него генов SARS-CoV-2. В организме эти гены отвечают за синтез белков, которые вызывают иммунный ответ. Созданные таким образом вакцины довольно безопасны и вызывают достаточную иммунную защиту. Однако при наличии иммунитета к вирусу-переносчику эффективность вакцины может снизиться. С помощью этой техники создана вакцина против лихорадки Эбола.
Чаще всего при создании вакцины используются части белков микроорганизма, в нашем случае используются белки вируса SARS-CoV-2
Так можно производить вакцины безопасно, быстро и в достаточных количествах. Однако такие вакцины вызывают ограниченную иммунную защиту, также часто требуется ревакцинация. По этой методике производятся вакцина против коклюша и вакцина против рака шейки матки.
В связи с проведением массовой вакцинации от COVID-19 актуальным представляется вопрос об условиях клинических испытаний лекарственных препаратов и их особенностях для отдельных категорий, участвующих в испытаниях граждан.
На данный момент ни одна из отечественных вакцин не прошла все фазы клинических испытаний ( см.: Реестр разрешений на проведение клинических исследований Государственного реестра лекарственных средств).
Под клиническим испытанием лекарственного препарата понимается изучение диагностических, лечебных, профилактических, фармакологических свойств лекарственного препарата в процессе его применения у человека, путем применения научных методов оценок в целях получения доказательств безопасности, качества и эффективности лекарственного препарата, данных о нежелательных реакциях организма человека на применение лекарственного препарата и об эффекте его взаимодействия с другими лекарственными препаратами и ( или) пищевыми продуктами. [1]
Главное отличие клинического испытания от доклинического исследования заключается в том, что испытуемыми являются не животные, а люди.
Для этих целей на подпись гражданину представляется информационный листок, где должны быть указаны следующие сведения:
- о лекарственном препарате для медицинского применения и сущности клинического исследования этого лекарственного препарата;
- о безопасности ( характеристика основанная на сравнительном анализе его эффективности и риска причинения вреда здоровью) лекарственного препарата для медицинского применения, его ожидаемой эффективности ( характеристика степени положительного влияния лекарственного препарата на течение, продолжительность заболевания или его предотвращение) и степени риска для пациента.
Кратко в данном разделе должна быть представлена информация, относящаяся к безопасности, фармакодинамике, эффективности и дозозависимости эффектов исследуемого продукта. Должны быть освещены значимые различия в характере/частоте нежелательных реакций, как для различных показаний, так и для различных популяций. Должны быть описаны возможные риски и нежелательные реакции, которые можно ожидать, основываясь на накопленном опыте применения, как исследуемого продукта, так и сходных с ним продуктов. Должны быть также описаны меры предосторожности или специальные методы наблюдения, которые необходимо применять при использовании продукта с исследовательскими целями; [3]
об условиях участия граждан в клиническом исследовании лекарственного препарата для медицинского применения;
На наш взгляд, кроме перечисленных выше сведений потенциальному участнику клинических испытаний должен быть представлен под роспись перечень противопоказаний для применения данного лекарственного средства с детальной расшифровкой каждого из них.
Следует отметить, что перед началом испытаний в обязательном порядке должно проводиться предварительное обследование состояния здоровья, в том числе должен быть детально и всесторонне оценен иммунный статус участника эксперимента. В противном случае невозможно будет назвать эту процедуру исследованием, поскольку не представится возможным оценить динамику показателей здоровья, в частности невозможно будет установить иммунный ответ испытуемого.
Необходимым условием является право на односторонний отказ от участия в испытании на любой его стадии без каких-либо ограничений со стороны пациента. Данная норма отражает положения Хельсинской декларации, а также конституционное право граждан, закрепленное в статье 21 — никто не может быть без добровольного согласия подвергнут медицинским, научным или иным опытам.
Субъектов испытаний в зависимости от наличия ограничений можно разделить на 3 группы.
Первую группу составляют категории граждан, которым на законодательном уровне установлен императивный запрет на участии в клинических испытаниях. В эту группу входят:
1.1. Дети сироты и дети без попечения;
1.2. Военнослужащие по призыву;
1.3. Сотрудники правоохранительных органов;
1.4. Лица, отбывающие наказания в местах лишения свободы и лица, находящиеся под стражей в следственных изоляторах.
В данный перечень, по нашему мнению, необходимо также включить пациентов, находящихся на стационарном лечении, состояние здоровья которых исходя из медицинских показателей не позволяет пациентам с онкологическими, инфекционными, аллергологическими, пульмонологическими и другими заболеваниями быть участниками клинический испытаний лекарственных препаратов.
Вторую группу составляют лица, которые могут стать субъектами клинических испытаний только при соблюдении определенных условий:
2.1. Несовершеннолетние могут участвовать в испытании только при условии, что: родители или законные представители дали на это информированное письменное согласие, проведение испытания необходимо для укрепления здоровья детей или профилактики инфекционных заболеваний в детском возрасте либо если целью такого исследования является получение данных о наилучшей дозировке лекарственного препарата для лечения детей. Такому исследованию должно предшествовать клиническое исследование лекарственного препарата для медицинского применения на совершеннолетних гражданах ( за исключением случаев, если исследуемый лекарственный препарат предназначен исключительно для использования несовершеннолетними).
2.2. Женщины в период беременности и грудного вскармливания при условии, что препарат предназначен для применения женщинами в указанный период, либо если исключается риск вреда женщине, плоду и ребенку.
2.3. Военнослужащие, при условии, что лекарственный препарат специально разработан для применения в условиях военных действий, чрезвычайных ситуаций, профилактики и лечения заболеваний и поражений, полученных в результате воздействия неблагоприятных химических, биологических, радиационных факторов
2.4. Лица с психическими заболеваниями могут стать субъектами клинических испытаний при наличии письменного согласия их законных представителей и при условии, что препарат предназначен для лечения психических заболеваний.
- лиц в домах престарелых;
- этнические меньшинства;
- лиц без определенного места жительства;
- беженцев;
- студентов университета;
- служебный, больничный и лабораторный персонал;
- наемных рабочих спонсора.
В частности предполагается, что на готовность указанных лиц участвовать в клиническом исследовании может излишне влиять ожидание, обоснованное или нет, или выгода, связанная с участием или негативной реакцией администрации в случае отказа от участия.
Если у вас по-прежнему есть проблемы со сроком действия документа, сообщите об ошибке на портале госуслуг через форму обратной связи. Еще в начале декабря Минздрав изменил срок действия QR-кода переболевшего. Теперь документ действует не полгода, а 12 месяцев. Изменения в старые сертификаты уже вносят.
Утром 8 ноября пользователи портала госуслуг обнаружили, что срок действия сертификата о вакцинации от коронавируса сократился с года до шести месяцев.
Это стало неожиданностью, поскольку в большинстве регионов России для посещения общественных мест сейчас требуют QR-коды , которые подтверждают перенесенный COVID-19 или пройденную вакцинацию. Сертификат о вакцинации нужен и путешественникам: во многих странах его принимают вместо отрицательного результата ПЦР-теста .
Важно понимать: в случае ухудшения эпидситуации срок действия QR-кода действительно могут ограничить до шести месяцев. Об этом сказано в методических рекомендациях о проведении вакцинации на сайте министерства здравоохранения.
Сразу после обновления сертификата на портале госуслуг несколько человек в редакции Т—Ж столкнулись с тем, что срок действия их документа после перенесенного коронавируса теперь не полгода, а год. А просроченные сертификаты переболевшего, которые ушли в архив, вновь стали действительными.
Такой сертификат о вакцинации получила наш редактор: в нем срок действия отсчитывают с момента выздоровления. То есть QR-код действителен до 16 марта 2022 года, хотя должен действовать до августа 2022 года
Возможно, сбои связаны с тем, что с 8 ноября Минздрав изменил форму коронавирусного сертификата. Теперь в одном документе указаны не только сведения о вакцинации, но и о перенесенном коронавирусе. Также в нем могут быть сведения о наличии противопоказаний к прививке. Сертификат по-прежнему доступен на двух языках: русском и английском.
Если у вас есть документ старого образца, но хочется получить новый в бумажном виде, нужно обратиться в МФЦ. Электронные сертификаты обновятся автоматически.



С 8 числа во многих регионах массово начали вводить ограничения.
В этот же день решили запилить глобальное обновление сертификатов и софта.
Как итог всё сломалось, действующие сертификаты стали просроченными, вместо новых у кого-то вылезли ошибки. А ведь местами даже в транспорт без QR нельзя было попасть, люди были очень "рады" узнать об этом уже по факту.
Ну гениально же, прям чувствуется типичное глупое принятие решений, подогреваемое приказами сверху.
A, Скорее отрабатывали в реальном времени функцию изменения сроков действия сертификатов.
теперь если будет дана команда о сокращении срока действия сертификатов, то все сработает, как говорится, "без шума и пыли" .
просто постепенно нарабатывают функционал системы.
У меня до сих пор полгода, дата формирования сертификата - сегодняшняя, старого нет. Разминаю пальчики и готовлюсь писать жалобу
Мария, Срать там сверху хотели на наши жалобы
Мария, а куда писать собираетесь - у меня такая же ситуация

Кузьменкова, уже никуда. с утра восстановился срок действия. но вообще писала бы в службу поддержки Госуслуг
Мария,благодарю, но пока у меня не восстанавливается
Кузьменкова Татьяна, у меня тоже после перенесенного заболевания срок сократился -вместо октябрь 22 -май 22. Написала в службу поддержки Госуслуг -жду.

Эх, ждём прекрасное будущее, сначала раз в полгода, затем в три месяца, месяц, неделя. В скором времени будем утром, днём и вечером за прививками ходить
Андрей, зрите в корень - функционал тестируют
У меня в старой форме - действие 1 год, в новой - полгода

До никакой даты. У меня его нет и не будет.
Мне кажется просто проверяли реакцию людей на их очередные подтасовки. На выборах уже научились. Почему технический сбой коснулся только сертификатов на ковид?
Количество требуемых антител. сроки действия иммунитета. сколько раз колоться. "сбои на Госуслугах"
Люди не видят главного. Жизнь каждого человека в новых условиях будет контролироваться записью в системе. Не важно кто ты, какие у тебя планы и чего ты добился в жизни.
Главная ценность новой навязанной реальности становится ДЕЙСТВУЮЩИЙ QR-код. Без него ты ничто, а с ним тебе дают ПРАВО (но не возможность) жить.
И глупо считать что такой инструмент контроля будет действовать, как первоначально объявляют, всего полгода. От такого "ошейника" не откажется ни одно руководство.
В начале на QR-код навешивается ковидная вакцинация, затем подтянут другую "заботу о гражданах". Пока это дело бесплатное, но как известно, что бы подсадить человека на зависимость его надо бесплатно угостить, а потом уже можно и деньги стричь. А дальше хочешь полноценно жить - плати по списку.
Потом к QR-кодам можно и налоги подключить, оплату кредитов, квартплату. Намерения ведь благие, народ поддержит.
С развитием скорости обработки информации дойдет и до "заботы о личности". Не так личность развивается: не то пишет, не то говорит, не так думает - Qr-кодик можно и приостановить, закрыть везде доступ, заблокировать счета до визита в Банк в который не пустят без QR-кода.
И всё - фенита ля комедия в самозаключении пока не исправишься.
Можно вспомнить фильм Враг государства. Там фантастически одним подходом к компьютеру
переписывали и ломали жизнь героя.
Будущее наступило. Теперь это реальность. Достаточно устроить мелкий "сбой" и если это не массово то никто даже и не заметит.
И наивно думать что добропорядочного гражданина это не коснется. Гражданин добропорядочный лишь до тех пор пока "порядок" не переписан ;)


Над созданием вакцины против COVID-19 работают ученые, врачи, производители и спонсоры со всего мира. Всемирная организация здравоохранения координирует участников. Рассказываем, что известно о разрабатываемых вакцинах против нового коронавируса, кто их создает и кто может получить иммунизацию первым.
Что такое вакцинация?
По определению Всемирной организации здравоохранения, вакцинация — это простой, безопасный и эффективный способ защиты от болезней до того, как человек вступит в контакт с их возбудителями. Вакцинация задействует естественные защитные механизмы организма для формирования устойчивости к ряду инфекционных заболеваний и делает иммунную систему сильнее.
Существует несколько способов вызвать иммунный ответ в организме человека. У каждого из них есть свои преимущества и недостатки. Если вакцина одного типа не пройдет испытания на эффективность и безопасность, есть шанс, что сработает другой способ.
Иммунизация является испытанным инструментом для борьбы с инфекционными болезнями, представляющими угрозу для жизни, и их ликвидации. По оценкам ВОЗ, иммунизация позволяет ежегодно предотвращать от 2 до 3 миллионов случаев смерти.
Когда появились вакцины?
Современное понятие вакцинации было введено британским врачом Эдвардом Дженнером в конце 18 века. К 1900 году существовало две человеческие противовирусные вакцины — против оспы и бешенства — и три бактериальные вакцины — против тифа, холеры и чумы. В прошлом веке также были созданы вакцины против коклюша, дифтерии, столбняка, туберкулеза, полиомиелита, краснухи и некоторых других инфекционных заболеваний.
В 1979 году Всемирная ассамблея здравоохранения объявила победу над оспой. Это достижение остается одной из величайших побед общественного здравоохранения в истории.
График ниже показывает уровень смертности от наиболее распространенных инфекционных заболеваний, которые можно предотвратить с помощью вакцинации, в период с 1990 по 2017 годы.
Сверху вниз: туберкулез, корь, коклюш, гепатит В, менингит, вызванный гемофильной инфекцией, столбняк, менингококковый менингит, желтая лихорадка, дифтерия.
Сколько времени занимает разработка вакцин?
Разработка вакцин — как правило, длительный процесс. Например, вакцина от вируса Эбола, который существует уже 43 года, была одобрена лишь в прошлом году. Вакцина против Эболы создана за рекордные пять лет. При этом выпуск первой партии ожидается лишь в третьем квартале 2020 года. Хотя исследования экспериментальной вакцины против этого вируса Эбола в 2015 году и в 2019 году продемонстрировали высокий профилактический эффект. Тем не менее эксперты ВОЗ заявили о необходимости оценки дополнительных вакцин.
Процесс испытания вакцин
После создания вакцины ученые начинают тестировать ее на животных. Обычно это грызуны и приматы. Этот этап называется стадией доклинических испытаний. Он должен выявить наличие иммунного ответа и первичную безопасность препарата. Обычно доклинические испытания длятся от трех месяцев до полугода.
Затем ученые приступают к клиническим испытаниям — исследование влияния вакцин на организм людей. Они занимают много времени, а пропускать их ни в коем случае нельзя.
Первая фаза клинических испытаний предполагает иммунизацию небольшого количества людей для проверки безопасности и выявления необходимой дозировки для получения иммунного ответа.
Вторая фаза клинических испытаний предполагает иммунизацию людей разной возрастной группы. На детей, взрослых и пожилых людей вакцина может действовать по-разному. Эти испытания дополнительно проверяют безопасность и иммуногенность вакцины.
В ходе третьей фазы клинических испытаний прививку получают тысячи людей. Другая группа получает плацебо. Наблюдения за состоянием здоровья добровольцев из обеих групп показывают уровень заболеваемости и степень защиты вакцины от инфекции.
Даже ускоренные клинические испытания занимают минимум шесть месяцев. За состоянием здоровья иммунизированной группы нужно наблюдать год-полтора, чтобы выявить все побочные эффекты и проверить эффективность препарата.
Финальный этап производства вакцин включает в себя детализированное тестирование. Оно необходимо для того, чтобы убедиться, что вакцина соответствует всем критериям. Кроме того, всегда существуют проблемы доступа к необходимым для производства технологиям.
Существуют ли вакцины против других коронавирусов?
Считалось, что коронавирусы, поражающие человека, за исключением тяжелого острого респираторного синдрома (SARS-CoV), обнаруженного в ноябре 2002 года в Китае, в основном вызывают легкие инфекции верхних дыхательных путей. По этой причине циркуляция коронавирусов не контролировалась, а разработке вакцин и препаратов против не уделялась такого внимания, как в случае с SARS-CoV-2.
Попытки создать вакцину предпринимались группами китайских и американских ученых. Они считали, что разработка вакцины против SARS-CoV крайне важна, так как эпидемия может повториться в будущем.
Вакцины от других штаммов коронавируса пока не существуют.
Вакцины против COVID-19
В феврале глава ВОЗ Тедрос Гебрейесус заявил, что вакцина против коронавируса может быть готова через 18 месяцев. Если спасение от заболевания действительно создадут к середине следующего года, вакцина станет самой быстро разработанной в истории.
По состоянию на 9 июня, в создании вакцины против нового коронавируса участвуют 136 организаций. 10 из них находятся на стадии клинических исследований.
В разработке находятся РНК- и ДНК-вакцины, субъединичные рекомбинантные, живые аттенуированные вакцины и вакцины на основе вирусных векторов. Наилучший потенциал с точки зрения темпов разработки имеют РНК- и ДНК-вакцины, за которыми следуют субъединичные рекомбинантные вакцины.
Стратегическая консультативная группа экспертов (СКГЭ) ВОЗ в области иммунизации проводит анализ имеющейся доказательной базы, чтобы оценить ход разработки кандидатных вакцин против COVID-19 и предоставить рекомендации относительно возрастных групп, в которых оптимально проводить вакцинацию.
Кроме того, СКГЭ даст рекомендации в отношении политики ускоренного использования вакцин (до и после их регистрации), рекомендации по распределению вакцин на ранних этапах, когда объем производства еще будет ограничен, а также руководящие принципы обеспечения справедливого доступа к вакцинации.
Виды вакцин против COVID-19
Вакцины на основе ослабленного вируса (живые)
Что это? В живых вакцинах используются ослабленные штаммы вирусов. Этот вид вакцины вызывает иммунный ответ, не вызывая заболевания. Вакцины на основе ослабленного вируса создаются с 1950-х годов. После введения вакцины в организм ослабленный вирус начинает размножаться и вызывает иммунный ответ.
Преимущества. Большинство привитых живыми вакцинами переносят прививку без выраженных клинических симптомов. Вирусные вакцины вызывают самый стойкий иммунитет.
Недостатки. Живые вирусные вакцины часто нуждаются в тщательном тестировании на безопасность. Некоторые живые вирусы могут передаваться человеку, который не был иммунизирован. Это касается людей, у которых ослаблена иммунная система. Они также могут мутировать и вызвать болезнь.
Разработчики. Разработкой живой вирусной вакцины занимается индийская компания Codagenix, австралийский Университет Гриффита, Центр исследований инфекций Германии и несколько других. Разработка живых вакцин находится на стадии доклинических исследований.
Инактивированные вакцины
Что это? В инактивированных вакцинах используется неспособная заражать клетка вируса. Такие прививки используются для профилактики гриппа, гепатита А и бешенства. Они вызывают иммунный ответ, но не инфекцию.
Преимущества. Инактивированные вакцины безопаснее живых, так как в них нет ослабленного вируса, который может мутировать.
Недостатки. Однако инактивированные вакцины могут не обеспечить такую же защиту, как живые вакцин. Этот тип вакцины часто требует повторных инъекций с увеличением дозы.
Разработчики. Над созданием инактивированный вакцины работают компания Sinopharm совместно с Уханьским институтом биопрепараторов и Пекинским институтом биологических продуктов, китайская компания Sinovac и Институт медицинской биологии совместно с Китайской академией медицинской науки
Вакцину компании Sinopharm получили более 2000 человек. По заявлению разработчиков, препарат может появиться на рынке уже к концу 2020 года.
Китайская биофармацевтическая компания Sinovac Biotech находится на второй стадии испытаний вакцины. В ней приняли участие более 1000 добровольцев. Заключительную фазу испытаний могут провести в Великобритании.
Векторные вакцины
Что это? Векторные вакцины создаются на основе совершенно других вирусов, в которые встроен участок генома SARS-CoV-2. Они являются транспортом для доставки нужного вируса в клетки организма.
Преимущества. Векторные вакцины демонстрируют высокую эффективность переноса ДНК бактерии из одной клетки в другую и повышают клеточный иммунитет. Векторные вакцины легко производить, а проверка препаратов на безопасность не требует серьезных усилий.
Недостатки. Тем не менее, существует риск интеграции вируса в геном хозяина, что может привести к развитию заболевания. Кроме того, векторные вакцины плохо изучены и ни одна подобная вакцина не была одобрена для людей.
Разработчики. Векторные вакцины разрабатываются Оксфордским университетом и китайской компанией CanSino Bio совместно с Пекинским биотехнологическим институтом. Обе вакцины находятся на второй фазе клинических испытаний.
Генно-инженерные вакцины
Что это? Этот тип вакцины использует генно-инженерную РНК или ДНК, которая имеет инструкции для создания копий белка, которые вызывают иммунный ответ на вирус.
ДНК-вакцины содержат информацию по созданию вирусного белка, которая после попадания в клетку станет частью генома хозяина. Клетки человека начнут вырабатывать белки-патогены или антигены, что вызовет иммунную реакцию человека.
Преимущества. ДНК-вакцины просто и быстро изготавливаются, устойчивы к высоким температурам по сравнению с традиционными вакцинами и могут применяться для профилактики и лечения болезней. Кроме того, они не содержат в качестве вируса-носителя SARS-CoV-2. Нет опасности, что вирус мутирует и снова будет вызывать болезнь.
Недостатки. ДНК-вакцины вызывают слабую иммуногенность (способность вызывать иммунный ответ). Кроме того, необходимо введение повторных вакцин высокими дозами ДНК.
Разработчики. Над созданием ДНК-вакцины работает американская компания Inovio Pharmaceuticals. Эта вакцина находится в первой фазе разработки. Клинические испытания на людях должны начаться в июне в Китае и Южной Корее. За состоянием добровольных участников планируется наблюдать в течение 52 недель.
РНК-вакцины содержат вирусную молекулу — матричную РНК (мРНК). В отличие от ДНК-вакцин, мРНК-вакцины не встраиваются в клеточный геном. Молекула вируса попадает в организм, после чего клетки организма начинают синтезировать вирусные белки.
Преимущества. Главное преимущество РНК-вакцин — их способность вызывать более сильный иммунный ответ. Это позволяет уменьшить вводимую дозу вакцины.
Недостатки. Это совершенно новая вакцина. Специализированных требований к качеству и доклиническим исследованиям безопасности и иммуногенности РНК-вакцин в настоящее время не разработано ни в одной стране мира.
Разработчики. Над созданием РНК-вакцины работает американская компания BioNTech. Первые участники исследования уже получили инъекцию в Германии.
Американская компания Moderna в сотрудничестве с Научно-исследовательским центром вакцин также работает над созданием РНК-вакцины. Компания уже начала испытывать вакцины на участниках в возрасте 18−55 лет. За состоянием их здоровья будут наблюдать в течение 13 месяцев.
На нынешней стадии разработки будут выявлены безопасность, реактогенность и иммуногенность. Участники получат две дозы прививок с интервалом в четыре недели. Третья фаза испытаний должна начаться в июле.
Кто получит вакцину первым?
Очевидно, когда вакцина будет создана, ее не смогут получить одновременно все 7,8 миллиардов человек. Производителям и разработчикам придется выбрать, кто получит вакцину первым.
Эксперт по биотехнологиям Университета Хопкинса Джонатан Морено считает, что первыми вакцину должны получить уязвимые перед вирусом группы населения. Как показывает статистика, чаще всего новый коронавирус вызывает тяжелые последствия у пожилых людей, людей с диабетом и гипертонией. Для иммунизации пожилых от COVID-19 вакцина должна показать свою эффективность на этой группе населения, что не всегда возможно.
Кроме того, ученые все еще пытаются выяснить, какую роль играют дети в качестве переносчиков вируса. Возможно, правильнее было бы вакцинировать людей тех возрастных групп, которые, может быть, не так остро нуждаются в вакцине, как пожилые, но могут защитить более уязвимые слои населения, будучи защищенными сами.
Некоторые исследования показывают, что смертность от COVID-19 выше среди отдельных расовых и этнических групп. Возможно, это связано с уровнем экономического благополучия этих слоев населения. В таком случае, развивающиеся страны со слабой системой здравоохранения и недостаточной инфраструктурой будут острее нуждаться в вакцинах.
Тогда возникает вопрос транспортировки вакцин в эти страны в надлежащих условиях. Но до тех пор, пока вакцина против COVID-19 не выбрана, никто не знает, какая температура будет оптимальной для транспортировки вакцин и как обеспечить непрерывную холодовую цепь в доставке препаратов в пункты их назначения.
Основатель Microsoft Билл Гейтс в интервью изданию BBC отметил, что первыми вакцину от нового коронавируса должны получить медицинские работники стран, в которых эпидемия продолжается. Затем вакцину должны получить сотрудники жизненно важных сфер, такие как полицейские или пожарные, считает Билл Гейтс.
Он добавил, что если вакцина покажет свою эффективность и безопасность на пожилых людях, можно будет приступить к иммунизации уязвимых слоев населения (престарелых, бездомных, заключенных), которые подвержены высокому риску инфицирования.
По словам Гейтса, фармкомпании дают свое согласие на использование их мощностей для производства вакцины в случае, если их разработки не получат одобрения. Кроме того, планируется построить новые заводы для увеличения производства.
Будет ли вакцина бесплатной или доступной для развивающихся стран?
Более 140 мировых лидеров и экспертов 14 мая подписали коллективное письмо с призывом сделать вакцину против коронавируса бесплатной для всех людей во всех странах. А также гарантировать бесплатные диагностику, тестирование и лечение от коронавируса для всего мира.
Кроме того, супруги Гейтс открыли фонд, который займется приобретением вакцины от коронавируса для бедных стран, заявил предприниматель изданию BBC.
Окончательный ответ станет известен лишь после одобрения вакцины одного из кандидатов.
Развивается ли иммунитет у людей, переболевших коронавирусом?
Однозначного ответа пока нет, т.к. SARS-CoV-2 циркулирует в популяции людей всего несколько месяцев. Но вирус оставляет свой след в организме. Его можно обнаружить специальными тестами на антитела.
Как долго вакцина от SARS-CoV-2 защищает человека? Означает ли выработка иммунитета, что человек защищен на всю жизнь?
Подобные свойства вакцины выявляются в ходе исследований. Это станет известно после создания вакцины и после более длительных наблюдений за переболевшими коронавирусом людьми.
Мутирует ли вирус SARS-CoV-2? Если да, сможет ли вакцина защитить от мутировавшего коронавируса?
Сам вирус не мутирует. Человечество вырабатывает к нему коллективный иммунитет. Чем больше резервуаров (человеческих тел) пропускает вирус, тем менее выражена болезнь. Сама ДНК-структура вируса остается таким же, поэтому вакцина будет действовать на вирус.
Фото: личный архив
Клиническое исследование лекарственного препарата - изучение диагностических, лечебных, профилактических, фармакологических свойств лекарственного препарата в процессе его применения у человека, животного, в том числе процессов всасывания, распределения, изменения и выведения, путем применения научных методов оценок в целях получения доказательств безопасности, качества и эффективности лекарственного препарата, данных о нежелательных реакциях организма человека, животного на применение лекарственного препарата и об эффекте его взаимодействия с другими лекарственными препаратами и (или) пищевыми продуктами, кормами. (Федеральный закон от 12.04.2010 N 61-ФЗ "Об обращении лекарственных средств" Статья 4 Пункт 41)
Клинические исследования во всем мире являются неотъемлемым этапом разработки препаратов, который предшествует его регистрации и широкому медицинскому применению. В ходе клинических исследований новый препарат изучается для получения данных о его эффективности и безопасности. На основании этих данных уполномоченный орган здравоохранения принимает решение о регистрации препарата или отказе в регистрации.
Обычно выделяют четыре фазы клинических испытаний. Фаза I. Цель этапа — убедиться, что препарат можно применять у людей. Фаза II. Цель этапа — дополнительно оценить безопасность лекарства и выяснить, работает ли препарат. Фаза III. Цель этапа — сравнить новый препарат со стандартным лечением. Фаза IV называется постмаркетинговой — этот этап клинического испытания начинается, когда готовое лекарство уже поступает в продажу.
Существует государственный реестр лекарственных средств, который содержит перечень лекарственных препаратов, прошедших государственную регистрацию (Федеральный закон от 12.04.2010 N 61-ФЗ "Об обращении лекарственных средств" Статья 33), другими словами реестр разрешений на проведение клинических исследований (РКИ).
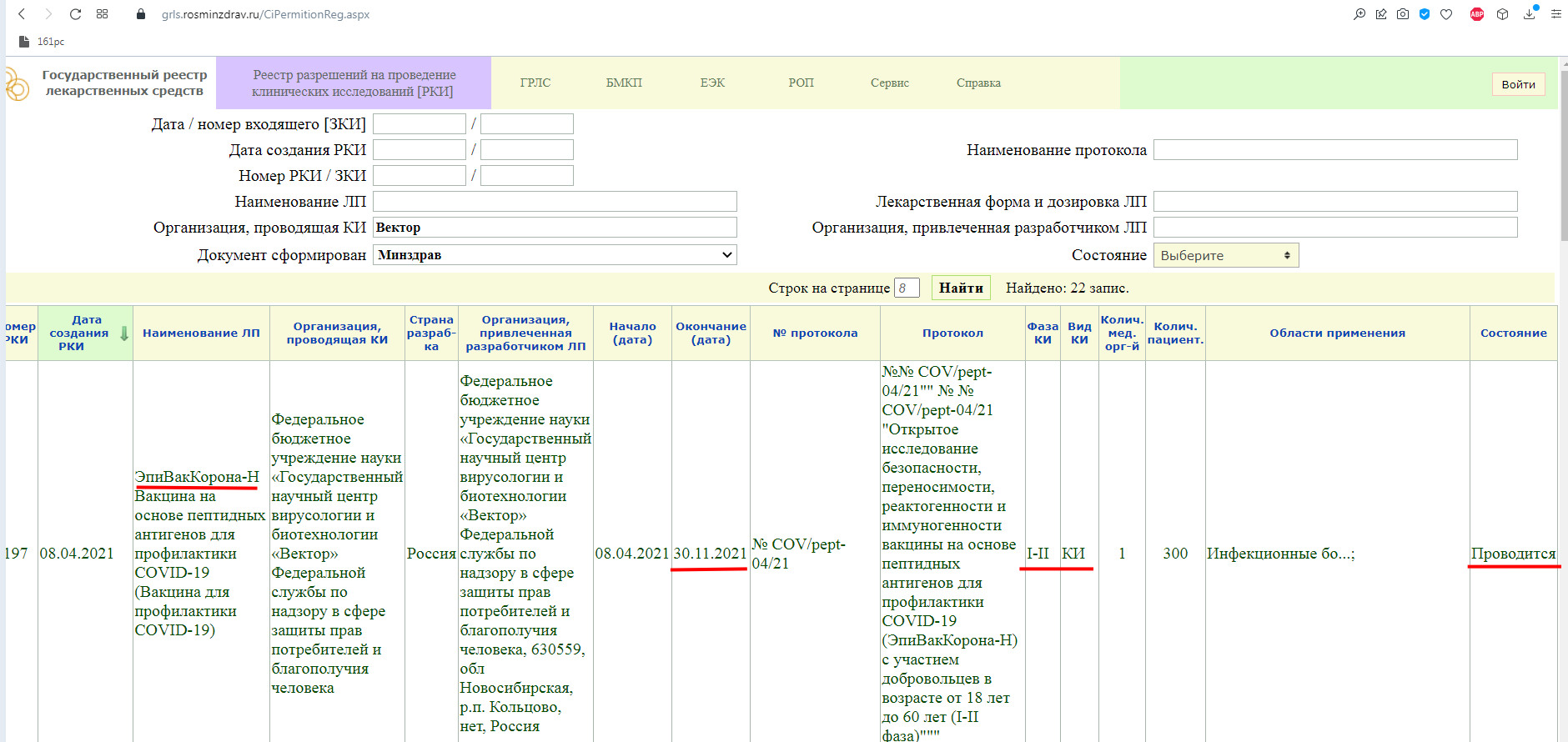
Как мы видим, в настоящий момент, проводится фаза клинического исследования 1-2 с участием добровольцев от 18 до 60 лет, и завершится она 30 ноября 2021 года.

Так же, проводится фаза клинического исследования 3-4 с участием добровольцев от 18 лет, и завершится она 31 августа 2021 года.


Завершенная фаза 3 клинического исследования, с участием добровольцев от 60 лет, и завершилась она 15 мая 2021 года.
Фаза клинического исследования 1-2 с участием добровольцев от 18 до 60 лет, проводится до 30 декабря 2021 года.

Тут так же видно, что проводится фаза клинического исследования 3 с участием добровольцев от 18 до 60 лет, и завершится она 30 декабря 2022 года.
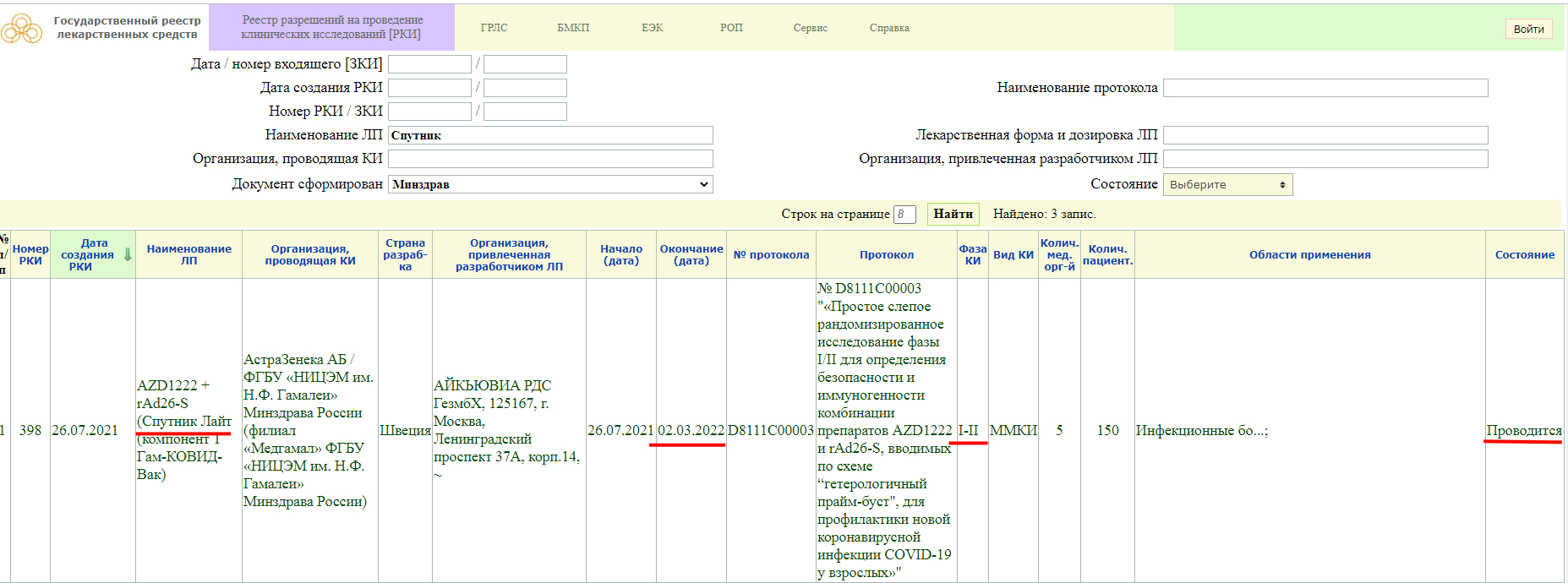
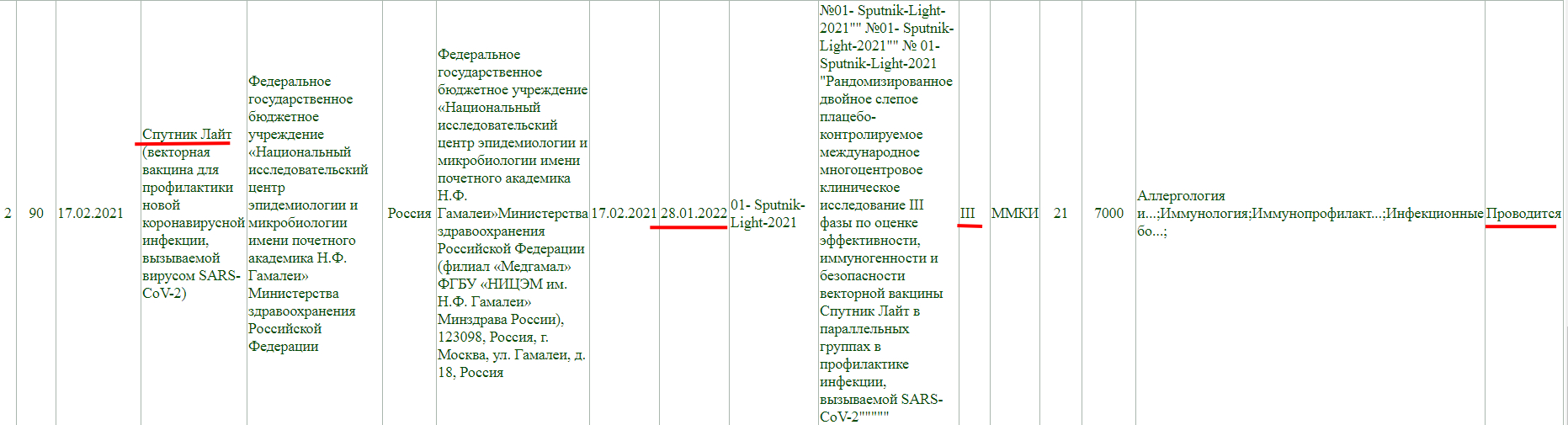
Так же, проводится фаза клинического исследования 3, и завершится она 28 января 2022 года.

Фаза клинического исследования 1-2, проводится до 31 декабря 2021 года.

Как и у остальных, клинические исследования не завершены, и в настоящий момент проводится фаза 3 с участием добровольцев от 18 до 60 лет, а завершится она 30 декабря 2022 года.
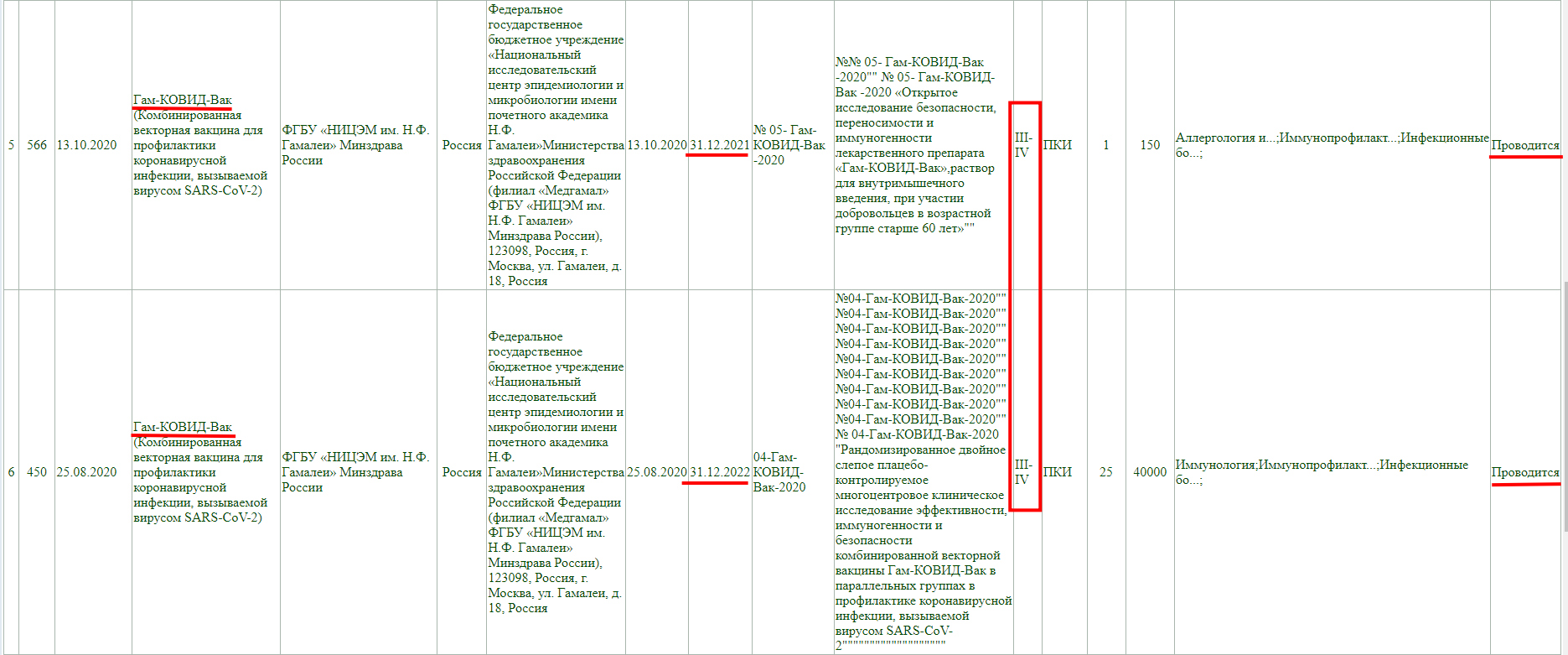
Тут аналогично, клинические исследования не завершены, проводится фаза 3-4, и завершится она 30 декабря 2022 года.
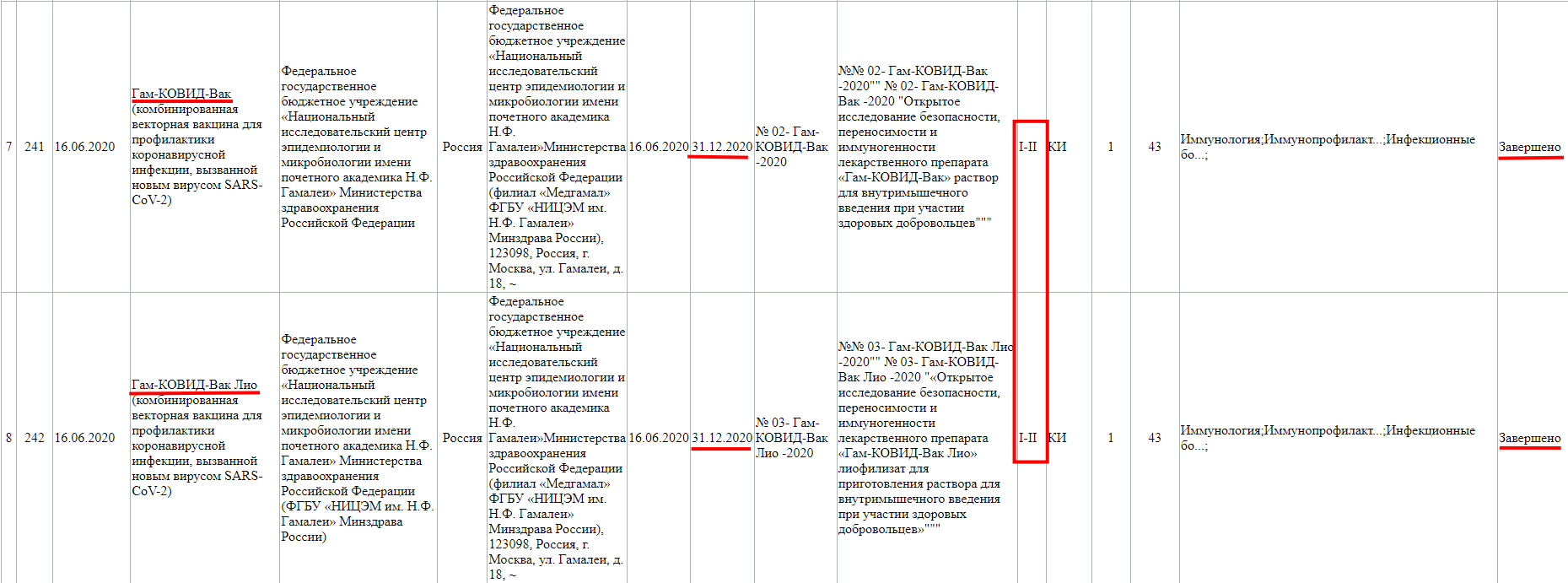
А тут клиническое исследование завершено, но только фазы 1-2.
И в завершение, по данным ВОЗ на 14 марта 2021 г., российские вакцины против COVID-19, в перечне безопасных и эффективных, отсутствуют.
-
Введите свой электронный адрес, после чего выберите любой удобный способ оплаты годовой подписки
Читайте также:
- Можно ли привлечь к уголовной ответственности за невозврат долга по расписке
- Как изменить время записи в гибдд через госуслуги если оплачена госпошлина
- Коррупция негативно влияет на правопорядок воздействует на него как дестабилизирующий фактор
- Через какое время можно делать рефинансирование кредита в плюс банке
- Партийное поручение что это

