Какие фазы сканирования включает мультифазный протокол исследования почек
Обновлено: 01.05.2024
Использование современных ультразвуковых технологий позволяет не только определить размеры и структуру органов, но и изучить особенности органной гемодинамики. Последнее обстоятельство имеет большое диагностическое и прогностическое значение для детей с острой почечной недостаточностью, когда использование традиционных урорентгенологических методов оценки состояния почек невозможно. Острая почечная недостаточность - одно из основных проявлений гемолитико-уремического синдрома - в значительной степени обусловливает тяжесть состояния больных и определяет прогноз заболевания.
Небольшие размеры ребенка, невыраженность подкожно-жировой клетчатки создают оптимальные условия для использования ультразвуковой техники с целью изучения ренальных структур и ренальной гемодинамики у данной группы больных. Неинвазивность и безвредность метода позволяют проводить динамический контроль за состоянием почек у детей любого возраста.
Цель исследования - определение особенностей ренальной гемодинамики у детей младшей возрастной группы (до 3 лет) при неосложненном течении гемолитико-уремического синдрома методом дуплексного допплеровского сканирования.
Материалы и методы
Выполнено 136 исследований почек у 28 детей с неосложенным течением гемолитико-уремического синдрома. Ультразвуковое исследование (УЗИ) включало в себя сканирование в В-режиме и допплеровское исследование ренального кровотока (дуплексное допплеровское сканирование в режиме цветового допплера и допплерография ренальных сосудов на всех визуализируемых уровнях). Исследование повторялось в динамике в зависимости от клинического состояния ребенка и эхографической картины. Результаты УЗИ сопоставлялись с клинико-лабораторными данными.
Результаты исследования
Для ангиотромботической фазы характерно резкое обеднение ренального кровотока. Обычно удается визуализировать только магистральные и сегментарные почечные сосуды, иногда - начальные отделы интерлобарных ветвей (рис. 1а). Для почки здорового ребенка того же возраста (рис. 1б) характерна возможность визуализации кровотока вплоть до субкапсулярного уровня, хорошо визуализируется кортикальный кровоток.
Рис. 1. Сравнение ренального кровотока при дуплексном допплеровском сканировании у больного гемолитико-уремическим синдромом и здорового ребенка того же возраста.
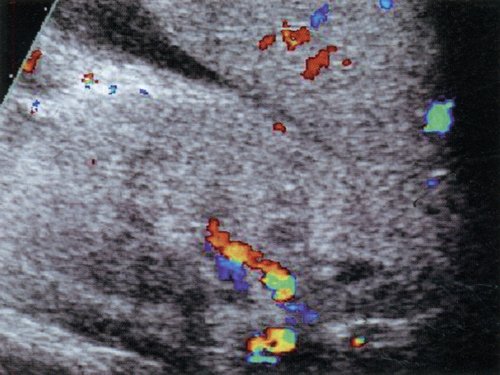
а) Дуплексное допплеровское сканирование почки здорового ребенка трех лет.
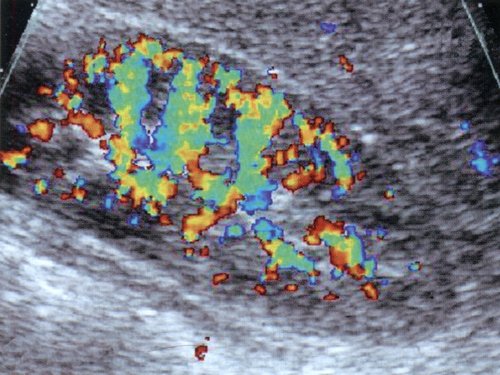
б) Дуплексное допплеровское сканирование почки ребенка с гемолитико-уремическим синдромом.
Принципиальное значение имеет оценка ренального кровотока в динамике сердечного цикла. В норме кровоток визуализируется на протяжении всего сердечного цикла, при этом обеднение его в диастолу соответствует снижению скорости кровотока при допплерографии (рис. 2а). Резистивный индекс RI составляет около 0,6. В ангиотромботической фазе гемолитико-уремического синдрома дуплексное допплеровское сканирование позволяет визуализировать кровоток только в систолическую фазу сердечного цикла. В диастолу кровоток в сосудах почки не определяется, что соответствует отсутствию антеградной диастолической составляющей ренального артериального кровотока (рис. 2б), соответственно, RI = 1,0. Реверсный диастолический артериальный кровоток в сосудах почки при дуплексном допплеровском сканировании определить не удается из-за его малой скорости, однако, при допплерографии реверсный кровоток четко прослеживается, RI может достигать 1,2.
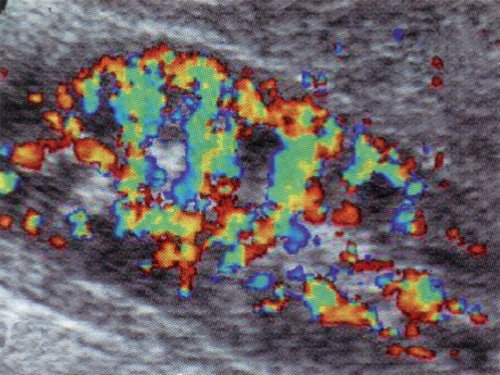
а) Дуплексное допплеровское сканирование почки здорового ребенка в фазу систолы сердечного цикла.
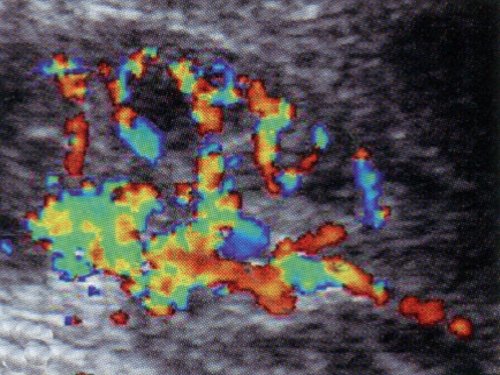
б) Дуплексное допплеровское сканирование почки здорового ребенка в фазу диастолы сердечного цикла.
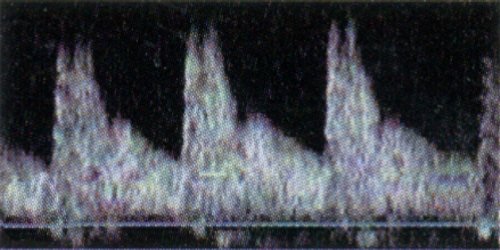
в) Допплерография на уровне сегментарной артерии почки здорового ребенка.
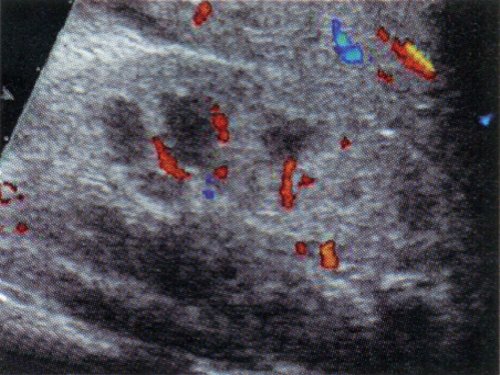
г) Дуплексное допплеровское сканирование почки больного гемолитико-уремическим синдромом в фазу систолы.
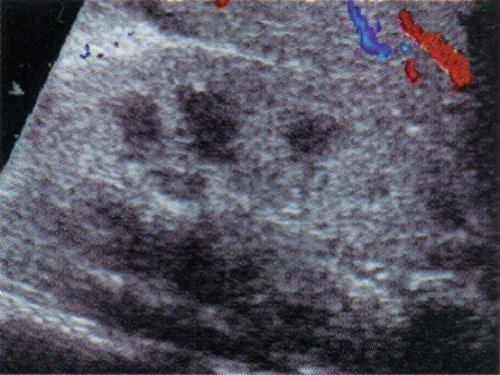
д) Дуплексное допплеровское сканирование почки больного гемолитико-уремическим синдромом в фазу диастолы.
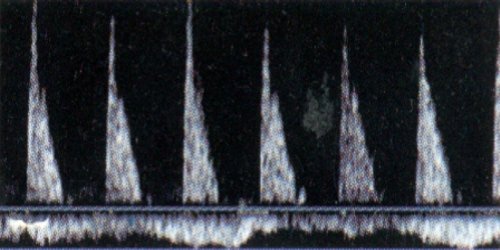
е) Допплерография на уровне сегментарной артерии почки больного гемолитико-уремическим синдромом.
В некоторых случаях при присоединении сердечной недостаточности (перегрузке правых отделов сердца) может определяться необычный характер движения крови в почечной вене, когда в систолу кровь в ней движется из почки, а в диастолу венозная кровь поступает в почку. Это четко прослеживается при дуплексном допплеровском сканировании и допплерографии (рис. 3).
Рис. 3. Необычный паттерн венозного опока из почки (уровень ствола почечной вены) у больного гемолитико-уремическим синдромом.
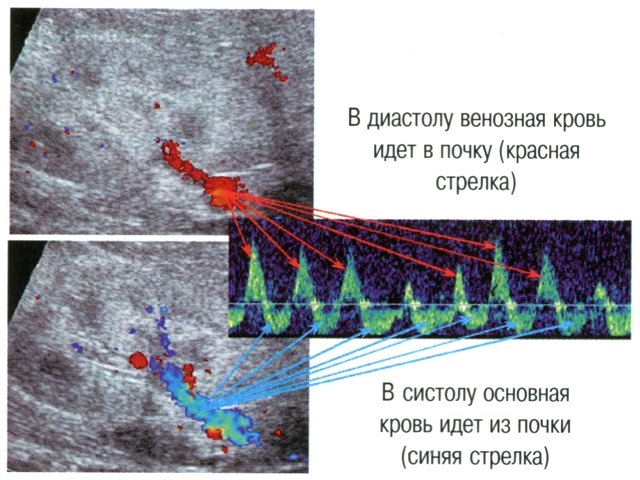
В диастолу венозная кровь идет в почку (красная стрелка), в систолу основная кровь идет из почки (синяя стрелка).
По мере развития патологического процесса, при переходе заболевания в фазу "глаукомы" почки, кровоток в ней существенно изменяется. Сначала появляется большее количество визуализируемых интерлобарных сосудов (диастолический антеградный компонент артериального ренального кровотока обычно еще полностью не восстанавливается (рис. 4). Позднее происходит полное восстановление диастолической антеградной составляющей ренального артериального кровотока на уровне магистральных, сегментарных и интерлобарных артерий, однако дуплексное допплеровское сканирование показывает отсутствие кровотока в кортикальном слое почки (рис. 5). Клинически эта сонографическая картина соответствует сохраняющейся высокой азотемии, анурии. Через 2-5 дней после восстановления резистивных характеристик артериального кровотока дети обычно начинали мочиться самостоятельно, однако азотемия сохранялась (еще 3-10 дней), и дети продолжали нуждаться в проведении диализа.
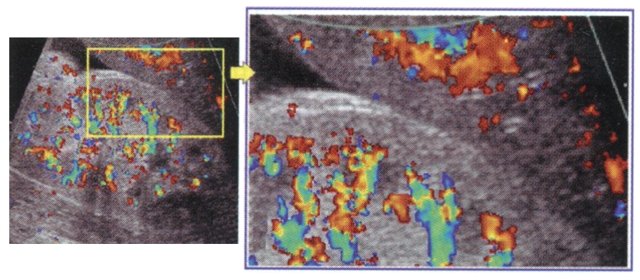
а) Дуплексное допплеровское сканирование почки - восстановление кровотока в медуллярном слое при сохранении ишемии кортикального слоя паренхимы.
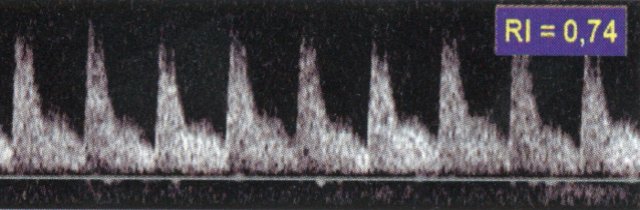
б) Допплерография почки в эту фазу заболевания.
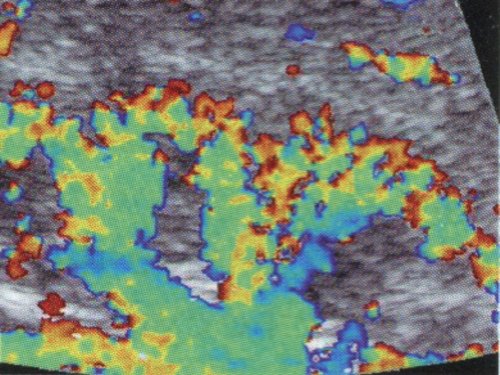
а) Дуплексное допплеровское сканирование почки в фазу систолы.
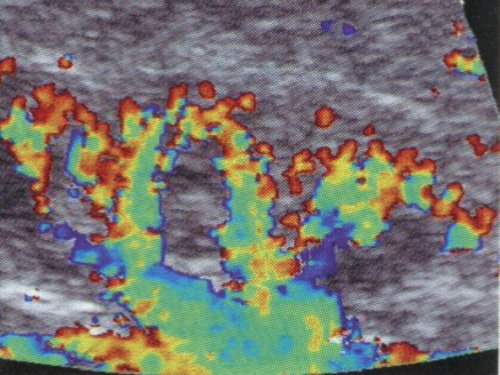
б) Дуплексное допплеровское сканирование почки в фазу диастолы.
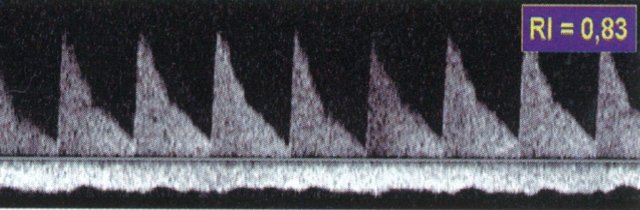
в) Допплерография на уровне интерлобарной артерии почки.
Подобная эхографическая картина имела место в начале заболевания у 6 детей. Клинически у этих детей анурии не было, но высокий уровень азотемии потребовал проведения диализа у 3 из них. В дальнейшем, в эхографической стадии репарации почек происходит постепенное восстановление кровотока в кортикальном слое почек, при этом резистивный индекс может значительно повышаться. К моменту клинического выздоровления ребенка RI обычно остается повышенным.
В литературе имеется ограниченное число публикаций об использовании эхографии для оценки состояния ренальных структур и ренальной гемодинамики при гемолитико-уремическом синдроме. Описаны отдельные случаи кортикального некроза при гемолитико-уремическом синдроме, различные морфологические его варианты при эхографии в В-режиме [4,6]. Наиболее популярной и цитируемой работой относительно использования допплеровских технологий в оценке ренальной гемодинамики при гемолитико-уремическом синдроме является статья Н. Patriquin [8,9]. Данное исследование было выполнено только на основании допплерографии ренальных сосудов (без дуплексного допплеровского сканирования ренального кровотока), что, видимо, связано с классом используемой техники. Автором высказано мнение о возможности прекращения диализа при восстановлении RI до 0,7. Другие исследователи не располагают скольнибудь значительным собственным опытом работы с данным контингентом больных [5,7] и в значительной степени ограничиваются пересказом указанной статьи [10,11].
Проведенное нами исследование не позволяет полностью согласиться с существующим мнением относительно диагностической и прогностической значимости нормализации показателя RI. Несоответствие между результатами допплерографии и дуплексного сканирования, а именно - нормальные резистивные показатели артериального кровотока при его отсутствии в кортикальном слое почечной паренхимы, в совокупности с описанными клиническими проявлениями заболевания в этот период заставляют думать о развитии в этой фазе заболевания выраженного артерио-венозного шунтирования крови на юкста-медуллярном уровне. Подобный патофизиологический механизм объясняет нормализацию показателей периферического сопротивления при отсутствии кортикального кровотока, а также сохраняющуюся азотемию в этот период заболевания.
Таким образом, представляется неприемлемым утверждение о возможности прекращения диализа больным гемолитико-уремическим синдромом только на основании нормализации резистивных характеристик артериального ренального кровотока. Изменения ренальной гемодинамики при гемолитико-уремическом синдроме являются результатом совокупности патофизиологических механизмов, оказывающих противоположное влияние на регистрируемые нами резистивные показатели артериального ренального кровотока. Так, если отек и инфильтрация стенок сосудов и периваскулярных тканей в совокупности с тромбообразованием обусловливают повышение резистивных показателей [1,3,10], то артериовенозное шунтирование крови [2] эти показатели снижает.
Изменения венозного кровотока в почках практически не исследованы. Единичные упоминания о возможности его изменения у детей с пороками сердца не содержат конкретного цифрового материала и не сопровождаются клинической оценкой этой эхографической находки. По нашим наблюдениям, подобные изменения венозного оттока встречаются у детей со среднетяжелым и тяжелым течением гемолитико-уремического синдрома (анурия не менее 1 недели) и, видимо, свидетельствуют о декомпенсации возможностей венозной системы почек поддерживать постоянное тканевое давление внутри почечной паренхимы на протяжении сердечного цикла. Нам представляется целесообразным продолжать исследования венозного оттока из почек.

Компьютерная томография мочевыделительной системы включает в себя:
- КТ мочевыделительной системы (почки, надпочечники, мочеточники, мочевой пузырь (с мультиснимком или DVD)
- КТ исследование с оценкой структуры конкрементов мочевыводящей системы в режиме 2х энергий
Метод Dual Energy (с использованием двух рентгеновских трубок) позволяет оценить химический состав конкрементов мочевыводящих путей, что влияет на дальнейшую тактику лечащих врачей.
Показания:
- выявление рентгеноконтрастных конкрементов в проекции почек, мочеточников и мочевого пузыря.
- исследование с оценкой структуры конкрементов мочевыводящей системы
- почечная колика, мочекаменная болезнь в анамнезе
- воспалительное поражение почек и паранефральной клетчатки
- подозрение на опухоль надпочечников
- выявление сопутствующие изменений в органах малого таза и в верхних мочевых путях, осложнений с их стороны, а также исключение различных аномалий развития
- травмы органов мочевыводящей системы
Подготовка к исследованию:
До назначения томографии пациент сообщает врачу обо всех возможных аллергических реакциях, которые может вызвать введение йодосодержащего контрастного вещества.
Накануне вечером - легкий ужин (до 18.00мин), в день исследования не завтракать. Накануне вечером очистительная клизма, либо очистка кишечника раствором Фортранса (по инструкции). Исследование брюшной полости производится натощак. Если назначено КТ-исследование во второй половине дня, утром можно легко позавтракать, не обедать. Если пациенту выполнялось рентгеновское исследование пищеварительного тракта (пищевод, желудок, ирригоскопия) с бариевой взвесью - компьютерная томография может быть выполнена не ранее, чем 7 суток.
Для получения информативных результатов КТ при диагностике органов малого таза обязательное условие — наполненный мочевой пузырь. Не мочиться в течение 1 часа, а также выпить 1 литр воды за час до томографии;
Общие требования для КТ с контрастированием:
Для выполнения исследования необходимо иметь при себе результат анализа крови
на креатинин, срок давности не более 30-го дня со дня сдачи биоматериала.
Обязательно сообщите врачу-рентгенологу перед обследованием с контрастом:
- есть ли у вас аллергия на йод, лекарства и продукты питания
- страдаете ли вы диабетом, астмой, заболеваниями сердца или щитовидной железы
Методика исследования:
Исследование проводится лежа на спине (при необходимости может быть дополнено положением на животе или на боку), одежда должна быть без металлических предметов. Выполняется сканирование тела. КТ мочевыделительной системы без контрастного вещества длится до 1 минуты. При необходимости врач может попросить пациента задержать дыхание на несколько секунд.
Дозовая нагрузка – около 12 мЗв (зависит о массы тела пациента)
Объемные построения (реконструкции):
После окончания исследования проводится построение объемных реконструкций мочевыводящей системы и костных структур на уровне исследования (изображения в 3D или 4D, MPR (многоплоскостные реконструкции)) с цветовым выделением конкрементов.
Преимущества перед рентгенологическим исследованием и МРТ:
- КТ-исследование методом Dual Energy (с использованием двух рентгеновских трубок) позволяет оценить химический состав конкрементов мочевыводящих путей, что влияет на дальнейшую тактику лечащих врачей.
- быстрота выполнения исследования
- трехмерное и четырехмерное моделирование органов мочевой системы позволяют более наглядно оценить органы мочевыделительной системы
- возможность диагностировать рентгеноконтрастные конкременты, их плотность
- КТ-исследования пациентов с металлическими имплантатами (суставы, аппараты внутренней и наружной фиксации и пр.), в том числе и с наличием электрокардиостимулятора, выполняется в полном объеме
Недостатки исследования для диагностики конкретной патологии и локализации патологических изменений:

Направление пациентов на бесплатные консультации, обследования и лечение в рамках клинических исследований по изучению инновационных лекарственных препаратов

Доступ к инновационным препаратам
Наблюдение в процессе лечения
Что надо знать о клинических исследованиях?

Что такое клинические исследования
В клинической практике стало нормой использовать новейшие противоопухолевые препараты, которые в результате лечения онкологических больных показывают очень эффективные результаты. В соответствии с общепринятыми правилами новые препараты до их официальной регистрации могут быть доступны для больных только в рамках клинических исследований. Именно поэтому клинические исследования являются неотъемлемой частью в разработке новейших инновационных лекарственных препаратов. Абсолютно все клинические исследования проходят с соблюдением специальных международных правил - GCP (Good Clinical Practice). Следование этим правилам служит гарантией того, что права пациентов, которые участвуют в исследованиях, защищены, а их результаты достоверны.
Фазы клинических исследований
Прежде чем препарат допускается к клиническим исследованиям, ему всегда предшествует процесс изучения в лабораториях в пробирках, или на лабораторных животных. Если в ходе доклинических исследований получены положительные результаты по безопасности и эффективности, препарат допускается на стадию клинических исследований.
Клинические исследования проходят в несколько фаз.
| На первоначальной фазе экспериментальный препарат тестируется с участием небольшой группы пациентов - 20-30 больных. Врачи оценивают его токсичность, определяют безопасную дозировку, идентифицируют побочные эффекты. |
| Во второй фазе расширяется контингент участников эксперимента от 100 до 300 пациентов. Проверяется его эффективность при конкретном заболевании и подробно оцениваются риски применения. |
| В третьей фазе в исследовании принимают участие от нескольких сотен, до нескольких тысяч пациентов (от одной до трех и более), чтобы на большой группе больных подтвердить эффективность препарата при определенном заболевании, выявить возникающие побочные эффекты и сравнить со стандартными способами лечения. |
| На четвёртой, заключительном этапе, который, как правило, проводится уже после регистрации препарата, получают дополнительную информацию о его безопасности, эффективности и оптимальном применении. Кроме того, пациенты получают возможность бесплатно проходить обследования и лечение, которые согласуются с принятыми международными стандартами. |


Проведение Исследований
Рекомендации пациенту


Возможные риски и польза
Польза: качественно разработанные и проведенные клинические исследования для пациентов, соответствующих критериям для участия, позволяют получить доступ к инновационным препаратам и методам лечения, до того, как они станут широко доступными; получать высококвалифицированную медицинскую помощь в ведущих учреждениях здравоохранения в период проведения исследования; помочь другим, внося свой вклад в медицинские исследования.
Риски: существуют риски, связанные с клиническими исследованиями могут потребовать дополнительного времени и внимания по сравнению с обычным лечением, включая более частые визиты к врачу исследовательского центра, дополнительные приемы препаратов, пребывание в центре, ведение дневников приема препаратов или сложные схемы приема препаратов.
Также экспериментальное лечение может быть неэффективным для участника, могут возникать побочные эффекты экспериментального лечения. Перед участием в исследовании пациенту следует поговорить с врачом, оценить потенциальные риски и пользу, связанные с участием, однако, если всё удовлетворяете критериям отбора в исследование, окончательное решение об участии пациент должен принять самостоятельно.
Противоопухолевая лекарственная терапия, которая предлагается пациенту в рамках клинического исследования, всегда основана на международных стандартах по ведению пациентов с конкретным онкологическим заболеванием. Лечение проводится в отделениях клиники Московского научно-исследовательского онкологического института имени П.А. Герцена - филиале ФГБУ "НМИЦ радиологии" Минздрава России.
Урологическое отделение
Главный исследователь Проф. Алексеев Борис Яковлевич
Компания Ferring Код протокола 000108. Фаза: III
Отделение лекарственной терапии
Главный Исследователь Феденко Александр Александрович
Исследование III фазы с целью сравнения комбинации пемпролизумаба с химиотерапией и комбинации плацебо с химиотерапией препаратами платины в качестве неоадьювантной терапии, и сравнения пемпролизумаба с плацебо как адювантной терапии у пациентов с немелкоклеточным операбельным раком легкого стадии II, IIIA и IIIB (T3-4N2) стадии.
Исследование фазы 3 применения Бригатиниба в сравнении с Алектинибом у пациентов с распространенным ALK-позитивным немелкоклеточным раком легких, у которых возникла прогрессия заболевания на фоне применения Кризотиниба.
Местно-распространенный или метастатический ALK+ НМРЛ
Отделение лекарственной терапии
Главный исследователь Феденко Александр Александрович
Отделение лекарственной терапии
Главный исследователь Феденко Александр Александрович
Исследование II фазы для изучения монотерапии олапарибом у ранее получавших лечение пациентов с распространенными злокачественными опухолями, позитивными по мутациям генов, задействованных в репарации путем гомологичной рекомбинации (HRRm), или с дефицитом гомологичной рекомбинации (HRD)
“Долгосрочное наблюдательное исследование фазы 4 для оценки профиля безопасности препарата радия-223 дихлорид”
Компания МЕРК ШАРП И ДОУМ КОРП представительство ООО "МСД Фармасьютикалс". Протокол № 7339-001-00/ENGOT-ov43 (договор 2019/78). Фаза III
Рандомизированное, двойное слепое клиническое исследование III Фазы с целью сравнения комбинации химиотерапии c применением и без применения пембролизумаба, с последующим поддерживающим лечением олапарибом или плацебо в качестве первой линии терапии у пациенток с распространённым эпителиальным раком яичника без мутации гена BRCA.
Лечение (группы открыты):
Оценка эффективности стандартной химиотерапии по сравнению химиотерапии с препаратами пембролизумаб и олапариб.
Компания ООО "Инвентив Хелс Клиникал". Протокол № R2810-ONC-1676/GOG-3016 (дог.б/н). Фаза III.
Открытое рандомизированное клиническое исследование фазы 3 препарата REGN2810 по сравнению с химиотерапией, выбранной исследователем, у пациентов с рецидивирующей или метастазирующей карциномой шейки матки, рефрактерной к препаратам платины.
Лечение (группы открыты):
Оценка эффективности стандартной химиотерапии по сравнению химиотерапии с препаратом REGN2810.
Рандомизированное, двойное слепое, плацебо-контролируемое исследование 3 фазы препарата Кабозантиниб (XL184) у пациентов с дифференцированной карциномой щитовидной железы, устойчивой к терапии радиоактивный йодом, и прогрессированием заболевания после предшествующей VEGFR-таргетной терапии
Отдел лекарственного лечения злокачественных новообразований
Ответственный (главный исследователь): Фалалеева Н.А.
Координатор исследований Екатерина Тел. 8 (910) 520-46-08
Компания: Ф. Хоффман Ля Рош, Код протокола: BO40747 Фаза исследования: III
Пациенты: на ранних стадиях HER2- позитивного рака молочной железы
Лечение (набор пациентов длится): Рандомизированное двойное слепое плацебо-контролируемое исследование III фазы по оценке эффективности и безопасности атезолизумаба или плацебо в комбинации с неодьювантной терапией доксорубицином+циклофосфамидом с поcледующим применением паклитаксела +трастузумаба+пертузумаба на ранних стадиях HER2- позитивного рака молочной железы
Компания: ООО "К-Ресерч"/Транслейшнл Ресерч Ин Онколоджи Код протокола: CLEEE011O12301C Фаза исследования: III
Пациенты: с гормон рецептор-положительным, HER2- отрицательным ранним раком молочной железы
Лечение (набор пациентов длится): Многоцентровое, рандомизированное, открытое исследование 3 фазы по оценке эффективности и безопасности рибоциклиба с эндокринной терапией как адъювантная терапия у пациентов с гормон рецептор-положительным, HER2- отрицательным ранним раком молочной железы (Новое Адъювантное Исследование с Рибоциклибом LEE011: NATALEE)
Отдел лекарственного лечения злокачественных новообразований
Ответственный (главный исследователь): Фалалеева Н.А.
Координатор исследований Екатерина Тел. 8 (910) 520-46-08
Компания: ЗАО "БИОКАД" Код протокола: BCD -217-1/OBERTON Фаза исследования: II
Пациенты: с нерезектабельной или метастатической меланомой
Лечение (новый набор состоится ориентировочно в марте 2020г. ): Международное многоцентровое двойное слепое плацебо-контролируемое сравнительное рандомизированное исследование эффективности и безопасности терапии препаратом BCD-217 (анти-CTLA-4 и анти-PD-1) с продолжением терапии препаратом BCD-100 (анти-PD-1) в сравнении с монотерапией препаратом BCD-100 в качестве первой линии терапии пациентов с нерезектабельной или метастатической меланомой.
Отдел лекарственного лечения злокачественных новообразований
Ответственный (главный исследователь): Фалалеева Н.А.
Координатор исследований Екатерина Тел. 8 (910) 520-46-08
Компания: ЗАО "БИОКАД" Код протокола: BCD-100-5/FERMATA Фаза исследования: III
Пациенты: c распространенным раком шейки матки, c гистологически верифицированным плоскоклеточным раком шейки матки.
Лечение (набор пациентов длится): Международное рандомизированное двойное слепое клиническое исследование BCD-100 в комбинации с платиносодержащей химиотерапией с бевацизумабом или без него в сравнении с плацебо в комбинации с платиносодержащей химиотерапией с бевацизумабом или без него у пациенток с распространенным раком шейки матки.
Рандомизированное двойное слепое плацебо-контролируемое многоцентровое международное исследование III фазы дурвалумаба или комбинации дурвалумаба с тремелимумабом в качестве консолидирующей терапии у пациентов с локализованным мелкоклеточным раком лёгкого I-III стадии, у которых не произошло прогрессирование после одновременной химиолучевой терапии (ADRIATIC).
Многоцентровое рандомизированное двойное слепое плацебо-контролируемое исследование для оценки эффективности и безопасности канакинумаба по сравнению с плацебо в качестве адъювантной терапии у взрослых пациентов с немелкоклеточным раком легкого (НМРЛ) II-IIIA и IIIB (T>5 cм и N2) стадии по классификации AJCC/UICC, версия 8, после полной резекции (R0).
Рандомизированное двойное слепое плацебо-контролируемое многоцентровое исследование III фазы для изучения дурвалумаба в качестве консолидирующей терапии у пациентов с местнораспространённым нерезектабельным немелкоклеточным раком легкого (III стадии) без прогрессирования заболевания после радикальной химиолучевой терапии на основе препаратов платины (PACIFIC 5).
Многоцентровое рандомизированное, двойное слепое, плацебо-контролируемое исследование III фазы, проводимое с целью оценки эффективности и безопасности анаморелина гидрохлорида, применяемого для восполнения дефицита массы тела и лечения анорексии, развившихся на фоне распространенного немелкоклеточного рака легкого у взрослых пациентов.
Пациенты со II−III стадией рака молочной железы с тройным негативным фенотипом (TNBC).
Лечение (группы открыты): терапия атезолизумабом в комбинации с паклитакселом с последующим применением атезолизумаба, введением через сокращенные интервалы доксорубицина или эпирубицина (по выбору исследователя) или циклофосфамида (далее — атезолизумаб + T-AC/EC) по сравнению с применением паклитаксела с последующим введением через сокращенные интервалы доксорубицина или эпирубицина (по выбору исследователя) или циклофосфамида (далее — T-AC/EC).
Тема: Многоцентровое, рандомизированное, открытое исследование III фазы атезолизумаба (антитело к PD-L1) в комбинации с адъювантной химиотерапией на основе антрациклина/таксана в сравнении только с химиотерапией у пациентов с операбельным трижды негативным раком молочной железы
Неоадъювантная терапия пациентов с HER2 – положительным раком молочной железы ранней стадии
Еще совсем недавно ультразвуковой метод исследования был единственным, в котором не рассматривалось применение контрастных препаратов. Ультразвуковая цветовая допплерография считалась уникальной неинвазивной методикой исследования сосудов. С внедрением в практику ультразвуковых исследований контрастных агентов стало возможным изучать сосудистый рисунок, оценивать его характер, прослеживать фазы накопления и выведения контрастных препаратов, изучать гемодинамику. По сути, появилась определенная альтернатива контрастной компьютерной рентгеновской томографии.

А.В. Зубарев, С.В.Сальникова, А.А. Федорова, А.В. Ганина, С.О. Чуркина, А.П. Норкина
Кремлевская медицина клинический вестник №3/2017
Введение.
В качестве контрастного вещества при эхоконтрастировании почек используются микропузырьковые взвеси, которые получают при внутривенном введении в кровь пациента специальных газообразующих препаратов. Размеры микропузырьков не превышают размеры эритроцита и полностью безвредны для пациента. К тому же они не вызывают аллергических реакций в организме, у них отсутствует нефротоксичность, свойственная рентгеноконтрастным препаратам. Микропузырьки взаимодействуют с ультразвуковым сигналом и начинают резонировать и лопаться, обеспечивая контрастирование различных по морфологическому строению сосудов и органов. [1]
Сегодня эхоконтрастные препараты активно внедряются в повседневную практику и все шире используются врачами ультразвуковой диагностики, обеспечивая возможность проведения контрастного усиления по аналогии методикам контрастного усиления при КТ и МРТ. [2, 3, 4, 5, 6] В то же время, возможности эхоконтрастирования в диагностике заболеваний почек пока мало знакомы нашим клиницистам. Вероятно, поэтому своих пациентов они чаще направляют на конкурирующие высокоинформативные и затратные методы визуализации, например, КТ или МРТ, позволяющие провести комплексную оценку морфологии и функции почек. Однако, важно напомнить, что КТ исследование почек отягощено лучевой нагрузкой и нефротоксичностью йодного рентгеноконтрастного препарата [ 7 ].
Мы предприняли попытку на собственном клиническом материале показать возможности эхоконтрастирования в диагностике различных патологических состояний почек.
Материалы и методы:
За период с мая 2016 года по апрель 2017 года мы провели эхоконтрастирование почек у 27 пациентов. Критерием отбора пациентов для проведения эхоконтрастирования было наличие изменений в структуре и функции почек, визуализируемых при стандартном УЗИ почек. Перед введением эхоконтрастного препарата у каждого пациента получали информированное согласие по утвержденному протоколу. Возраст обследованных пациентов составлял от 31 до 64 лет, в среднем - 47 лет. У 13 пациентов подозревались кистозные образования почек, у 7- пиелонефрит, и еще у 7 – объемные солидные образования неясного, предположительно, злокачественного генеза. Результаты компьютерной и магнитно-резонансной томографии были доступны у 23 пациентов; 15 пациентам проводилось последующее патоморфологическое исследование после выполненных оперативных вмешательств.
Во время обычного ультразвукового исследования почек с применением методик серой шкалы и УЗ-ангиографии мы оценивали наличие патологических изменений в структуре и функции почек. После этого выявляли зону интереса. Стараясь не смещать датчик от области интереса, активировали на ультразвуковом сканере формат двойного экрана. В режиме двух экранов на ультразвуковом аппарате контрастное изображение почки отображалось параллельно и одновременно с соответствующим изображением почки в B-режиме.
При наличии в почке объемного образования эхоконтрастирование позволяет изучить характер сосудистого рисунка, оценить различные фазы контрастирования, выявить участки деструкции или распада ткани органа или опухоли.
Для предотвращения быстрого разрушения микропузырьков при сканировании мы использовали низкие показатели механического индекса (МИ визуализация. 2015;(1):94-114. [Zubarev A.V., Fedorova A.A., Chernishev V.V., Varlamov G.V., Sokolova N.A., Fedorova N.A. Application of Contrast Enhanced Ultrasound (Ceus) in the Clinic and Prospects of Synchronization Ultrasound, CT and MRI Images (Personal Experience and Literature Review). Medical Visualization. 2015;(1):94-114.
Demosthenes D. Cokkinos, Eleni G. Antypa, Maria SkilakakiContrast Enhanced Ultrasound of the Kidneys: What Is It Capable of? BioMed Research International Volume 2013, Article ID 595873, 13 pages
Jakobsen JA, Oyen R, Thomsen HS, Morcos SK; Members of Contrast Media Safety Committee of European Society of Urogenital Radiology (ESUR). Safety of ultrasound contrast agents. Eur Radiol 2005; 15: 941-945
Emilio Quaia Michele Bertolotto Vincenzo Cioffi Comparison of Contrast-Enhanced Sonography with Unenhanced Sonography and Contrast- Enhanced CT in the Diagnosis of Malignancy in Complex Cystic Renal Masses AJR 2008; 191:1239–1249 DOI:10.2214/AJR.07.3546
Robbin ML. Ultrasound contrast agents: a promising future. Radiol Clin North Am 2001; 39:399–414
Ashutosh Prakash, Gerald Jit Shen Tan, Gervais Khin-Lin Wansaicheong Contrast enhanced ultrasound of kidneys. Pictorial essayMedical Ultrasonography 2011, Vol. 13, no. 2, 150-156
J.-M. Correas, M. Claudon, F. Tranquart, and O. H´el´enon, “The kidney: imaging with microbubble contrast agents,” Ultrasound Quarterly, vol. 22, no. 1, pp. 53–66, 2006.
F. Piscaglia, C. Nolsøe, C. F. Dietrich et al., “The EFSUMB guidelines and recommendations on the clinical practice of contrast enhanced ultrasound (CEUS): update 2011 on nonhepatic applications,” Ultraschall in der Medizin, vol. 33, no. 1, pp. 33–59, 2012
Hélénon O, Correas JM, Balleyguier C, Ghoudani M, Cornud F. Ultrasound of renal tumors. Eur Radiol 2001; 11:1890–1901
Robbin ML, Lockhart ME, Barr RG. Renal imaging with ultrasound contrast: current status. Radiol Clin North Am 2003; 41:963–978

КТ с контрастированием – исследование, предполагающее использование рентгеновского излучения в минимальных дозах, а также сопровождающееся введением специального вещества для усиления контрастности здоровых и патологически измененных тканей.
Компьютерная томография (КТ) — один из самых эффективных и наиболее точных методов современной диагностики. В отличие от обычной рентгенографии, компьютерная томография позволяет получить объемное изображение исследуемой области организма. При этом толщина среза может составлять до 0,5 мм. При КТ тело визуализируется в поперечных срезах, что позволяет получать 3Д-изображения сложных структур. Обычная рентгенограмма — это двумерное представление трехмерной структуры. Часто бывает трудно разделить перекрывающие друг друга структуры на обычном снимке, например, в грудной клетке, а КТ эффективно устраняет эту проблему. Кроме того, КТ гораздо более чувствительна к различиям в плотности и может выявлять аномалии, не обнаруживаемые при обычной рентгенографии.
КТ с контрастом назначается далеко не в каждом случае использования методики компьютерной томографии. Этот способ обследования является очень точным, позволяя рассмотреть даже мельчайшие опухоли, тромбы и гематомы и применяется при необходимости детализации картины заболевания.
Вводя контрастный препарат внутривенно, мы отвечаем сразу на несколько вопросов: есть ли гипо- или гиперваскулярные опухоли в интересующей нас зоне и каковы ее размеры,
есть ли в ней некроз или кровоизлияние,
нет ли тромбозов , аневризм, инвазий сосудов,
нет ли нарушения целостности сосудистой стенки, нет транзиторных нарушений перфузии исследуемого органа.
КТ с контрастом выполняется в случаях, когда нужно очень четко разделять нормальные и аномальные структуры в человеческом организме. Такая дифференцировка достигается посредством усиления сигнала от больных тканей. Эффект контрастирования при КТ основывается на том, что большинство опухолей, особенно, злокачественных, кровоснабжается лучше, чем здоровые ткани. Поэтому контрастное вещество будет накапливаться в них, давая картину отличия от прочих тканей. Кроме того, контраст необходим для изучения состояния сосудов – вен, артерий. На снимках КТ контраст будет выделяться белым цветом, что позволит хорошо изучить этот участок.
КТ с контрастом и онкология
В большинстве случаев процедура рекомендуется при подозрении на онкологический процесс, либо для дифференцирования доброкачественной опухоли со злокачественной. Так, рекомендуется КТ с контрастным веществом при:
- Опухолях паренхиматозных органов брюшной полости и забрюшинного пространства (при раке почек, карциноме печени, поджелудочной железы, селезенки).
- Раке полых органов брюшной полости – кишечника, желчного пузыря.
- Образованиях грудной клетки – легких, средостения, сердца.
- Опухолях головного мозга и основания черепа.
- Новообразованиях опорно-двигательного аппарата.
Томография с контрастированием позволит различить банальную и часто встречающуюся кисту почки от почечно-клеточного рака или доброкачественной липомы, ангиомы. При изучении состояния печени КТ поможет дифференцировать цирроз печени, доброкачественные опухоли и гепатоцеллюлярный рак.
Применяется КТ с контрастным усилением при лимфомах – для отличия их от другого ракового заболевания (лимфогранулематоз) или от простого лимфаденита. Контрастирование позволит установить степень ракового заболевания, его распространенность, поражение регионарных лимфоузлов, наличие метастазов. Часто назначают КТ и при малигнизации доброкачественных опухолей, которая будет заметна по ряду специфических признаков (васкуляризация, увеличение в размерах и т.д.).
Компьютерная томография с контрастным усилением весьма информативна при диагностике внутри просветных тромбов, а также тромбированных аневризм, зон сужения тромбами аорты. Также контраст позволит детально изучить сосудистые мальформации, в том числе – перед оперативным вмешательством по поводу их удаления. Обследование даст полную картину при истончении стенок вен, варикозе глубоких вен и при тромбофлебите, а также при атеросклерозе артерий.
Компьютерная томография с контрастированием применяется при заболеваниях таких зон организма:
- Полых органов – желудка, кишечника, пищевода.
- Легких, бронхов и трахеи.
- Гортани и голосовых связок.
- Головного мозга, спинного мозга.
- Основания черепа.
- Всех отделов позвоночника.
- Костей.
- Челюстей.
- Носа и пазух.
Для процедуры применяются различные препараты – ионные и неионные, с содержанием йода. Именно йод повышает интенсивность изображения, при этом вред от его проникновения в организм практически отсутствует. Самыми распространенными являются ионные препараты, но неионные еще более предпочтительны (их токсичность равна нулю).
К ионным средствам относят - Метризоат, Диатризоат, Иоксаглат,
к неионным – Йопромид, Йопамидол, Йогексол и другие.
До введения препарата врач обязательно уточняет наличие некоторых заболеваний и состояний у пациента, которые могут стать противопоказаниями к процедуре.
До обследования пациент должен сдать ряд лабораторных анализов
(биохимия крови: мочевина (2,4-6,4 ммоль/л) и креатинин (мужчины старше 15 лет — 80-150 мкмоль/л, старше 60 лет — 71-115; женщины старше 18 лет — 53-97, старше 50 лет — 53-106).
При повышении указанных показателей проведение контрастирования не проводится. Количество контрастного вещества рассчитывается исходя из веса человека.
Есть разные способы введения контраста, основные из них таковы:
- Болюсный. При болюсном способе введения в локтевую или другую вену устанавливается шприц-инжектор, у которого нормируется скорость подачи препарата.
- Внутривенный однократный. Препарат один раз вводится в вену обычным шприцем.
- Пероральный. В этом случае средство принимается через рот.
- Ректальный. Для сканирования кишечника контрастное вещество вводится через прямую кишку однократно.
Противопоказаниями при КТ с конрастными веществами, содержащими йодсодержащие препараты являются:
Строгим противопоказанием к любой КТ является беременность, ведь исследование предполагает использование рентгеновского излучения. Относительное противопоказание – грудное вскармливание: после процедуры в течение 1-2 суток следует исключать кормление грудью. У томографа есть ограничение по весу пациента, и при выполнении КТ у людей с массой тела более 110-120 кг могут возникнуть сложности.
Обычно рекомендуется не выполнять процедуру чаще, чем раз в 6 месяцев. Это ограничение связано не с применением контраста, а с получением лучевой нагрузки во время КТ. Тем не менее, эта нагрузка минимальна, и по жизненным показаниям КТ может быть проведена чаще. Следует помнить, что у ряда пациентов (1-3%) наблюдаются патологические реакции на введение контрастного вещества, что также может ограничить частоту выполнения процедуры. К таким реакциям относятся:
Такие реакции считаются признаками аллергии на контрастное вещество и требуют врачебной помощи. Нормальными являются лишь легкий металлический привкус во рту, боль в области инъекции, чувство тепла в теле.
Подготовка к КТ с контрастным усилением включает такие меры:
• Не принимать пищу в течение 4-8 часов перед процедурой (в зависимости от конкретной зоны исследования)
Пациента укладывают на кушетку, вводят ему контрастное вещество, либо устанавливают шприц-инжектор. Через определенный промежуток времени начинают процедуру сканирования – закатывают человека под дугу томографа и выполняют серию снимков. Чем дальше изучаемый орган расположен от сердца, тем дольше нужно контрасту для его окрашивания.
Основные отличия КТ с контрастным усилением и без
При обследовании полых органов обычная нативная КТ без контраста покажет их как однородную серую массу без выделения. Если ввести контрастное вещество, стенки органов окрасятся, что даст возможность рассмотреть любые заболевания их слизистой оболочки и мышечного слоя.
При диагностике раковых опухолей различия между процедурой с контрастом и без такового проявляются наиболее сильно. Именно злокачественные новообразования питаются наибольшим количеством сосудов, поэтому окрашиваются четко, ярко, с видимыми границами. Поэтому зачастую после нативной КТ, на которой обнаружена опухоль, рекомендуют КТ с контрастированием для уточнения диагноза.
В целом, отличия между процедурами таковы:
КТ с контрастным усилением за одно обследование дает намного больше информации для врача.
Компьютерная томография с контрастом делает снимки отдельных анатомических зон более детальными, четкими.
Заболевания, при которых применяется компьютерная томография с контрастом:
Читайте также:

