Успешное развитие трансплантологии обеспечило открытие циклоспорина в каком году
Обновлено: 28.06.2024
Циклоспорин , также называемый циклоспорином и циклоспорином , представляет собой ингибитор кальциневрина , используемый в качестве иммунодепрессанта . Это натуральный продукт . [3] Его принимают внутрь или путем инъекции в вену при ревматоидном артрите , псориазе , болезни Крона , нефротическом синдроме , а также при трансплантации органов для предотвращения отторжения . [3] [4] Он также используется в качестве глазных капель при сухом кератоконъюнктивите. (сухие глаза). [5]
- AU :S4 (только по рецепту)
- Великобритания :POM (только по рецепту)
- США :только ℞
- В общем: ℞ (только по рецепту)
(3 S , 6 S , 9 S , 12 R , 15 S , 18 S , 21 S , 24 S , 30 S , 33 S ) -30-Этил-33 - [(1 R , 2 R , 4 E ) - 1-гидрокси-2-метил-4-гексен-1-ил] -6,9,18,24-тетраизобутил-3,21-диизопропил-1,4,7,10,12,15,19,25,28 -нонаметил-1,4,7,10,13,16,19,22,25,28,31-ундекаазациклотритриаконтан-2,5,8,11,14,17,20,23,26,29,32-ундекон
CC [C @ H] 1C (= O) N (CC (= O) N ([C @ H] (C (= O) N [C @ H] (C (= O) N ([C @ H]) (C (= O) N [C @ H] (C (= O) N [C @@ H] (C (= O) N ([C @ H] (C (= O) N ([C @ H ] (C (= O) N ([C @ H] (C (= O) N ([C @ H] (C (= O) N1) [C @@ H] ([C @ H] (C) C / C = C / C) O) C) C (C) C) C) CC (C) C) C) CC (C) C) C) C) C) CC (C) C) C) C ( В) В) СС (В) В) В) В
Ключ: PMATZTZNYRCHOR-CGLBZJNRSA-N Y
Общие побочные эффекты включают высокое кровяное давление, головную боль, проблемы с почками , усиленный рост волос и рвоту. [4] Другие серьезные побочные эффекты включают повышенный риск инфекции, проблемы с печенью и повышенный риск лимфомы . [4] Следует проверять уровень лекарства в крови, чтобы снизить риск побочных эффектов. [4] Использование во время беременности может привести к преждевременным родам ; однако циклоспорин не вызывает врожденных дефектов . [6]
Считается, что циклоспорин снижает функцию лимфоцитов . [4] Она делает это путем формирования комплекс с циклофилином блокировать фосфатазы активность кальцинейрином , что в свою очередь уменьшает выработку воспалительных цитокинов с помощью Т-лимфоцитов . [7]
В дополнение к этим показаниям циклоспорин также используется при тяжелом атопическом дерматите , болезни Кимуры , гангренозной пиодермии , хронической крапивнице , остром системном мастоцитозе и заднем или промежуточном увеите неинфекционной природы. [ необходима цитата ] Он также используется, хотя и нечасто, при тяжелом ревматоидном артрите и связанных с ним заболеваниях. [ необходима цитата ]
Циклоспорин также применялся у людей с острым тяжелым язвенным колитом и крапивницей, которые не поддаются лечению стероидами . [16]
Побочные эффекты циклоспорина могут включать увеличение десен , усиление роста волос, судороги , пептические язвы , панкреатит , лихорадку , рвоту , диарею , спутанность сознания , повышение уровня холестерина , затрудненное дыхание , онемение и покалывание (особенно губ), зуд , высокое кровяное давление , задержка калия (возможно, приводящая к гиперкалиемии ), дисфункция почек и печени , [17] ощущение жжения на кончиках пальцев и повышенная уязвимость к условно-патогенным грибковым и вирусным инфекциям . Циклоспорин вызывает гипертензию, вызывая сужение сосудов в почках и увеличивая реабсорбцию натрия. Повышение артериального давления может вызвать сердечно-сосудистые заболевания; Таким образом, рекомендуется использовать самую низкую эффективную дозу для людей, нуждающихся в длительном лечении. [18]
Циклоспорин внесен в список канцерогенов IARC группы 1 (т. Е. Имеется достаточно доказательств канцерогенности для людей) [20], конкретно приводящий к плоскоклеточному раку кожи и неходжкинской лимфоме . [21]
Механизм действия
Основное действие циклоспорина - снижение активности Т-клеток ; он делает это путем ингибирования кальциневрина в пути кальциневрин-фосфатаза и предотвращения открытия поры перехода митохондриальной проницаемости. Циклоспорин связывается с цитозольным белком циклофилином (иммунофилином) лимфоцитов , особенно Т-клеток. Этот комплекс циклоспорин-циклофилин ингибирует кальциневрин , который обычно отвечает за активацию транскрипции интерлейкина 2 . В Т-клетках активация рецептора Т-клеток обычно увеличивает внутриклеточный кальций, который действует через кальмодулин, активируя кальциневрин. Затем кальциневрин дефосфорилирует фактор транскрипции NF-AT (ядерный фактор активированных Т-клеток), который перемещается в ядро Т-клетки и увеличивает транскрипцию генов IL-2 и родственных цитокинов. [7] Циклоспорин, предотвращая дефосфорилирование NF-AT, приводит к снижению функции эффекторных Т-клеток ; [22] [23] [24] [25] он не влияет на цитостатическую активность. [ требуется медицинская цитата ]
Циклоспорин также связывается с белком циклофилин D, который составляет часть поры перехода митохондриальной проницаемости (MPTP). [23] [26] MPTP находится в митохондриальной мембране клеток сердечной мышцы и перемещает ионы кальция ( Ca 2+
) в митохондрии. [23] [26] В открытом состоянии Ca 2+
проникает в митохондрии и заставляет мышечные клетки (и, следовательно, сердце) сокращаться. Если не регулировать, приток Са 2+
может способствовать набуханию и дисфункции митохондрий. [26]
Фармакокинетика.
Циклоспорин - циклический пептид из 11 аминокислот ; он содержит одну D- аминокислоту , которая редко встречается в природе. В отличие от большинства пептидов циклоспорин не синтезируется рибосомами. [27]
Циклоспорин сильно метаболизируется у людей и животных после приема внутрь. Метаболиты, которые включают циклоспорин B, C, D, E, H и L [28], обладают менее 10% иммунодепрессивной активности циклоспорина и связаны с более высокой токсичностью для почек. [29] Отдельные метаболиты циклоспорина были выделены и охарактеризованы, но, по-видимому, недостаточно изучены. [ требуется медицинская цитата ]

Биосинтез циклоспорина. Bmt = бутенилметил-треонин, Abu = L-альфа-аминомасляная кислота, Sar = саркозин
Циклоспорин синтезируется нерибосомальной пептид- синтетазой, циклоспорин-синтетазой. [30] Фермент содержит adenylation домен, тиолирование домны, домен конденсации , а также N-метилтрансферазу домен. Adenylation домен ответственен за распознавание субстрата и активации, в то время как домен тиолирование ковалентно связывает adenylated аминокислоты с фосфопантетеин , а область конденсации удлиняется пептидной цепи. Субстраты циклоспорин синтетазы включают L- валин , L- лейцин , L- аланин , глицин , 2-аминомасляную кислоту , 4-метил треонин и D-аланин , который является исходной аминокислотой в процессе биосинтеза. [31] С доменом аденилирования циклоспорин синтетаза генерирует ацил-аденилированные аминокислоты, а затем ковалентно связывает аминокислоту с фосфопантетеином через тиоэфирную связь. Некоторые из аминокислотных субстратов становятся N-метилированными S-аденозилметионином . На стадии циклизации из фермента высвобождается циклоспорин . [32] Аминокислоты, такие как D-Ala и бутенилметил-L-треонин (Bmt), указывают на то, что циклоспорин синтетаза требует действия других ферментов. Рацемизация L-Ala в D-Ala аланинрацемазой является пиридоксальфосфат- зависимой. Образование бутенил-метил-L-треонина осуществляется поликетид-синтазой Bmt, в которой в качестве исходного материала используется ацетат / малонат. [33]
Генный кластер
Tolypocladium inflatum , вид, который в настоящее время используется для массового производства циклоспорина, имеет гены биосинтеза, организованные в кластер из 12 генов. Из этих 12 генов SimA ( Q09164 ) представляет собой циклоспорин-синтетазу, SimB ( CAA02484.1 ) представляет собой аланин-рацемазу и SimG (аналогично ATQ39432.1 ) представляет собой поликетид-синтазу. [34] Эти гены связаны с активным ретротранспозоном. [35] Хотя эти последовательности плохо аннотированы в GenBank и других базах данных, 90% подобных последовательностей можно найти для циклоспорин-продуцирующей Beauveria felina (или Amphichorda ~ ). [36] SimB имеет два паралога в одном организме с разными, но перекрывающимися функциями из-за их низкой специфичности. [37]
В 1970 году новые штаммы грибов были выделены из образцов почвы, взятых в Норвегии и Висконсине в США, сотрудниками Sandoz (ныне Novartis ) в Базеле , Швейцария . Оба штамма производили семейство натуральных продуктов, называемых циклоспоринами. Два родственных компонента, обладающих противогрибковой активностью, были выделены из экстрактов этих грибов. Норвежский штамм Tolypocladium inflatum Gams позже был использован для крупномасштабной ферментации циклоспорина. [38]
Натуральный продукт был назван циклоспорином немецкоязычными учеными, которые первыми выделили его [38], и циклоспорином при переводе на английский язык. За международного непатентованного наименования (МНН) руководящих принципов для лекарственных средств, [48] у заменяли I , так что МНН лекарства пишется циклоспорин. [ необходима цитата ]
Циклоспорин - это МНН и британское одобренное название (BAN), циклоспорин - это принятое в США название (USAN), а циклоспорин - бывший BAN. [ необходима цитата ]
Доступные формы
Циклоспорин проявляет очень плохую растворимость в воде, и, как следствие, были разработаны суспензионные и эмульсионные формы лекарства для перорального применения и для инъекций. Изначально циклоспорин был выведен на рынок компанией Sandoz (теперь Novartis ) под торговой маркой Sandimmune, которая доступна в виде мягких желатиновых капсул, раствора для перорального применения и состава для внутривенного введения. Все это неводные композиции. [49] Более новый микроэмульсии , [50] перорально вводили препарат, Неорал, [51] доступен в виде раствора и в виде мягких желатиновых капсул. Композиции Neoral предназначены для образования микроэмульсий при контакте с водой. [ требуется медицинская цитата ]
Общие препараты циклоспорина продаются под различными торговыми наименованиями, включая Cicloral ( Sandoz / Hexal ), Gengraf ( Abbott ) и Deximune ( Dexcel Pharma ). С 2002 года эмульсия циклоспорина для местного применения для лечения воспаления, вызванного сухим кератоконъюнктивитом (синдромом сухого глаза), продается под торговым названием Restasis (0,05%). Икервис - аналогичный препарат с концентрацией 0,1%. [52] Ингаляционные препараты циклоспорина находятся в стадии клинической разработки и включают раствор в пропиленгликоле и дисперсии липосом . [53] [54]
Нейропротекция
В настоящее время циклоспорин проходит фазу II / III (адаптивного) клинического исследования в Европе для определения его способности уменьшать повреждение нейрональных клеток и реперфузионное повреждение (фаза III) при черепно-мозговой травме. Это многоцентровое исследование организовано NeuroVive Pharma и Европейским консорциумом по травмам мозга с использованием препарата циклоспорина NeuroVive под названием NeuroSTAT (также известного под своим торговым названием CicloMulsion, обеспечивающим защиту сердца ). В этой рецептуре вместо кремофора и этанола используется липидная эмульсионная основа . [55] NeuroSTAT был недавно сравнен с Sandimmune в исследовании фазы I и оказался биоэквивалентным. В этом исследовании NeuroSTAT не проявлял анафилактических реакций и реакций гиперчувствительности, обнаруженных в продуктах на основе кремофора и этанола. [56]
Циклоспорин исследовался как возможное нейропротекторное средство при таких состояниях, как черепно-мозговая травма , и в экспериментах на животных было показано, что он снижает повреждение мозга, связанное с травмой. [57] Циклоспорин блокирует образование поры перехода митохондрий проницаемости , которая, как было обнаружено, вызывает большую часть повреждений, связанных с травмами головы и нейродегенеративными заболеваниями . Нейропротекторные свойства циклоспорина были впервые обнаружены в начале 1990-х годов, когда два исследователя (Эскил Эльмер и Хироюки Учино) проводили эксперименты по трансплантации клеток. Неожиданным открытием было то, что CsA обладал сильным нейропротекторным действием при пересечении гематоэнцефалического барьера. [58] Тот же самый процесс разрушения митохондрий через открытие поры MPT вовлечен в гораздо более тяжелые черепно-мозговые травмы. [59]
Сердечная болезнь
Циклоспорин использовался экспериментально для лечения гипертрофии сердца [23] [60] (увеличение объема клеток).
Неправильное открытие поры перехода митохондриальной проницаемости (MPTP) проявляется в ишемии [23] (ограничение кровотока в ткани) и реперфузионном повреждении [23] (повреждение, возникающее после ишемии, когда кровоток возвращается в ткань), после инфаркта миокарда [24] ( сердечный приступ) и когда происходят мутации в митохондриальной ДНК-полимеразе. [23] Сердце пытается компенсировать болезненное состояние за счет увеличения внутриклеточного Ca 2+
для увеличения скорости цикла сократимости. [26] Постоянно высокий уровень митохондриального кальция 2+
вызывают несоответствующее открытие MPTP, ведущее к снижению сердечного диапазона функций, что приводит к сердечной гипертрофии как попытке компенсировать проблему. [26] [24]
Было показано, что CsA (циклоспорин A) снижает гипертрофию сердца, влияя на сердечные миоциты разными способами. CsA связывается с циклофилином D, чтобы блокировать открытие MPTP и, таким образом, снижает высвобождение белка цитохрома C, который может вызвать запрограммированную гибель клеток. [23] [26] [61] CypD - это белок в MPTP, который действует как ворота; связывание CsA уменьшает количество несоответствующего открытия MPTP, что снижает внутримитохондриальный Ca 2+
. [26] Снижение внутримитохондриального Ca 2+
позволяет обратить вспять сердечную гипертрофию, вызванную исходной сердечной реакцией. [26] Уменьшение высвобождения цитохрома С привело к снижению гибели клеток во время травм и болезней. [23] CsA также ингибирует кальциневриновый путь фосфатазы (14). [23] [24] [62] Было показано, что ингибирование этого пути снижает гипертрофию миокарда. [24] [60] [62]
Лекарство одобрено в США для лечения атопического дерматита у собак. [63] В отличие от человеческой формы лекарства, более низкие дозы, используемые для собак, означают, что препарат действует как иммуномодулятор и имеет меньше побочных эффектов, чем у людей. Преимущества использования этого продукта включают снижение потребности в сопутствующих терапиях для контроля состояния. Он доступен в виде офтальмологической мази для собак под названием Optimmune , производимой Intervet , которая является частью Merck . Он также используется для лечения сального аденита (иммунный ответ против сальных желез ), листовидной пузырчатки (аутоиммунное заболевание кожи с образованием пузырей), воспалительного заболевания кишечника , анального фурункулеза (анального воспалительного заболевания) и миастении (нервно-мышечного заболевания). [63] [64]
Иногда его назначают в крайних случаях иммуноопосредованной гемолитической анемии . [64]
1. Трансплантология и биоэтика. Биоэтические проблемы трансплантологии
2. Трансплантация
ТРАНСПЛАНТАЦИЯ
Трансплантация (от лат. transplantare –
пересаживать) – процесс замены
поврежденных или утраченных органов
путем пересадки таких же органов,
взятых из здоровых организмов того же
вида.
Различают три вида трансплантации:
аутотрансплантацию –
трансплантацию в пределах одного
организма,
алло- или гомотрансплантацию –
трансплантацию в пределах одного вида
гетеро- или ксенотрансплантация –
трансплантацию между различными
видами.
Актуальность изучения этических проблем пересадки органов
в клинической практике обусловлена тем, что в каждом случае
она связана с решением сразу двух людей — донора —
человека, который может отдать свои органы или ткани для
пересадки — и реципиента — лица, нуждающегося в такой
пересадке.
Профессиональная врачебная этика в отношении
трансплантации органов однозначна: помочь больномуреципиенту необходимо обязательно, но не за счет здоровья
донора. Законом запрещается пересадка органа, если заведомо
известно, что эта операция нанесет необратимый вред донору.
Второе правило объясняет механизм принятия решения
врачом: трансплантация органов допустима, если результат
операции оправдывает нежелательные побочные эффекты.
Типы забора органов для
трансплантации от трупа
Презумпция
согласия
Презумпция
несогласия
рутинный забор
Рутинный забор
основанием является сложившаяся практика, согласно
которой власти могут по своему усмотрению
распоряжаться телом умершего человека. В частности,
они дают службам здравоохранения полномочия
производить вскрытие, забирать органы для научных и
прочих манипуляций, использовать физиологические
жидкости и ткани трупа для самых разных целей.
Тело умершего человека в данном случае трактуется как
государственная собственность, которую медики
могут использовать в общественных интересах.
8. Механизм презумпции согласия (или предполагаемого согласия)
МЕХАНИЗМ ПРЕЗУМПЦИИ СОГЛАСИЯ
(ИЛИ ПРЕДПОЛАГАЕМОГО СОГЛАСИЯ)
Этот принцип отличается от рутинного забора тем,
что хотя специальное разрешение на забор органов
после смерти и не испрашивается, но согласие на
такой забор предполагается, то есть констатируется
отсутствие отказа от подобной манипуляции.
Действующий
закон
по
трансплантологии
предоставляет право на отказ как самому человеку –
заранее, так и его родственникам – после его смерти.
12. Основные этические принципы, регулирующие трансплантацию органов или тканей человека
ОСНОВНЫЕ
ЭТИЧЕСКИЕ ПРИНЦИПЫ, РЕГУЛИРУЮЩИЕ
ТРАНСПЛАНТАЦИЮ ОРГАНОВ ИЛИ ТКАНЕЙ ЧЕЛОВЕКА
1. Органы человека не могут рассматриваться как
объект купли и продажи.
2. Пересадка от живого донора может основываться
только на добровольном самопожертвовании ради
спасения жизни другого человека. В этом случае согласие
на изъятие органа становится проявлением любви и
сострадания.
3. Потенциальный донор должен быть полностью
информирован о возможных последствиях эксплантации
органа для его здоровья.
4. Морально не допустима эксплантация, прямо
угрожающая жизни донора. Согласно российскому
законодательству изъятие органа у живого донора
допускается только в том случае, если донор состоит с
реципиентом в генетической связи, за исключением
случаев пересадки костного мозга.
5. Неприемлемо сокращение жизни одного человека, в
том числе через отказ от жизнеподдерживающих
процедур с целью продления жизни другого.
15. К оспроблемам трансплантологии новным этическим и правовым следует отнести проблемы:
К ОСПРОБЛЕМАМ ТРАНСПЛАНТОЛОГИИ НОВНЫМ
ЭТИЧЕСКИМ И ПРАВОВЫМ СЛЕДУЕТ ОТНЕСТИ ПРОБЛЕМЫ:
• определения момента смерти человека;
• изъятия донорского материала (у живого донора
или трупа);
• торговли человеческими органами и тканями;
• распределения дефицитных ресурсов (донорских
органов и тканей);
• распределением органов и/ или тканей между
реципиентами
• коммерциализацией трансплантологии
• ксенотрансплантации и др.
16. Определение смерти человека
18. Опасность коммерциализации донорства
Ксенотрансплантациями
называются пересадки органов и
тканей от животных человеку.
Попытки переливать кровь от животных
человеку и пересаживать органы имеют давнюю
историю. Однако только с появлением
циклоспорина, подавляющего реакции
отторжения трансплантатов, и с прогрессом в
области генетической инженерии, который
сулит преобразовать геном животных-доноров
для обеспечения гистосовместимости, возникли
реальные коммерческие проекты в области
ксенотрансплантологии.
Ксенотрансплантация сталкивается с
контраргументами не только
медицинского, экономического и
юридического, но и чисто морального
свойства.
Сторонниками экологической этики
нередко выдвигаются требования если не
запрета, то резкого ограничения
экспериментов в этой области.
20. Проблема отторжения
С этической точки зрения
донорство должно быть
добровольной, осознанно
совершаемой и
бескорыстной
(альтруистической)
жертвой

Проблемы трансплантологии в современной медицине
Трансплантация органов и тканей человека является одной из вершин современной медицины и отражает состояние медицинской науки и практики государства. Пересадка почек, сердца, других органов и тканей человека давно перестали быть сенсацией и широко внедрены в развитых странах.
Проблемы трансплантологии интенсивно изучались в ряде ведущих научно- исследовательских институтов. До начала 60-х годов трансплантология оставалась в нашей стране действительно областью экспериментальной хирургии, но без этих экспериментов многие достижения мировой хирургии в области трансплантологии могли быть отодвинуты на многие годы назад или не осуществиться вообще. Интерес мировой общественности к проблемам трансплантологии вспыхнул с необычайной силой после первой пересадки сердца.
За последние два – три десятилетия трансплантология сделала стремительный рывок вперед. Увеличился и уменьшился набор иммунодепрессантов, позволяющих блокировать, обращать вспять или предотвращать процессы отторжения чужого органа (трансплантата) организмом больного. Совершенствовались методы хранения трансплантатов, это открыло путь для расширения географии пересадок и создание национальных и межнациональных систем обеспечения органами. Отшлифовалась хирургическая техника пересадок. Первая трансплантация сердца воспринялась как некое чудо, таинство, теперь – это рядовая операция. Детально отработана пересадка почек, печени, есть проекты пересадки головного мозга.
Успехи трансплантологии показали, что перед человечеством открылась новая, чрезвычайно перспективная возможность лечения больных, ранее считавшихся обреченными. Одновременно возник целый спектр правовых и этических проблем, требующих для своего разрешения совместных усилий специалистов в области медицины, права, этики, психологии и других дисциплин. Эти проблемы не могут считаться решенными, если выработанные специалистами подходы и рекомендации не получат общественного признания и не будут пользоваться общественным доверием.
Пересадка органов не стала в нашей стране массовым видом медицинской помощи вовсе не потому, что потребность в ней невелика. Причины иные. Важнейшая и, увы, самая прозаичная - выливается в сумму, которую нашему человеку среднего достатка за всю жизнь не накопить. Обеспечить это дорогостоящее лечение обязано государство. Но его возможности нам известны.
Проблема номер два современной трансплантологии – недостача донорских органов, применительно к российской действительности. Вроде бы на первый взгляд простейшее ее решение - использовать органы случайно погибших здоровых людей. И хотя ежедневно, как ни прискорбно, только в нашей стране от травм умирают сотни людей, обеспечение органного донорства дело непростое. Опять же по многим причинам: нравственным, религиозным, чисто организационным.
В разных странах мира действуют разные подходы к заготовке донорских органов. В Китае законом разрешено брать их у трупов казненных. Для России это неприемлемо. У нас действует мораторий на смертную казнь. Намного симпатичней и перспективней китайского опыта представляются принятые во многих государствах акты дарения органов. Люди в молодые годы и в полном здравии завещают на случай, если, неожиданно погибнут, свои органы тем, кому они могут спасти жизнь. Папа Иоан Павел II такого рода дарения назвал микровоспроизведением подвига Христа. Если бы в России такие акты привились, забор органов для прямого донорства намного упростился бы, и мы смогли бы помочь несравненно большему числу тяжелобольных.
Несколько лет назад в Москве на базе одной из городских больниц был создан единственный на весь мегаполис центр по заготовке органов. И если забор почек от трупов производился, то с изъятием сердец было совсем плохо. НИИ кардиологии (нынче в России он монополист по их пересадке) получал до десяти сердец в год, в то время как их ждут, только по данным медицинских изданий, около тысячи находящихся на грани жизни и смерти кардиологических больных. Забором печени и легких, требующим высочайшей квалификации трансплантологов и связанного с жестким ограничением во времени, московский центр практически вовсе не занимается, даже при том, что на всю Россию в год производится не более 600 пересадок почки, сердца, печени, легких.
И когда орган находится, еще нужно, чтобы полностью совпали иммуно-генетические параметры донора и реципиента. Но это еще тоже не гарантия приживления пересаженного сердца или почки, а следовательно еще одна проблема - преодоление риска отторжения органов. Унифицированных средств, предупреждающих процесс отторжения, пока не существует. В мире постоянно работают над новыми иммуносупрессорами. И каждый лучше предыдущего, и каждый очередной поначалу принимается на ура. Но по мере того, как начинают с ним работать, восторг спадает. Все существующие препараты этого ряда пока по-разному несовершенны, все обладают побочными эффектами, все снижают общий иммунологический ответ, в свою очередь вызывая тяжелые посттрансплантационные инфекционные поражения, а отдельные еще бьют по почкам, печени, повышают артериальное давление. Приходится отказываться от моноиммуносупрессорной терапии. Приходится комбинировать разные препараты, лавировать дозами каждого, идти на компромиссы.
Этические проблемы трансплантологии
Этические проблемы трансплантологии существенно различаются в зависимости от того, идет ли речь о заборе органов для пересадки у живого человека или из тела умершего.
Пересадка от живых доноров. Пересадка почек – первое направление трансплантологии, которое нашло место в практической медицине. В настоящее время – это бурно развивающееся во всем мире направление оказания медицинской помощи больным с необратимо нарушенной деятельностью почек. Пересадки почек не только спасли от смерти сотни тысяч пациентов, но и обеспечили им высокое качество жизни.
Помимо почки, от живого донора пересаживают долю печени, костный мозг и т.д., что во многих случаях так же является спасающим жизнь пациента методом лечения. Однако при этом возникает целый ряд непростых моральных проблем:
→ пересадка органов от живого донора сопряжена с серьезным риском для последнего;
→ пересадка должна проходить с информированного, осознанного, добровольного согласия;
→ пересадка должна обеспечиваться соблюдением принципа конфиденциальности.
Донорство органов умершего человека. Использование трупа человека в качестве источника органов для пересадки вызывает целый спектр непростых моральных проблем. Все мировые религии требуют бережного и почтительного отношения к телу умершего человека.
Считается, что права индивида, который лишился права контролировать судьбу уже бесполезных для него останков, перевешивается очевидным благом для общества в лице потенциальных реципиентов, жизнь которых может быть спасена в результате пересадки.
Подобная практика и подобное отношение, с позиций соблюдения прав человека, считается морально ущербным.
Все более широкий размах принимает использование для целей трансплантологии органов и тканей не только человека, но и животных – ксенотрансплантация. Наиболее близкими генетически к человеку являются приматы. Эволюционная близость усиливает риск передачи и последующего распространения среди людей вирусных инфекций, существующих у приматов.
Создаются универсальные доноры органов для человека и на базе некоторых пород свиней, физиологическое и анатомическое строение внутренних органов которых достаточно близко к человеческому. Но, пересаживая человеку органы, к примеру, свиньи, мы рискуем так же одновременно перенести ему такие заболевания, как бруцеллез, грипп свиней и целый ряд других инфекций – как наблюдающихся, так и не наблюдающихся в обычных условиях у человека. Последнее особо опасно, так как в человеческом организме нет эволюционно отработанных защитных механизмов для борьбы с ними.
ПЕРЕСАДКА ОРГАНОВ (трансплантация) - изъятие жизнеспособного органа у одной особи (донора) с перенесением его другой (реципиенту). Если донор и реципиент принадлежат к одному и тому же виду, говорят об аллотрансплантации; если к разным - о ксенотрансплантации. В тех случаях, когда донор и пациент - однояйцовые (идентичные) близнецы или представители одной и той же инбредной (т.е. полученной в результате кровнородственного скрещивания) линии животных, речь идет об изотрансплантации.
Ксено- и аллотрансплантаты, в отличие от изотрансплантатов, подвергаются отторжению. Механизм отторжения - несомненно иммунологический, сходный с реакцией организма на введение чужеродных веществ. Изотрансплантаты, взятые у генетически родственных особей, обычно не отторгаются.
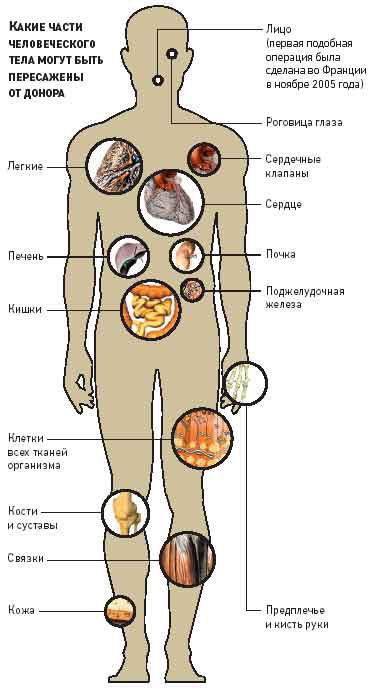
В экспериментах на животных производилась пересадка практически всех жизненно важных органов, однако далеко не всегда с успехом. Жизненно важные органы - те, без которых сохранение жизни практически невозможно. Примером таких органов могут служить сердце и почки. Однако ряд органов, скажем поджелудочную железу и надпочечники, обычно не считают жизненно необходимыми, так как утрату их функции можно компенсировать заместительной терапией, в частности введением инсулина или стероидных гормонов. Человеку пересаживали почки, печень, сердце, легкие, поджелудочную, щитовидную и околощитовидную железы, роговицу и селезенку. Некоторые органы и ткани, такие, как сосуды, кожа, хрящ или кость, пересаживают с целью создания каркаса, на котором могут формироваться новые ткани реципиента.
Трансплантация органов и тканей
Классификация:
Аутотрасплантация – пересадка реципиенту собственной ткани из одного участка тела в другой, например пересадка кожного лоскута.
Изотрансплатнация – пересадка ткани от генетически идентичного лица (монозиготный близнец)
Аллотрансплантация – пересадка тканей от генетически отличного донора одного биологического вида (трансплантация трупной почки).
Ксенотрансплантация – пересадка ткани от донора другого биологического вида. В настоящее время используется только 1 ксенотрансплантант – временный свиной кожный лоскут при ожогах.
Перед операцией донору подробно объясняется ход операции, возможные исходы и в присутствии ближайшего родственника. Пройти полное медицинское и психологическое обследование.
Вначале берут кровь для определения группы и типирования тканей. HLA типирование - исследование главного комплекса гистосовместимости человека - HLA комплекса. Это образование включает в себя область генов на 6-й хромосоме, которые кодируют HLA-антигены, участвующие в различных реакциях иммунного ответа. Если они совместимы выполняется ряд анализов крови: гемоглобин, ОАК, СОЭ, МЭ, креатинин, ФПП, глюкоза. Исследования на гепатиты C и B, ВИЧ. Проводят ОРГК и ЭКГ. Выполняется перекрёстная проба между лимфоцитами донора и сывороткой реципиента. Эта проба показывает иммунный ответ лимфоцитов хозяина на клеточные антигены донора in vitro. Положительная реакция является противопоказанием к трансплантации. Далее проводят артериографию. Она требуется для подтверждения структурно-функциональной целостности органов.
Живые неродственные доноры.
Современный опыт свидетельствует, что трансплантация от некровных доноров может быть успешной. Организационные моменты при некровных донорах такие же как и при кровных. Но врач должен убедиться, что на донора не оказывают никакого давления. Это очень важно, что бы быть уверенным в свободе донора в своём выборе. И донора, и реципиента приглашают встретиться с независимым экспертом. Эксперт должен удостовериться, что донор понимает, что вовлечено в донорство. Выяснить причины желания быть донором и удостовериться, что донор не испытывает какую-либо форму давления.
Трупные доноры.
Получение разрешение на донорство трупными органами.
1. Лечащий врач-консультант должен определить потенциального донора.
2. С трансплантационной бригадой можно связаться до установления смерти ствола головного мозга, чтобы определить подходит ли донор.
Общие критерии для трупных органов:
• Причины смерти:
- травма головного мозга
- кровоизлияние в головной мозг
- суицид
- первичная опухоль головного мозга (гистологически подтверждённая)
- остановка сердца со смертью мозга
• Исключения:
- злокачественная опухоль
- ВИЧ-инфекция
- гепатит В и С
- болезнь Крейтцфельда-Якоба.
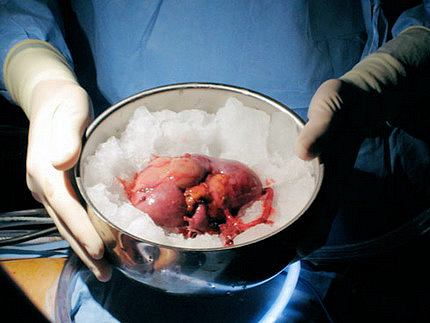
3. Проводят первое определение стволовой смерти. Поднимается вопрос с родственниками о донортсве.
4. Берётся анализ крови на группу крови, ВИЧ, гепатиты.
Подбор тканей
АВ0-совместимость.
Группа 0 – универсальный донор.
Совместимость по лейкоцитарным антигенам человека (HLA). Показатель локализуется на коротком плече 6- хромосомы.
Цитотоксические перекрёстные пробы. Должны быть отрицательными. Кровт реципиента исследуется на цитотоксические антитела против антигенов на Т-лимфоцитах донора. Если антитела имеются, то в случае трансплантации они будут связываться с пересаженным органом и разрушать его.
Отторжение
– возникает при несовместимости по системе АВ0 и при наличии оразовавшихся ранее цитотоксических антител. Оно происходит на операционном столе. В случае трансплантации почки она выглядит сморщенной, цианотичной, в итоге тромбируется. Показана нефроэктомия.
Ускоренное острое отторжение – быстрое начало в пределах 1-й недели. Эффективность низкая.
Острое отторжение – в пределах 3-х месс. Характерна инфильтрация органа Т-лимфоцитами. Лечение метилпреднизолоном, антилимфоцитарным глобулином и т.д.
Хроническое отторжение – проявляется медленным снижением фун-ии. Происходит утолщение интимы сосудов. Это состояние неизлечимо.

Отторжение кожи после операции перетонита, пересадка искусственной кожи.

Трансплантация и донорство органов не могли появиться в науке и клинической практике одномоментно. В отличие от хирургии, которая совершенствовалась поэтапно, чтобы успешно пересадить человеку органы и ткани, требовался большой багаж научных знаний: как работает организм человека, какие механизмы управляют клетками в его тканях. И конечно, усовершенствованное мастерство сшивания сосудов, знания об иммунологии и многое-многое другое.
Только в конце XIX века врачи-исследователи вплотную приблизились к идее того, что сращиваться могут не только поврежденные ткани на теле человека - так закрывается хирургический разрез или ранка на сбитой коленке, - но возможно отделить ткань или даже орган полностью и перенести его в другой организм. Сама по себе идея о том, что человеку можно заменить поврежденный орган или часть тела, существовала с древних времен. В мировую науку и практику неоценимый вклад внесли отечественные исследовали.
О том, с чего начиналась трансплантология в России: от смелых идей величайшего хирурга Николая Пирогова до наших дней, - читайте в нашем материале.
1. Работы Николая Ивановича Пирогова
Именно работы Николая Ивановича Пирогова заложили основу пересадки тканей и кости. Во второй половине XIX века трансплантология была неотделима от пластической хирургии - речь шла преимущественно о восстановлении носа, необходимости закрыть крупные повреждения на теле (от болезни или ранений), трансплантации кости, чтобы сохранить человеку здоровье, а зачастую и жизнь.
В одной из своих лекций Пирогов обратил внимание на то, что самые лучшие лекарства, которые имелись на тот момент в арсенале врача, существенно уступали тем удивительным процессам восстановления, на которые способен организм человека: "Наши лучшие средства, пластыри, швы, - писал он, - все принадлежности хирургической перевязки представляются мелочными, исчезают в ничтожестве пред этим чудным явлением, на познании которого хирург основывает самые смелые свои надежды при делании пластических операций".
2. Труды по трансплантации кости
Следующим важным этапом в работе отечественных врачей стали труды по трансплантации кости. Эти работы проводили ученики Пирогова. Одним из таких исследователей был Михаил Руднев, который уже вместе со своими учениками подтвердил, что костный мозг является важным органом для образования кости, а в некоторых случаях только костный мозг обеспечивает приживление трансплантата. С момента открытия российских исследователей принято считать подтвержденным учение о том, что костный мозг участвует в процессе образования кости. Тогда же проводились первые опыты по восстановлению костей черепа.
Наиболее известен случай, описанный в журнале "Врач" (1883, № 13, с. 207): в начале того же года врач пересадил 71-летнему мужчине три части кости собаки для восстановления функции сустава надколенника. Это был первый описанный случай трансплантации от животного к человеку.
3. Попытки пересадить ткани животного человеку
В работе врача-исследователя отрицательный результат - тоже важный результат, так как он дает понять, в какую сторону двигаться не стоит. Так, уже в последние годы XIX века стало понятно, что попытки пересадить человеку кожу, взятую у животного, не принесут пользы. Сам Пирогов, который уже в то время не практиковал, но внимательно следил за всем, что происходит в этой области, назвал такие опыты "биологической погрешностью".
А вот довольно смелая для 1980 года идея о пересадке кожи от умершего человека, напротив, была встречена с интересом. Оказалось, что ткани эпителия остаются жизнеспособными довольно долго после смерти человека, поэтому их можно использовать для трансплантации. Позднее хирурги на практике убедились в невозможности истинного приживления кожи, взятой от трупа. Пересаженный лоскут бесследно исчезал под воздействием лейкоцитов примерно через 1–2 месяца. Но иногда даже этого выигранного времени хватало, чтобы битва за жизнь и здоровье пациента завершилась успешно.
4. Нобелевская премия за теорию иммунитета
Поистине эпохальное для всей мировой науки и для трансплантологии в частности открытие произошло в конце XIX века, и связано оно с трудами великого русского биолога Ильи Мечникова, получившего впоследствии Нобелевскую премию за теорию иммунитета. Возникновение инфекционной и неинфекционной иммунологии, в том числе трансплантационной, дало объяснение процессам, происходящим в пересаженных тканях. А также позволило врачам, занимающимся трансплантационной деятельностью, понять, почему вроде бы прижившиеся кожные лоскуты "таяли" на глазах, а другие и вовсе отторгались организмом реципиента.
5. Создание отделения экспериментальной хирургии
6. Первая в мире монография по трансплантологии
Развитие мировой и отечественной трансплантологии принято связывать в первую очередь с именем Владимира Петровича Демихова. Начиная с 1946 года он регулярно проводил уникальные операции по пересадке внутренних органов собакам. К значимым событиям в работе Демихова можно отнести операции по пересадке мозга и первую имплантацию искусственного сердца. Он подготовил в 1960 году книгу "Пересадка жизненно важных органов в эксперименте", ставшую первой в мире монографией по трансплантологии. Два года спустя книгу "мирового отца трансплантологии" переиздадут в Нью-Йорке, Берлине, Мадриде.
Первую в мире пересадку сердца сделал Кристиан Барнард в больнице Грооте-Схур в Кейптауне в 1967 году. При этом врач неоднократно отмечал, что именно русского ученого и врача Владимира Демихова считает своим учителем.
7. Первая успешная пересадка почки в России
1965 год стал поворотным для отечественной трансплантологии - состоялась первая успешная пересадка почки в нашей стране. Выполнена она хирургом Борисом Васильевичем Петровским. С тех пор эта операция уже давно стала рутинной, вошла в арсенал хирургов и является самой распространенной в России и мире трансплантацией.
8. Первая успешная пересадка сердца от умершего человека в нашей стране
Накопленные знания и опыт привели к стремительному развитию трансплантологии и многим успешным практикам. Так, уже в 1987 году в России была выполнена первая успешная пересадка сердца от умершего человека молодой женщине. Всего за несколько месяцев до операции смерть человека стали констатировать по "смерти мозга". Профессор Шумаков, его соратники и ученики добивались этого несколько десятилетий. И как только это признали законным, стало возможно развивать трансплантационную деятельность и внедрять ее в клиническую практику.
25-летняя Александра Шалькова болела кардиомиопатией, после операции по пересадке сердца она прожила еще 8,5 лет, успев выйти замуж. Как отмечал в одном из интервью Шумаков, молодая женщина умерла из-за собственной неосторожности, так как не приняла вовремя препараты, которые подавляют иммунитет, из-за чего началось отторжение пересаженного органа. Тогда же в НИИ трансплантологии и искусственных органов МЗ СССР было создано отделение коронарной хирургии и трансплантации сердца. Сейчас весь центр носит имя Валерия Шумакова. В июне 2018 года в центре провели тысячную трансплантацию сердца.
9. Пересадка правой доли печени от живого родственного донора
Важным достижением в мировой и отечественной трансплантологии стала пересадка правой доли печени от живого родственного донора в ноябре 1997 года. Операцию провел Сергей Готье. Сейчас Алексей Мишин уже взрослый человек, работает программистом, любит путешествовать.
10. Трансплантация трех органов ребенку
Уникальная для всего мирового сообщества успешная операция по трансплантации сразу трех органов девятилетнему ребенку. У мальчика Миши из села Таранай под Южно-Сахалинском еще в младенчестве обнаружили муковисцидоз. Он поразил печень и легкие мальчика так, что стало понятно: мальчику нужны новые легкие и новая печень. Операция длилась 16 часов и прошла успешно. Прошло 1,5 года после трансплантации, Миша чувствует себя хорошо.

Развитие трансплантологии и донорства органов уже гораздо меньше зависит от новых знаний в этой области. Конечно, когда-нибудь ученые смогут выращивать и искусственные органы, но пока сложно сказать, что это произойдет в сколь-нибудь обозримом будущем. Сейчас основной проблемой является "искусственный" дефицит донорских органов. Государственная политика у нас в стране создает необходимые механизмы для того, чтобы трансплантационная деятельность развивалась. Именно в этих условиях на первый план выходят информированность общества в вопросах донорства, а также готовность врачей в больницах и организаторов здравоохранения в регионах налаживать трансплантационную деятельность. Готовность людей к посмертному донорству и принятие в обществе идеи того, что это один из способов проявления бескорыстной помощи, уже сейчас позволяют спасать жизни тех, кому все известные способы лечения уже помочь не могут. И речь здесь идет о спасении нескольких тысяч жизней ежегодно.
Трансплантация и донорство органов не могли появиться в науке и клинической практике одномоментно. В отличие от хирургии, которая совершенствовалась поэтапно, чтобы успешно пересадить человеку органы и ткани, требовался большой багаж научных знаний: как работает организм человека, какие механизмы управляют клетками в его тканях. И конечно, усовершенствованное мастерство сшивания сосудов, знания об иммунологии и многое-многое другое.
Только в конце XIX века врачи-исследователи вплотную приблизились к идее того, что сращиваться могут не только поврежденные ткани на теле человека - так закрывается хирургический разрез или ранка на сбитой коленке, - но возможно отделить ткань или даже орган полностью и перенести его в другой организм. Сама по себе идея о том, что человеку можно заменить поврежденный орган или часть тела, существовала с древних времен. В мировую науку и практику неоценимый вклад внесли отечественные исследовали.
О том, с чего начиналась трансплантология в России: от смелых идей величайшего хирурга Николая Пирогова до наших дней, - читайте в нашем материале.
1. Работы Николая Ивановича Пирогова
Именно работы Николая Ивановича Пирогова заложили основу пересадки тканей и кости. Во второй половине XIX века трансплантология была неотделима от пластической хирургии - речь шла преимущественно о восстановлении носа, необходимости закрыть крупные повреждения на теле (от болезни или ранений), трансплантации кости, чтобы сохранить человеку здоровье, а зачастую и жизнь.
В одной из своих лекций Пирогов обратил внимание на то, что самые лучшие лекарства, которые имелись на тот момент в арсенале врача, существенно уступали тем удивительным процессам восстановления, на которые способен организм человека: "Наши лучшие средства, пластыри, швы, - писал он, - все принадлежности хирургической перевязки представляются мелочными, исчезают в ничтожестве пред этим чудным явлением, на познании которого хирург основывает самые смелые свои надежды при делании пластических операций".
2. Труды по трансплантации кости
Следующим важным этапом в работе отечественных врачей стали труды по трансплантации кости. Эти работы проводили ученики Пирогова. Одним из таких исследователей был Михаил Руднев, который уже вместе со своими учениками подтвердил, что костный мозг является важным органом для образования кости, а в некоторых случаях только костный мозг обеспечивает приживление трансплантата. С момента открытия российских исследователей принято считать подтвержденным учение о том, что костный мозг участвует в процессе образования кости. Тогда же проводились первые опыты по восстановлению костей черепа.
Наиболее известен случай, описанный в журнале "Врач" (1883, № 13, с. 207): в начале того же года врач пересадил 71-летнему мужчине три части кости собаки для восстановления функции сустава надколенника. Это был первый описанный случай трансплантации от животного к человеку.
3. Попытки пересадить ткани животного человеку
В работе врача-исследователя отрицательный результат - тоже важный результат, так как он дает понять, в какую сторону двигаться не стоит. Так, уже в последние годы XIX века стало понятно, что попытки пересадить человеку кожу, взятую у животного, не принесут пользы. Сам Пирогов, который уже в то время не практиковал, но внимательно следил за всем, что происходит в этой области, назвал такие опыты "биологической погрешностью".
А вот довольно смелая для 1980 года идея о пересадке кожи от умершего человека, напротив, была встречена с интересом. Оказалось, что ткани эпителия остаются жизнеспособными довольно долго после смерти человека, поэтому их можно использовать для трансплантации. Позднее хирурги на практике убедились в невозможности истинного приживления кожи, взятой от трупа. Пересаженный лоскут бесследно исчезал под воздействием лейкоцитов примерно через 1–2 месяца. Но иногда даже этого выигранного времени хватало, чтобы битва за жизнь и здоровье пациента завершилась успешно.
4. Нобелевская премия за теорию иммунитета
Поистине эпохальное для всей мировой науки и для трансплантологии в частности открытие произошло в конце XIX века, и связано оно с трудами великого русского биолога Ильи Мечникова, получившего впоследствии Нобелевскую премию за теорию иммунитета. Возникновение инфекционной и неинфекционной иммунологии, в том числе трансплантационной, дало объяснение процессам, происходящим в пересаженных тканях. А также позволило врачам, занимающимся трансплантационной деятельностью, понять, почему вроде бы прижившиеся кожные лоскуты "таяли" на глазах, а другие и вовсе отторгались организмом реципиента.
5. Создание отделения экспериментальной хирургии
6. Первая в мире монография по трансплантологии
Развитие мировой и отечественной трансплантологии принято связывать в первую очередь с именем Владимира Петровича Демихова. Начиная с 1946 года он регулярно проводил уникальные операции по пересадке внутренних органов собакам. К значимым событиям в работе Демихова можно отнести операции по пересадке мозга и первую имплантацию искусственного сердца. Он подготовил в 1960 году книгу "Пересадка жизненно важных органов в эксперименте", ставшую первой в мире монографией по трансплантологии. Два года спустя книгу "мирового отца трансплантологии" переиздадут в Нью-Йорке, Берлине, Мадриде.
Первую в мире пересадку сердца сделал Кристиан Барнард в больнице Грооте-Схур в Кейптауне в 1967 году. При этом врач неоднократно отмечал, что именно русского ученого и врача Владимира Демихова считает своим учителем.
7. Первая успешная пересадка почки в России
1965 год стал поворотным для отечественной трансплантологии - состоялась первая успешная пересадка почки в нашей стране. Выполнена она хирургом Борисом Васильевичем Петровским. С тех пор эта операция уже давно стала рутинной, вошла в арсенал хирургов и является самой распространенной в России и мире трансплантацией.
8. Первая успешная пересадка сердца от умершего человека в нашей стране
Накопленные знания и опыт привели к стремительному развитию трансплантологии и многим успешным практикам. Так, уже в 1987 году в России была выполнена первая успешная пересадка сердца от умершего человека молодой женщине. Всего за несколько месяцев до операции смерть человека стали констатировать по "смерти мозга". Профессор Шумаков, его соратники и ученики добивались этого несколько десятилетий. И как только это признали законным, стало возможно развивать трансплантационную деятельность и внедрять ее в клиническую практику.
25-летняя Александра Шалькова болела кардиомиопатией, после операции по пересадке сердца она прожила еще 8,5 лет, успев выйти замуж. Как отмечал в одном из интервью Шумаков, молодая женщина умерла из-за собственной неосторожности, так как не приняла вовремя препараты, которые подавляют иммунитет, из-за чего началось отторжение пересаженного органа. Тогда же в НИИ трансплантологии и искусственных органов МЗ СССР было создано отделение коронарной хирургии и трансплантации сердца. Сейчас весь центр носит имя Валерия Шумакова. В июне 2018 года в центре провели тысячную трансплантацию сердца.
9. Пересадка правой доли печени от живого родственного донора
Важным достижением в мировой и отечественной трансплантологии стала пересадка правой доли печени от живого родственного донора в ноябре 1997 года. Операцию провел Сергей Готье. Сейчас Алексей Мишин уже взрослый человек, работает программистом, любит путешествовать.
10. Трансплантация трех органов ребенку
Уникальная для всего мирового сообщества успешная операция по трансплантации сразу трех органов девятилетнему ребенку. У мальчика Миши из села Таранай под Южно-Сахалинском еще в младенчестве обнаружили муковисцидоз. Он поразил печень и легкие мальчика так, что стало понятно: мальчику нужны новые легкие и новая печень. Операция длилась 16 часов и прошла успешно. Прошло 1,5 года после трансплантации, Миша чувствует себя хорошо.
Развитие трансплантологии и донорства органов уже гораздо меньше зависит от новых знаний в этой области. Конечно, когда-нибудь ученые смогут выращивать и искусственные органы, но пока сложно сказать, что это произойдет в сколь-нибудь обозримом будущем. Сейчас основной проблемой является "искусственный" дефицит донорских органов. Государственная политика у нас в стране создает необходимые механизмы для того, чтобы трансплантационная деятельность развивалась. Именно в этих условиях на первый план выходят информированность общества в вопросах донорства, а также готовность врачей в больницах и организаторов здравоохранения в регионах налаживать трансплантационную деятельность. Готовность людей к посмертному донорству и принятие в обществе идеи того, что это один из способов проявления бескорыстной помощи, уже сейчас позволяют спасать жизни тех, кому все известные способы лечения уже помочь не могут. И речь здесь идет о спасении нескольких тысяч жизней ежегодно.
Читайте также:
- Почему все боятся прокурора
- Возможно ли процессуальное правопреемство при защите чести и достоинства
- Кто является наследником алексея михайловича
- Процентная ставка выше чем по жилищному кредиту залог не обязателен достаточно только поручителя
- Как правильно написать предвыборную речь кандидата на должность главы сельсовета

