Права и левая часть сердца разделено из прочной перегородка как они называются
Обновлено: 30.06.2024
Дефект межжелудочковой перегородки (ДМЖП) — одна из распространенных врожденных аномалий сердца новорожденных. ДМЖП отличается формированием дефекта в перегородке, разделяющей левый и правый желудочки сердца.
Небольшие дефекты межжелудочковой перегородки могут не представлять опасности и даже иногда самостоятельно закрываются. В то же время крупные отверстия в перегородке непосредственно угрожают жизни ребенка.
О том, что такое ДМЖП и чем он проявляется, напишем далее.
Причины возникновения ДМЖП у плода
Любые пороки сердца, и ДМЖП в том числе, чаще всего возникают в первом—втором триместре беременности под влиянием неблагоприятных факторов. Именно в этот период начинают закладываться ткани сердечной мышцы и кровеносной системы. Любое нарушение нормального процесса формирования и деления клеток может приводить к тяжелым последствиям.
Возникает ДМЖП у плода по причине таких обстоятельств как:
- острое инфекционное заболевание беременной в первом триместре,
- хронические инфекционные болезни матери,
- влияние на организм беременной токсинов, алкоголя, никотина,
- пожилой возраст одного из родителей,
- наследственная отягощенность и пр.
Очень часто при ДМЖП причины возникновения патологии вообще не обнаруживаются.
Поэтому в зоне риска может быть абсолютно любой ребенок.
Для выявления ДМЖП и причин его возникновения предусмотрен ряд диагностических мероприятий. Чаще всего необходимую информацию о здоровье сердца плода удается получить по данным ультразвукового исследования.
Особенности кровообращения при врожденном пороке сердца ДМЖП
Особенностью врожденного порока сердца ДМЖП является наличие отверстия в перегородке, которая разделяет левый и правый желудочки сердца. Левый желудочек в норме нагнетает обогащенную кислородом кровь в аорту и ко всем органам тела по большому кругу кровообращения. Правый желудочек направляет кровь в легкие для очистки от углекислого газа и насыщения ее кислородом.
Через имеющийся при ВПС дефекте межжелудочковой перегородки происходит ненормальное поступление крови из левого желудочка в правый, что вызывает резкую его перегрузку.
Повышение давления в легочных сосудах приводит к их уплотнению и обратному забрасыванию бедной кислородом крови из правого в левый желудочек.
В результате при дефекте межжелудочковой перегородки у новорожденных в органы поступает недостаточно насыщенная кислородом кровь, и происходит их голодание.
Симптомы дефекта межжелудочковой перегородки у новорожденных
В зависимости от размера отверстия при ДМЖП симптомы могут значительно различаться.
Небольшой дефект межжелудочковой перегородки у новорожденных мало влияет на качество их жизни, но характеризуется выраженным шумом в сердце. Проходящая через узкое отверстие кровь издает много звуков, что четко выслушивается доктором.
Кардиологи знают, что чем опаснее порок, тем меньше он издает звуков. Крупные отверстия ДМЖП у детей с первых часов после рождения дают о себе знать. Ребенок плохо прибавляет в весе, его кожа бледная или бледно-синюшная. Систолический шум при выслушивании сердца может быть не очень интенсивным, но постоянным.
Впоследствии при ДМЖП к симптомам добавляется быстрая утомляемость, высокая частота инфекционных процессов дыхательной системы, развитие недостаточности сердца.
Чем опасен дефект межжелудочковой перегородки
Дефект межжелудочковой перегородки у ребенка вызывает резкую перегрузку сердечной мышцы и травму легочных сосудов.
Постоянное повышение давления в кровеносной системе легких вызывает склероз, утолщение артерий, повышение массы правого желудочка.
В результате смешивания бедной и богатой кислородом крови возникает постоянное кислородное голодание тканей ребенка, больше всего страдают наиболее чувствительные органы: головной мозг, почки, сердце.
Родители должны четко осознавать чем опасен дефект межжелудочковой перегородки для понимания важности правильного лечения.
ДМЖП у плода: что делать, и когда нужна операция?
При таком пороке сердца как дефект межжелудочковой перегородки операция — наиболее эффективное и надежное средство лечения.
На сегодняшний момент ни одно лекарство или процедура не способны вызвать произвольное закрытие отверстия перегородки сердца. Дефект возможно лишь ушить или закрыть трансплантатом.
В ряде случаев происходит самостоятельное исчезновение небольших дефектов, что избавляет от необходимости вмешательства. Крошечные отверстия перегородки без существенных нарушений кровотока позволяют применить выжидательную тактику до 6 — 36 месяцев.
Тем не менее, большие дефекты являются абсолютным показанием к хирургии. В зависимости от размеров дефекта и общего состояния новорожденного операция ДМЖП у ребенка может выполняться в первые месяцы жизни или откладываться до определенного срока.
Выбор метода вмешательства и времени его выполнения зависит от общего состояния ребенка, расположения и размера дефекта, давления в желудочках и предсердиях сердца, наличия противопоказаний.
Крупные дефекты ушиваются после рассечения грудной клетки и камеры сердца. Операция проводится при помощи аппарата искусственного кровообращения большой бригадой опытных хирургов. Риск осложнений сводится до статистического минимума благодаря современному оборудованию и высочайшему мастерству оперирующих кардиохирургов.
В случае обнаружения небольших отверстий в перегородке предпочтение может отдаваться эндоваскулярной хирургии. Достоинствами методики являются отсутствие разрезов и меньший риск нежелательных последствий. Устранение дефекта при этом производится специальным устройством, которое вводится в сердечно-сосудистую систему через небольшой прокол бедренной артерии.
Эндоваскулярной техникой нельзя провести лечение детей с большими дефектами и выраженной недостаточностью сердца.
В нашем центре есть все необходимое для лечения детей с указанной патологией.
На первичной консультации доктор подробно расскажет о прогнозах и степени ДМЖП у плода, и что делать с имеющейся проблемой дальше.
При необходимости операции она будет выполнена в наилучших для этого условиях — современной оснащенной операционной коллективом из самых опытных кардиохирургов.

Что такое дефект межпредсердной перегородки?
В нормальном сердце правые и левые отделы разделены между собой тонкой стенкой, так называемой перегородкой. Дефект межпредсердной перегородки это отверстие между камерами сердца – левым и правым предсердиями (Рис 1). Давление в левых отделах сердца в норме выше, чем правых. Кровь из левого предсердия попадает в правое передсердие, затем в правый желудочек и легочную артерию, вызывая растяжение и перегрузку этих отделов сердца. Это в свою очередь приводит к ряду неприятных проблем.
Естественное течение порока. Или к чему приведет дефект межпредсердной перегородки?
Перегруженные кровью правый желудочек и правое предсердие увеличиваются в размерах, что приводит к нарушению работы сердца, развитию сердечной недостаточности и различных аритмий. Порок проявляется отдышкой, постоянным чувством усталости, а в запущенных случаях – отеками и ощущением перебоев в работе сердца. Перегрузка кровью легочной артерии приводит к развитию частых бронхо-легочных заболеваний, а в запущенных случаях – к необратимым изменениям со стороны сосудов легких, их склерозу. В таких случаях закрытие дефекта межпредсердной перегородки противопоказано.
Что такое открытое овальное окно?
У некоторых здоровых людей есть небольшая щель между предсердиями, которая называется открытым овальным окном. Такая щель есть у плода в утробе матери и, как правило, закрывается она самостоятельно в первые несколько месяцев жизни. Открытое овальное окно не является пороком развития и не приводит к развитию тех симптомов, которые проявляются при дефекте межпредсердной перегородки. Довольно редко у взрослых людей открытое овальное окно может привести к развитию внезапной тромбоэмболии сосудов головного мозга (инсульту у лиц молодого возраста). Только в этом случае открытое овальное окно требует эндоваскулярного закрытия.
Лечение дефекта межпредсердной перегородки.
Показанием для выполнения операции является перегрузка и увеличение правых отделов сердца. Оптимальный возраст для операции при неосложненном течении - дошкольный. В случае большого дефекта межпредсердной перегородки, значительного сброса крови, при появлении и нарастании симптомов сердечной недостаточности операция должна быть выполнена вне зависимости от возраста пациента. На сегодняшний день существует два способа закрытия дефектов: эндоваскулярный способ и операция в условиях искусственного кровообращения (ушивание ДМПП или закрытие его заплатой).
Эндоваскулярное закрытие ДМПП
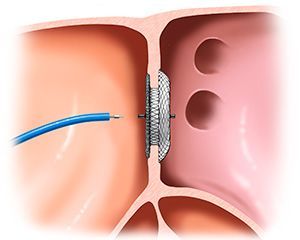
В последние два десятилетие появились устройства, позволяющие выполнить закрытие дефекта межпредсердной перегородки не прибегая к открытому вмешательству, требующему разреза, проведения искусственного кровообращения и длительной реабилитации. Для выполнения этой манипуляции было предложено большое количество специальных устройств - окклюдеров (Рис 2 - 4).
Рис 2 – Внешний вид окклюдера
Рис 3 – Окклюдер на системе доставки
Рис 4 – Окклюдер может растягиваться и деформироваться, но в сердце он примет нужную нам форму
Устройство представляет собой два диска из нитинола (сплав элементов титана и никеля, обладает эффектом памяти формы), заполненные тонкими нитями из дакрона (синтетический полимер). В сложенном состоянии окклюдер располагается в тоненькой трубочке – катетере (Рис 5 - 7).
Рис 5 – Окклюдер частично сложен в систему доставки (вид сзади)
Рис 6 – Окклюдер частично сложен в систему доставки (вид спереди)
Рис 7 – Окклюдер полностью сложен в систему доставки диаметром всего в 4 мм
Материалы, из которых сделан окклюдер полностью биосовместимые и гипоалергенные, не имеют магнитных свойств. Эндоваскулярное вмешательство выполняется в условиях рентгеноперационной. Перед проведением операции эндоваскулярного закрытия дефекта межпредсердной перегородки всем пациентам проводится транспищеводное ультразвуковое исследование сердца (УЗИ). Поскольку наше сердце располагается непосредсдвенно за пищеводом, транспищеводное УЗИ дает полную информацию об анатомии такого порока сердца.
Рис 8 – Транспищеводная ЭхоКГ
Рис 9 – Измерение размера дефекта по данным ЭхоКГ
Рис 10 – Измерение размера дефекта с помощью измерительного баллона, который заведен и раздут в отверстии между предсердиями. Размер перетяжки на баллоне соответствует размеру дефекта.
Рис 11 – Система доставки заведена в бедренную вену
Рис 12 – Дефект закрыт окклюдером (транспищеводная ЭхоКГ)
Только этот метод диагностики позволит точно определить показания и противопоказания к эндоваскулярному лечению (Рис 8). Транспищеводный датчик у большинства пациентов вызывает дискомфорт, поэтому операция закрытия дефекта межпредсердной перегородки окклюдером проводится под наркозом. Ни разреза грудной клетки, ни использования аппарата искусственного кровообращения при этом не требуется.
2). Если окклюдер установлен правильно, катетер отсоединяется и извлекается наружу, если произошло смещение, окклюдер может быть снова втянут в доставляющий катетер и процесс установки повторится. Продолжительность вышеописанной процедуры, включая подготовку пациента - около часа. Через сутки после операции проводится контрольное обследование и пациента выписывают. После выписки пациент находится под наблюдением кардиохирурга, с периодичностью сначала в один, затем в три месяца выполняется эхокардиография для контроля положения окклюдера и герметичности межпредсердной перегородки. На сегодняшний день более чем у 90% пациентов дефект межпредсердной перегородки может быть устранен при помощи эндоваскулярной операции. В то же время имеются противопоказания. Это огромные дефекты без краев, что делает невозможным надежную фиксацию окклюдера, наличие у пациента других внутрисердечных аномалий (часто это бывает аномальный дренаж одной или нескольких легочных вен), требующих хирургической коррекции. Отсутствие аортального края или аневризма перегородки не являются противопоказаниями к эндоваскулярному лечению порока. Хочется отметить, что возможность закрытия дефекта окклюдером могут точно определить лишь опытный УЗИ-специалист или эндоваскулярный хирург после проведения транспищеводной ЭхоКГ. На данные обычной трансторакальной ЭхоКГ ориентироваться можно лишь условно.
Реабилитация после процедуры
Как правило, пациентов выписывают на следующий день после процедуры. На месте введения катетера в сосуд еще некоторое время должна оставаться стерильная повязка. Некоторое время после процедуры вы будете чувствовать дискомфорт в горле, обусловленный введением транспищеводного датчика. В течение 6 месяцев после операции вы будете принимать аспирин для профилактики тромбообразования и в случае простудных заболеваний проводить антибиотикопрофилактику инфекционного эндокардита. В течение одного месяца после процедуры необходимо будет ограничить физические нагрузки. Уже через 6 месяцев после операции окклюдер полностью покрывается собственными клеточками сердца – эндотелизируется. До этого времени пациентам стоит воздержаться от плановой вакцинации и планирования беременности. Спустя 6 месяцев наш пациент может вести привычный для него образ жизни – теперь он абсолютно здоров! У нас наибольший в Украине опыт по эндоваскулярному закрытию вторичного дефекта межпредсердной перегородки – более 350 операций. Мы имеем доступ к оборудованию для закрытия дефектов любых размеров. Для того чтобы попасть к нам на консультацию или госпитализироваться позвоните по одному из телефонов или запишитесь на прием онлайн.
Видео 1 – В этой красочной анимации Вы сможете увидеть, как закрывают дефект межпередсердной перегородки окклюдером.
ДМПП составляют неоднородную группу аномалий эмбрионального развития межпредсердной перегородки. Они различаются:
- по расположению дефекта: центральный, верхний, нижний, задний, передний;
- по размеру дефекта: от небольшого щелевидного отверстия (например, при незаращении овального отверстия), до полного отсутствия межпредсердной перегородки (единое предсердие);
- по количеству дефектов: от 1-2 до множественных.

Автоматизация клиники: быстро и недорого!
- Подключено 300 клиник из 4 стран
- 800 RUB / 4500 KZT / 27 BYN - 1 рабочее место в месяц

Автоматизация клиники: быстро и недорого!
- Подключено 300 клиник из 4 стран
- 1 место - 800 RUB / 4500 KZT / 27 BYN в месяц
Мне интересно! Свяжитесь со мной
Классификация
1. Первичный ДМПП (частичный дефект атриовентрикулярной перегородки, частичный атриовентрикулярный канал). Составляет около 15% от всех ДМПП. Локализуется в месте соединения всех четырех камер сердца. При этом атриовентрикулярные клапаны, как правило, деформированы, что осложняется регургитацией крови различной степени тяжести.
2. Вторичный ДМПП. Составляет 80% от всех ДМПП. Локализуется в области овальной ямки или рядом с ней.
3. Дефект синуса верхней полой вены. Составляет 5% от всех ДМПП. Локализуется в области впадения верхней полой вены. Сочетается с частичным или полным соединением между правыми легочными венами и верхней полой веной или правым предсердием.
4. Дефект синуса нижней полой вены. Составляет менее 1% от всех ДМПП. Локализуется в области впадения нижней полой вены.
5. Локализованный ДМПП у коронарного синуса (дефект крыши коронарного синуса). Составляет менее 1% от всех ДМПП. Характеризуется частичным либо полным отсутствием отделения от левого предсердия.
ДМПП часто сочетается с другими пороками:
- аномальное соединение легочных вен;
- персистирующая левая верхняя полая вена;
- стеноз клапанов легочного ствола;
- пролапс митрального клапана;
- вторичный ДМПП может сочетаться с патологией верхней конечности (синдром "рука-сердце", синдром Холта-Орама): наблюдается деформация верхней конечности.
Этиология и патогенез
Анатомическая характеристика дефектов межпредсердной перегородки (ДМПП) разнообразна и заключается не только в величине и количестве отверстий, но и в их локализации.
По эмбриологическому происхождению
2. Вторичный распространенная форма порока; составляет 85−98% от общего числа изолированных ДМПП. При вторичных ДМПП всегда сохраняется край межпредсердной перегородки в нижнем отделе, которым он отделен от уровня клапанов. Расположение дефекта может быть различным, и на основании этого принципа выделяют 6 форм.
3. Единственное встречающийся порок. Для единственного предсердия характерны:
- дефект больших размеров, занимающий по площади всю межпредсердную перегородку;
- отсутствие остатка перегородки в нижнем отделе;
- патология клапанов.
Основным признаком нарушения при ДМПП является сброс артериальной крови из левого предсердия в правое. Величина сброса варьирует в широких пределах, но обычно достигает 10-15 л/мин.
Сброс крови слева направо, благодаря большой резервной возможности и низкой сопротивляемости сосудистого русла легких, не приводит к быстрому и значительному повышению давления в правом желудочке. Возрастает прежде всего объемная нагрузка, и работа правого желудочка увеличивается в несколько раз.
При большом сбросе крови через дефект нередко возникает перепад давления между правым желудочком и легочной артерией. Появление перепада связано с возникновением относительного стеноза на уровне фиброзного кольца, которое не расширяется в такой степени, как легочная артерия и полость правого желудочка.
Длительное поступление большого количества крови в сосуды легких отражается на динамике кровообращения малого круга и постепенно приводит к развитию легочной гипертензии Легочная гипертензия - повышенное давление крови в сосудах малого круга кровообращения
.
При длительном течении заболевания функциональные механизмы повышения давления постепенно заменяются органической обструкцией легочных артериол.
Высокая легочная гипертензия у детей наблюдается крайне редко. Как правило, она появляется после 16-20 лет, и частота ее увеличивается по мере увеличения возраста больных.
Эпидемиология
Дефект межпредсердной перегородки (ДМПП) встречается в 3-20% случаев от всех врожденных сердечных пороков.
ДМПП чаще встречается у женщин.
Продолжительность жизни при данном пороке составляет в среднем около 25 лет.
Порок диагностируется при рождении или в течение первого года жизни у 40% больных, у остальных - в возрасте 2-5 лет.
Факторы и группы риска
Факторы риска, влияющие на формирование врожденных пороков сердца у плода
Семейные факторы риска:
- наличие детей с врожденными пороками сердца (ВПС);
- наличие ВПС у отца или ближайших родственников;
- наследственные заболевания в семье.
Клиническая картина
Клинические критерии диагностики
Cимптомы, течение
Клинически дефект межпредсердной перегородки (ДМПП) относится к гемодинамически длительно компенсированным и маломанифестным порокам. Выраженность его симптоматики зависит от величины и локализации дефекта, а также от длительности существования порока и развития вторичных осложнений.
При дефектах среднего и большого размера первые признаки врожденного порока сердца могут обнаруживаться уже в первом полугодии или к концу года жизни.
Заболевание проявляется следующими признаками:
- стойкая бледность;
- умеренное отставание в физическом развитии;
- недостаточный прирост массы тела;
- склонность к частому возникновению респираторных заболеваний, особенно рецидивирующим бронхитам (реже - пневмониям).
Респираторные заболевания при ДМПП могут протекать со скудными общеклиническими и острофазовыми показателями, но с выраженной физикальной симптоматикой со стороны легких (длительный влажный кашель, обильные рецидивирующие влажные хрипы, стойкая одышка и другие). Это обусловлено наличием гиперволемии Гиперволемия (плетора) - наличие в сосудистом русле увеличенного объема циркулирующей крови
малого круга кровообращения.
В связи с частичным "обкрадыванием" большого круга кровообращения и недостаточным притоком крови на периферию, к 5-7 годам жизни дети чаще выглядят бледными, субтильными, умеренно равномерно отставая в росте, массе тела и физическом развитии. Предположительно это обуславливает склонность таких детей к головокружениям, обморокам, а также характерные жалобы на быструю утомляемость и одышку при физической нагрузке.
В некоторых случаях быстрая утомляемость и одышка, неадекватные нагрузке, являются единственными жалобами на фоне отсутствия или неопределенности какой-либо другой симптоматики.
Появляющиеся позже жалобы на колотье в сердце, перебои, сердцебиение и чувство замирания связаны с перегрузкой правых отделов сердца на фоне неадекватно низкого коронарного кровотока.
При небольшой величине дефекта (до 10-15 мм) дети развиваются нормально, удовлетворительно переносят нагрузки. Первые симптомы порока могут появляться у них в возрасте старше 10 лет.
Границы сердца увеличены вправо и вверх за счет предсердий, но при больших дефектах и в старшем возрасте отмечается также расширение левой границы сердца, как правило, за счет правого желудочка, оттесняющего левый желудочек кзади. Выраженная кардиомегалия Кардиомегалия - значительное увеличение размеров сердца за счет его гипертрофии и дилатации
возникает редко.
Аускультация
I тон чаще усилен. II тон, как правило, усилен и расщеплен над легочной артерией.
Диагностика
1. Рентгенография грудной клетки. Наиболее часто выявляется нормальное или легкое увеличение кардиоторакального индекса с усилением сосудистого легочного рисунка и расширением центральной легочной артерии.
2. ЭКГ. Наиболее частые признаки:
- отклонение электрической оси вправо;
- гипертрофия правого желудочка;
- удлинение комплекса QRS ‹120 мс в правых отведениях с неполной блокадой правой ножки Гиса;
- в случае дефекта первичного отверстия наблюдается отклонение электрической оси влево на фоне гипертрофии правого желудочка.
3. Эхокардиография. Наиболее важные признаки включают дилатацию правого предсердия и правого желудочка, часто сопровождающиеся дилатацией легочной артерии. Правые отделы сердца испытывают перегрузки объемом, что может приводить к парадоксальным (вперед при систоле) движениям межжелудочковой перегородки.
Предсердный дефект нужно визуализировать непосредственно, что чаще всего удается при субкостальном доступе. Обследование должно включать определение размера и количества дефектов, локализацию в перегородке, описание краев, количество и ассоциированные аномалии (например, аномальный дренаж легочных вен).
Визуализация дефекта венозного синуса может оказаться затруднительной, но он должен подозреваться у всех пациентов с непонятным увеличением правых отделов сердца.
4. МРТ и КТ сердца являются альтернативными методами исследования, если при эхокардиограмме не было получено достаточно данных. В частности, при оценке перегрузки объемом правого желудочка и состояния легочных венозных анастомозов.
5. Катетеризация сердца. Проводится пациентам с высоким легочным артериальным давлением (по данным эхокардиографического исследования) для определения легочного сосудистого сопротивления .
Дифференциальный диагноз
Дифференциальную диагностику дефекта межпредсердной перегородки с большим сбросом следует проводить:
1. С врожденными пороками сердца, протекающими с обогащением малого круга кровообращения (дефект межжелудочковой перегородки, открытый артериальный проток, аномальный дренаж легочных вен, атриовентрикулярная коммуникация).
2. С умеренным изолированным стенозом легочной артерии.
При малых вторичных дефектах межпредсердной перегородки необходимо проводить дифференциальную диагностику с функциональной кардиопатией и нейроциркуляторной дистонией.
Осложнения
Дефект межпредсердной перегородки может осложнятся инфекционным эндокардитом, однако реже, чем другие врожденные пороки сердца.
Относительно частым осложнением является ревматизм (10% случаев).
Лечение
Хирургическая коррекция
Оптимальный возраст проведения операции - 5-12 лет.
Операция не показана:
1. Больным в бессимптомной стадии доказанного порока, при которой отсутствуют жалобы и определенная клиническая симптоматика, изменения на ЭКГ, а единственный признак порока - наличие аускультативной и эхокардиографической симптоматики.
2. Пациентам в терминальной стадии заболевания, с выраженной легочной гипертензией, у которых произошла смена шунта на веноартериальный, с цианозом и нарушениями в обоих кругах кровообращения.
3. Не следует закрывать дефект у пациентов с физиологией Эйзенменгера (класс рекомендаций: III, уровень доказательности: C).
Показания к проведению коррекции дефекта межпредсердной перегородки (ДМПП):
1. Пациентам со значительным сбросом крови (есть признаки перегрузки правого желудочка объемом) и легочным сосудистым сопротивлением 1,5) следует рассматривать как кандидатов на закрытие дефекта (класс рекомендаций: IIb, уровень доказательности: C).
При ранней хирургической коррекции дефекта и при отсутствии легочной артериальной гипертензии отмечается низкий уровень смертности (менее 1 % больных без серьезных сопутствующих заболеваниях) и хороший отдаленный прогноз (нормальная продолжительность жизни и низкий уровень заболеваемости в отдаленном будущем).
Летальный исход наблюдается чаще среди пожилых пациентов и пациентов с сопутствующими заболеваниями.
Прогноз
Естественное течение дефекта межпредсердной перегородки (ДМПП) и прогноз определяются размером дефекта и величиной артериовенозного сброса.
Дети с вторичными ДМПП и малым сбросом крови развиваются нормально, не предъявляют жалоб, многие годы у них сохраняется физическая работоспособность, а первые симптомы неблагополучия иногда выявляются лишь в третьем десятилетии жизни. Однако в дальнейшем заболевание быстро прогрессирует, и большая часть пациентов умирает в возрасте до 40 лет, оставшаяся часть больных к 50 годам становятся инвалидами.
Описаны случаи, когда больные с вторичным ДМПП доживали до 70-80 лет. У некоторых пациентов с небольшим дефектом происходит спонтанное закрытие дефекта в течение первых 2- 5 лет жизни.
Младенческая смертность в основном обусловлена первичным ДМПП и (или) наличием ДМПП, дефектов атриовентрикулярных клапанов, а также сочетанием ДМПП с другими экстракардиальными врожденными аномалиями. Непосредственными причинами смерти чаще всего являются тяжелые вирусные инфекции, рецидивирующие пневмонии, кишечные инфекции.
Профилактика
Профилактика возникновения врожденных пороков сердца (ВПС) очень сложна и в большинстве случаев сводится к медико-генетическому консультированию и разъяснительной работе среди людей, относящихся к группе повышенного риска заболевания. К примеру, в случае, когда 3 человека, состоящие в прямом родстве, имеют ВПС, вероятность появления следующего случая составляет 65-100% и беременность не рекомендуется. Нежелателен брак между двумя людьми с ВПС. Помимо этого необходимо тщательное наблюдение и исследование женщин, имевших контакт с вирусом краснухи или имеющих сопутствующую патологию, которая может привести к развитию ВПС.
Профилактика неблагоприятного развития ВПС:
- своевременное выявление порока;
- обеспечение надлежащего ухода за ребенком с ВПС;
- определение оптимального метода коррекции порока (чаще всего, это хирургическая коррекция).
Обеспечение необходимого ухода является важной составляющей в лечении ВПС и профилактике неблагоприятного развития, так как около половины случаев смерти детей до 1-го года во многом обуславливаются недостаточно адекватным и грамотным уходом за больным ребенком.
Специальное лечение ВПС, (в том числе, кардиохирургическое) должно проводиться в наиболее оптимальные сроки, а не немедленно по выявлению порока, и не в самые ранние сроки. Исключение составляют только критические случаи угрозы жизни ребенка. Оптимальные сроки зависят от естественного развития соответствующего порока и от возможностей кардиохирургического отделения.
Профилактика осложнений ВПС определяется характером осложнений.
Грозным осложнением ВПС является инфекционный эндокардит Инфекционный эндокардит - это инфекционное полипозно-язвенное воспаление эндокарда, сопровождающееся образованием вегетаций на клапанах или подклапанных структурах, их деструкцией, нарушением функции и формированием недостаточности клапана
Подробно , который может осложнить любой вид порока и может появиться уже в дошкольном возрасте.
Рекомендуется ограничить назначение антибиотикопрофилактики инфекционного эндокардита группам пациентов с наибольшей вероятностью развития инфекционного эндокардита:
1. Пациенты после протезирования клапана сердца.
2. Инфекционный эндoкардит в анамнезе.
3. Пациенты со следующими врожденными пороками:
- "синие" пороки, без предшествующей хирургической коррекции или с остаточными дефектами, паллиативными шунтами или кондуитами;
- пороки после хирургической коррекции с применением искусственных материалов до 6 месяцев (до тех пор, пока не произошла эндотелизация);
- если после операции на сердце или чрескожной коррекции есть остаточный дефект в месте имплантации искусственного материала или устройства.
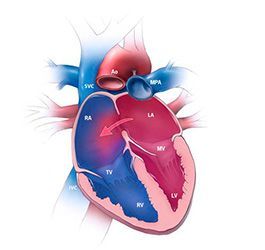
Сердце – это сложный орган, состоящий из нескольких отделов. В норме левые и правые отделы должны быть надежно разделены. В ходе развития и роста организма может появиться такой дефект как врожденный порок сердца или дефект междпредсердной перегородки (ДМПП) – так в медицине называют неполное закрытие перегородки между отделами. Если появляется отверстие между двумя предсердиями, это сказывается на работе сердца и общем состоянии организма. Правильная циркуляция достигается разницей давлений, поддерживать которую помогает перегородка. В ее отсутствии кровь циркулирует из левого предсердия в правое, затем идет дальше по соответствующему кругу кровообращения. Перегрузка сердечной мышцы может привести к серьезным проблемам со здоровьем, поэтому дефект стараются устранить сразу после выявления.
Эндоваскулярное закрытие дефекта межпредсердной перегородки (без стоимости устройства для закрытия) - 90 000 - 140 000 руб.
манипуляция, обезболивание, пребывание в стационаре, медикаменты и питание (стоимость окклюдера оплачивается отдельно).
Чем опасна патология?
На первый взгляд может показаться, что закрытие дефекта межпредсердной перегородки – это не срочная процедура. На самом деле отделы правой стороны сердца несут повышенную нагрузку, со временем они увеличиваются в размерах. Результат – сердечная недостаточность и аритмия, одышка, постоянная усталость, отеки и дискомфорт в области груди. Они могут привести к развитию хронических заболеваний.
От избыточной нагрузки страдает и легочная артерия, с которой начинается малый круг кровообращения. Это приводит к бронхо-легочным болезням. В особо сложных случаях может развиться склероз сосудов легких – необратимое изменение, которое уже не поддается лечению и является противопоказанием для закрытия дефекта. Поэтому важно вовремя начинать диагностику и лечение, не дожидаясь осложнений со стороны сердца и дыхательной системы.
У здоровых людей также существует отверстие в перегородке, которое называется овальным окном – и представляет собой небольшую щель между предсердиями. Она формируется еще в период эмбрионального развития и у некоторых остается во взрослой жизни. Если не наблюдается неприятных симптомов, то окно, сохранившееся во взрослом возрасте, не требует лечения и не считается заболеванием. Но в редких случаях оно может вызывать сосудистые патологии – в таком случае предусмотрено хирургическое лечение.
Эндоваскулярное лечение порока сердца – это наиболее современная операция, которая позволяет закрыть дефект перегородки. Если нет осложнений, то рекомендуется проводить операцию в возрасте до 7 лет. Если дефект выявлен позже, то рекомендуется лечение вне зависимости от возраста. При нарастании симптоматики операцию можно проводить даже совсем маленьким детям.
- наличие дефекта межпредсердной перегородки;
- симптомы перегрузки сердца,
- увеличение отделов сердца.
- высокая вероятность тромбоэмболии;
- нарушение свертываемости крови;
- индивидуальные реакции непереносимости антикоагулянтов;
- сочетание ДМПП с другими пороками сердца, требующими более сложного вмешательства;
- наличие отверстий в перегородке больше одного;
- диаметр отверстия слишком большой для заплатки-окклюдера;
- острое инфекционное или воспалительное.
Преимущества эндоваскулярной методики
Эндоваскулярный способ закрытия дефекта выгодно отличается от операции по ушиванию ДМПП. Последняя требует искусственного поддержания кровообращения во время операции, имеет больше противопоказаний и значительный период реабилитации. Несмотря на то, что хирургическое лечение прочно вошло в практику и применялось долгое время, сейчас оно уступает место эндоваскулярному методу.
Главное преимущество в том, что эндоваскулярная операция – это малоинвазивная хирургия. После нее не остается шрамов, процедура не требует разрезов или открытого доступа. У эндоваскулярного метода чрезвычайно низкий процент послеоперационных осложнений. Пациентам не требуется длительная госпитализация и реабилитация.
На данный момент эндоваскулярная операция – это общепризнанный мировой стандарт, отвечающий всем требованиями безопасности и эффективности.
Принцип работы окклюдера
Впервые операция с помощью окклюдера была произведена в конце 80-х годов прошлого века – это был эксперимент на животных. Окклюдер – это специальное устройство, которое устанавливают через сосудистый доступ, а после установки оно выполняет функцию заплатки. Со временем техника выполнения таких операций совершенствовалась, и сейчас успешно применяется для лечения тысяч пациентов. Уже в 21 веке появилось множество модификаций и разновидностей окклюдеров для разных случаев.
Принцип работы устройства следующий: конструкция, раскрывающаяся подобно зонтику, заводится в нужное место через сосуд. После установки заплатки никаких других манипуляций не требуется. Окклюдер производят из сплавов металлов, давно применяемых в медицине – из никеля и титана, покрытых сверху специальным биосовместимым волокном. Материалы протестированы множество раз, они не вызывают аллергии. Устройство сконструировано таким образом, что центровка в отверстии перегородки происходит самостоятельно – задача врача довести окклюдер по сосудам до нужного места. Модель устройства подбирается в зависимости от конкретного дефекта – существуют разные модификации для лечения разных пороков сердца.
Доставка к сердцу производится с помощью катетера, который заводят в крупный сосуд – артерию или вену бедра. Размер окклюдера не больше 2,5 мм в диаметре, поэтому он спокойно проходит по сосудистому руслу. Устройство раскрывается только после установки в соответствующее положение рядом с дефектом перегородки.
Операция выполняется квалифицированными врачами, прошедшими специальное обучение. Процедура проводится в операционной. Пациент во время операции лежит. Врач может контролировать все свои действия с помощью специального оборудования, передающего изображение на мониторы. В ходе операции проводится мониторинг жизненных показателей.
Читайте также:
- Кто не обязан вносить плату за негативное воздействие на окружающую среду
- Статья 113 уголовного кодекса российской федерации о чем гласит
- В оказании бесплатной юридической помощи может быть отказано если гражданин обратившийся
- Как посмотреть результаты анализов через госуслуги
- Для чего нужны забастовки

