Метаболические изменения миокарда берут ли в армию
Обновлено: 09.05.2024
Рассмотрены причины метаболических кардиомиопатий (КМП), возникающих на фоне нарушений обмена жирных кислот. Выделены экстракардиальные и кардиальные критерии диагностики. Ранняя диагностика позволяет своевременно начать специфическое лечение, направленно
Diagnostics and treatment of metabolic cardiomyopathy in children appearing during the disorders of the exchange of the fatty acids
Are examined the reasons for metabolic cardiomyopathy (KMP), disturbances of the exchange of fatty acids appearing against the background. The extracardial and cardiac criteria of diagnostics are listed. Early diagnostics makes it possible to begin the specific treatment in proper time, directed toward the correction of metabolic disorders.
Кардиомиопатии (КМП) — гетерогенная группа заболеваний сердца, характеризующихся структурной перестройкой миокарда, с непрерывно прогрессирующим течением и неблагоприятным прогнозом. В большинстве случаев диагностика КМП основывается на клинических симптомах и данных функционального обследования, в первую очередь эхокардиографии [1–3]. При этом истинная этиология КМП не всегда устанавливается. По данным наиболее крупного регистра КМП у детей США и Канады среди группы, в которой причина КМП была установлена, в 29,1% был диагностирован миокардит, в 24,2% — семейная изолированная КМП, в 22,2% — нейромышечные заболевания, в 15,4% — врожденные нарушения метаболизма и в 8,8% — различные генетические синдромы [3–6].
Причинами метаболических КМП являются врожденные нарушения обмена веществ или нарушения функции органелл клетки. Нарушения метаболизма жирных кислот являются наиболее частой причиной развития метаболических КМП. По данным педиатрического регистра при гипертрофических КМП в 20% случаев выявлены нарушения транспорта карнитина или дефекты окисления жирных кислот, нарушения окислительного фосфорилирования [7]. При дилатационных КМП дефекты транспорта карнитина/нарушения оксидации жирных кислот встречаются в 40% [8]. Наследственные дефекты обмена жирных кислот являются причиной не менее 5% случаев внезапной детской смерти [9].
Нарушения метаболизма жирных кислот могут возникать вследствие дефицита карнитина, нарушения транспорта карнитина при недостаточности ферментов, обеспечивающих перенос соединений карнитина, а также при дефектах оксидации жирных кислот [10].
Дефицит карнитина можно определить как дефицит внутриклеточного содержания карнитина, при котором концентрация карнитина в плазме менее 20 мкмоль/л, а содержание карнитина в тканях менее 20% от нормы. В зависимости от причины дефицита карнитина выделяют первичный дефицит карнитина, возникающий при генетически детерминированных дефектах метаболизма карнитина, и вторичный дефицит карнитина, связанный с нарушением обмена органических кислот, дефицитом ацил-КоА-дегидрогеназ, дефектами в цепи дыхательных ферментов митохондрий, рядом соматических заболеваний и патологических состояний [11].
Первичный дефицит карнитина может проявляться в двух формах: системной [13, 14] и мышечной [11, 16]. Системный дефицит карнитина обусловлен мутацией гена SLC22A5, локализованного на длинном плече 5-й хромосомы (5q319), продуктом которого является белок, переносящий карнитин (OCTN2). Результатом этой мутации является дефицит карнитина в тканях. Заболевание наследуется по аутосомно-рецессивному типу [13–14]. При гомозиготной форме сроки манифестации заболевания варьируют от 1 месяца до 7 лет, в среднем 2 года. При гетерозиготной форме манифестация заболевания возникает в подростковом возрасте [14–16].
При раннем дебюте заболевания первыми признаками являются отказ от кормления, раздражительность, низкая прибавка в весе, отставание в физическом и психомоторном развитии. Характерным признаком является гипокетотическая гипогликемическая энцефалопатия (вялость, сонливость, повторная рвота), имеющая приступообразное течение. Во время гипогликемического криза возникают общая слабость, тахикардия, церебральная дисфункция (повышенная возбудимость, раздражительность). В дальнейшем развиваются гепатомегалия, стеатоз печени, нарушения желудочно-кишечного тракта (боли в животе, диарея), скелетная миопатия (мышечная слабость, гипотония), синдром Рейе. Как правило, дети часто болеют интеркуррентными заболеваниями: инфекционные заболевания верхних дыхательных путей и острый гастроэнтерит. У ряда пациентов возникает гипохромная анемия. Тяжесть заболевания варьирует от легких до крайне тяжелых вариантов. При легком течении отставание в физическом и психомоторном развитии может быть единственным проявлением заболевания [14–16].
КМП развивается в 30–40% случаев системного дефицита карнитина. Она может быть изолированной или сочетаться с другими симптомами, обычно миопатией или печеночной энцефалопатией [15–19]. Первые признаки КМП появляются в 3–5 месяцев и, при отсутствии заместительной терапии, имеют плохой прогноз. Границы сердца резко расширены, аускультативно определяется глухость сердечных тонов, ритм галопа, систолический шум относительной недостаточности митрального и трикуспидального клапанов, реже диастолический шум, акцент II тона над легочной артерией, тахипноэ. Признаки сердечной недостаточности (СН) проявляются рано и быстро прогрессируют: нарастает тахикардия, одышка, гепатомегалия, выслушиваются застойные хрипы в легких, возникают отеки, возможно развитие асцита, накопление жидкости в перикарде и плевральных полостях [19]. Тромбоэмболические осложнения возникают у 20–25%. Симптомы СН могут маскировать мышечную гипотонию. Традиционное лечение СН малоэффективно [20]. Часто возникают нарушения сердечного ритма, предсердные или желудочковые аритмии, причиной которых является отложение липидных депозитов в миокарде [21]. На фоне гипогликемии в 10–20% случаев возникает выраженная транзиторная брадикардия, вплоть до асистолии, что может привести к внезапной смерть ребенка [10, 21].
У гетерозиготных носителей мутации гена SLC22 A5 карнитиновая недостаточность может проявиться в более старшем возрасте в виде гипертрофической КМП [16].
Лабораторные признаки системного дефицита карнитина: низкий уровень карнитина в тканях (печени, мышцах); приступы гипогликемии, не сопровождающиеся кетозом; повышение активности трансаминаз, уровня аммиака в крови; гипохромная анемия. Уровень свободного карнитина в крови обычно резко снижен. При исследовании методом тандемной масс-спектрометрии содержание свободного карнитина (С0) 70–100. В фибробластах снижена активность карнитинпальмитоилтрансферазы I (около 10% от нормы), окисление пальмитата составляет около 5% от нормы [23, 24].
Дефицит карнитинпальмитоилтрасферазы II. Наследование аутосомно-рецессивное, вызывается мутациями в гене карнитинпальмитоилтрансферазы II. Заболевание может протекать в трех формах: неонатальной (летальной), детской (инфантильной) и поздней (форма взрослых).
Неонатальная (летальная) форма характеризуется манифестацией с первых дней жизни, прогрессирующим течением, очень тяжелым состоянием детей и плохим прогнозом. Заболевание проявляется полиорганным поражением. У новорожденных развиваются гипотермия, летаргия, судороги, гипотония, гиперрефлексия и гепатомегалия, почечная недостаточность. Характерны дисморфии лица, контрактуры коленей и локтей, длинные сужающиеся пальцы рук и ног, гепатомегалия (макровезикулярный стеатоз), поликистоз почек, дисплазия почечной паренхимы, гидронефроз, тубулярные расстройства (проксимальный и дистальный канальциевый ацидоз), грубые изменения ЦНС (вентрикуломегалия, кальцификаты, дисплазия мозолистого тела, полимикрогирии, кисты паравентрикулярные и базальных ядер) [25].
Поражение сердца проявляется с рождения в виде гипертрофии левого желудочка или бивентрикулярной гипертрофии, реже возможно развитие кардиомегалии с низкой сократительной способностью сердца. В большинстве случаев регистрируются нарушения ритма сердца, возникновение желудочковой тахиакардии часто является причиной внезапной смерти [25].
Лабораторные признаки: некетотическая гипогликемия, увеличение в сыворотке, моче и тканях длинноцепочечных ацилкарнитинов (С16, С18), снижение плазменного общего и свободного карнитина, длинноцепочечная дикарбоновая ацидурия, гипераммониемия, увеличение общего билирубина, трансаминаз печени, кретинфосфокиназы, высокое содержание дикарбоксильных кислот в моче. Заболевание верифицируется выраженным снижением активности (менее 10% от нормы) карнитинпалмитоилтрансферазы II в большинстве тканей, отсутствием белка CPT II [24, 25].
При морфологическом исследовании обнаруживается накопление липидов в ткани печени, почек, скелетных мышц, легких, надпочечников и др.
Инфантильная форма манифестирует с 3 месяцев, провоцируется лихорадочными состояниями и нарушениями питания. Характерны гепатомегалия, миопатический синдром, судороги. Поражение сердца — по типу дилатационной КМП. Миопатическая форма (поздняя) протекает благоприятно, может дебютировать как в детском возрасте, так и у взрослых. Основные проявления: боли в мышцах, обычно сопровождающиеся миоглобинурией. Характерна высокая активность креатинфосфокиназы в крови, при голодании может возникать умеренный кетоз. Изменения со стороны сердца минимальны [24].
Дефицит карнитинацилкарнитинтранслоказы — редкое аутосомно-рецессивное заболевание, приводящее к нарушению утилизации длинноцепочечных жирных кислот [24]. Выделяют две формы заболевания: неонатальная и инфальтильная. Неонатальная форма характеризуется высокой летальностью вследствие сердечно-легочной недостаточности. Основные проявления: нарушение общего состояния и психомоторного развития, расстройства дыхания, изменения со стороны ЦНС в виде мышечной слабости, судорог, возможно развитие комы на фоне голодания, гепатомегалия с нарушением функции печени.
Поражение сердца встречается чаще по типу дилатационной КМП, характерно снижение систолической функции, возможны нарушения ритма: брадикардия, атриовентрикулярная блокада, желудочковая экстрасистолия, тахикардия. На ЭКГ — признаки гипертрофии левого желудочка. У новорожденных описаны случаи внезапной смерти вследствие апноэ, кардиореспираторного ареста. Если заболевание возникает в более позднем возрасте, то КМП протекает на фоне мышечной слабости и энцефалопатии [10, 26].
Отклонения в лабораторных показателях включают гипогликемию при отсутствии кетоза, увеличение в крови уровня аммиака, иногда калия и мочевой кислоты, высокую активность креатинфосфокиназы, трансаминаз, дикарбоксильную и гидроксидикарбоксильную ацидурию, а также увеличение уровня ацилкарнитинов в крови (С16–С18) в сочетании с низким уровень свободного карнитина (С0). Патология верифицируется низкой активностью карнитин-ацилкарнитин-транслоказы.
Дефекты окисления жирных кислот. Карнитин-ацилтрансферазы осуществляют перенос карнитина к ацильным компонентам коротких, средних и длинных цепей. Ацил-КоА-дегидрогеназы длинных цепей обеспечивают внутримитохондриальную бета-оксидацию жирных кислот с длинными карбоновыми цепями. Ацил-КоА-дегидрогеназы средних цепей регулируют внутримитохондриальное окисление жирных кислот средней длины карбоновых цепей. Ацил-КоА-дегидрогеназы коротких цепей обуславливают внутримитохондриальное окисление жирных кислот с короткой длиной карбоновых цепей, являются буфером ацильных групп, регулируя их поступление в цикл Кребса [27–29].
Дефицит ацил-КоА-дегидрогеназы жирных кислот с очень длинной углеродной цепью возникает в результате мутации гена дегидрогеназы очень длинной цепи ацил-КоА, наследование аутосомно-рецессивное. Мультисистемная патология: поражаются печень (гепатомегалия, стеатоз печени, гепатоцеллюлярный некроз), мышцы. Симптомами поражения мышц являются гипотония, мышечная слабость, связанная с голоданием или инфекцией, боль в мышцах при физической нагрузке, ригидность мышц, рабдомиолиз при физической нагрузке. Миопатические эпизоды вызваны физическими упражнениями, голоданием, инфекцией, воздействием низких температур. По срокам появления первых признаков выделяют 3 формы заболевания: неонатальную, детскую и позднюю [27–29].
Неонатальная форма характеризуется ранней манифестацией, в течение первых дней жизни, с развитием КМП и ранней смерти. Поражение сердца по типу гипертрофической КМП в сочетании со сниженной контрактильной способностью, часто возникают жизнеугрожающие нарушения сердечного ритма. Во время гипогликемической комы возможно развитие асистолии и внезапной смерти [30].
При детской форме (около 40% больных) начальные симптомы обычно появляются на протяжении первого года жизни. Поздняя форма характеризуется более благоприятным течением, манифестирует в подростковом возрасте, клинически проявляется болями в мышцах, как правило, сердце не вовлекается в патологический процесс.
Лабораторные признаки: некетоновая гипогликемия, дикарбоновая ацидурия, повышение концентрации лактата в крови. Диагностический маркер — снижение свободного карнитина при увеличении ацилкарнитинов (С14:1 и С14, С16OH), повышение активности креатинфосфокиназы, ацидурия дикарбоксильных кислот с длинной углеродной цепью (С14–С18) [23]. Специфична низкая активность дегидрогеназы очень длинной цепи ацил-КоА в фибробластах или мононуклеарных лейкоцитах.
Дефицит ацил-КоА-дегидрогеназы жирных кислот со средней длиной углеродной цепи возникает в результате мутации гена средней цепи ацил-КоА-дегидрогеназы, наследования аутосомно-рецессивное. Наиболее распространенное нарушение окисления жирных кислот [27, 29].
Клиническая картина варьирует от бессимптомной до молниеносной. Заболеванию свойственна острая манифестация. Провоцирующими факторами обычно служат сопутствующие болезни: острые респираторные заболевания, детские инфекционные болезни, желудочно-кишечные расстройства, оперативные вмешательства. Возраст появления первых признаков различный, чаще от 3 до 15 месяцев. Характерно приступообразное течение заболевания, обусловленное гипогликемическими кризами. Приступы протекают тяжело и могут заканчиваться летально, в 5% случаев смерть детей происходит в первые дни жизни, около 20% пациентов умирает до установления диагноза. Межприступный период протекает благоприятно, у 80% детей отмечается нормальное нервно-психическое развитие с полным отсутствием других признаков патологии. Клиническая симптоматика полиорганна: в процесс вовлекается желудочно-кишечный тракт (частая рвота, нарушение стула), гепатомегалия (стеатоз печени), ЦНС (задержка умственного развития, генерализованные тонико-клонические судороги, прогрессирующие вялость, сонливость, нарушение сознания вплоть до комы, отек головного мозга).
Характер поражения сердца аналогичен таковому при карнитиновой КМП. Часто возникают тяжелые нарушения сердечного ритма, остановка синусового узла, желудочковая тахикардия (по типу приступов пируэтной тахикардии (torsades de pointes)) [10, 30]. Дефицит ацил-КоА-дегидрогеназы жирных кислот со средней длиной углеродной цепи является в 1–3% причиной внезапной смерти у детей раннего возраста [10].
Лабораторные признаки: гипогликемия, метаболический ацидоз, дикарбоновая ацидурия средних цепей, ацилглицинурия, низкое содержание плазменного карнитина. Может отмечаться умеренная кетонурия. В крови повышен уровень среднецепочечных ацилкарнитинов (С6–С10). В моче определяется специфическая органическая ацидурия с преобладанием среднецепочечных дикарбоновых кислот, глициновых конъюгатов [27–28].
Дефицит ацил-КоА-дегидрогеназы жирных кислот с короткой длиной углеродной цепи. Возникает в результате мутации гена короткой цепи ацил-КоА-дегидрогеназы, наследование аутосомно-рецессивное.
Генерализованная форма может проявиться у новорожденных или детей первого года жизни, течение неблагоприятное, возможен летальный исход. Характерны судороги, задержка развития, микроцефалия, повторные приступы рвоты, прогрессирующая мышечная слабость, вялость, сонливость. Поражение сердца характеризуются дилатационной КМП, осложненной тяжелой СН. При мышечной форме первые признаки болезни появляются в старшем возрасте. В клинической картине на первый план выступают миопатические расстройства, низкая толерантность к физической нагрузке. Поражение сердца по типу дилатационной КМП протекает субклинически и выявляется обычно у подростков [29, 30].
Множественный дефицит ацил-КоА-дегидрогеназ описан как глутаровая ацидурия 2-го типа, наследование аутосомно-рецессивное. Патология обусловлена дефектом электронно-транспортного флавопротеина и дефицитом нескольких флавопротеин-содержащих дегидрогеназ, что значительно снижает эффективность митохондриального бета-окисления. Нарушены функции изовалерил-, изобутирил-, метилбутирил-, глутарил-КоА-дегидрогеназ, участвующих в метаболизме ряда аминокислот и холина.
Выделяют несколько клинических форм: неонатальную форму с врожденными аномалиями (летальную), неонатальную форму без врожденных аномалий, позднюю форму.
Метаболические проявления включают тяжелый метаболический ацидоз, гипогликемию, гипераммониемию. Кетоз выражен умеренно или отсутствует, гиперлактат- и гиперпируватемия с увеличением их соотношения до 20 и выше (норма
И. В. Леонтьева, доктор медицинских наук, профессор
Ю. М. Белозеров, доктор медицинских наук, профессор
ФГБУ НИИ педиатрии и детской хирургии Минздравсоцразвития России, Москва
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Кардиомиопатия: причины появления, симптомы, диагностика и способы лечения.
Определение
Кардиомиопатии (КМП) – группа гетерогенных (разнородных) заболеваний, характеризующихся патологией сердечной мышцы с ее структурными и/или функциональными нарушениями, не обусловленными ишемической болезнью сердца, гипертензией, клапанными пороками и врожденными заболеваниями.

Причины появления кардиомиопатий
Считается, что кардиомиопатия возникает как результат совокупности различных факторов: генетических (мутации генов), аутоиммунного воспаления (при некоторых бактериальных и вирусных заболеваниях), поражениях органов при генерализованном (полиорганном) заболевании.
Классификация кардиомиопатий
Согласно классификации Всемирной организации здравоохранения, кардиомиопатии делятся на идиопатические, специфические и неклассифицируемые болезни миокарда.
- дилатационная;
- гипертрофическая (обструктивная или необструктивная);
- рестриктивная;
- аритмогенная дисплазия правого желудочка;
- перипортальная (послеродовая).
- инфекционные;
- метаболические:
- эндокринные (при гипо- и гипертиреозе, микседеме, акромегалии, феохромоцитоме, сахарном диабете, ожирении),
- при болезнях накопления (амилоидозе, гемохроматозе, саркоидозе, лейкозе, мукополисахаридозе, гликогенозе, липидозе),
- при дефиците микроэлементов, питательных веществ и электролитном дисбалансе;
- одышка при физической нагрузке (у некоторых больных в покое и в ночные часы), обусловленная венозным застоем крови в легких из-за диастолической дисфункции увеличенного левого желудочка сердца;
- кардиалгии, связанные с несоответствием коронарного кровотока весу миокарда;
- головокружения и синкопальные (обморочные) состояния; у детей они отмечаются при физической нагрузке и эмоциональном стрессе;
- учащенное сердцебиение из-за нарушений ритма сердца;
- быстрая утомляемость.
- Пожилой возраст. Чем старше человек, тем, согласно статистике, выше риск развития метаболического синдрома.
- Этническая принадлежность. Латиноамериканцы подвергаются наибольшему риску развития метаболического синдрома. Но это не значит, что россияне не страдают от данного заболевания.
- Ожирение. Как уже было сказано в начале, лишний вес повышает шансы заработать МС.
- Сахарный диабет. Вероятность получить метаболический синдром растет, если у пациентки был диабет во время беременности (гестационный диабет). Диабет 2 типа в семейной истории – тоже повод для пристального внимания за здоровьем.
- Прочие болезни. Риск метаболического синдрома выше, если у пациента был жировой гепатоз, синдром поликистозных яичников или апноэ во сне.
- Сахарный диабет 2 типа. Если не изменить образ жизни и не взять лишний вес под контроль, может развиться инсулинорезистентность, что может вызвать повышение уровня сахара в крови. В конечном итоге она приводит к диабету 2 типа.
- Заболевания сердца и сосудов. Высокий уровень холестерина и высокое кровяное давление способствуют образованию бляшек в артериях. Эти бляшки сужают артерии, что может привести к сердечному приступу или инсульту.
- изменение образа жизни;
- лечение ожирения;
- лечение нарушений углеводного обмена;
- лечение артериальной гипертонии;
- лечение дислипидемии.
- Инфекционные заболевания (вирусные, бактериальные, протозойные, грибковые, паразитарные).
- Аутоиммунные патологии (например, гигантоклеточный артериит, гранулематоз с полиангиитом).
- Тяжелые формы аллергических болезней.
- Ранее перенесенный миокардит.
- Токсическое воздействие на организм (прием сильнодействующих препаратов, алкогольное отравление, наркотики, ионизирующее излучение).
- первичные (изолированные);
- вторичные (симптоматические — как проявление системной патологии).
- инфекционные (вирусные, бактериальные, протозойные, паразитарные, грибковые);
- неинфекционные (аллергические, токсические); смешанные; идиопатические (невыясненный генез).
- острый миокардит сердца;
- хронический.
- Клинический анализ крови.
- СОЭ.
- Антитела к миокарду.
- СРБ.
- Бактериальный посев крови.
- Ревматоидный фактор.
- Антитела к стрептококку, миокарду.
- Общий белок.
- Миокардиальные маркеры.
- Антибиотики — показаны при миокардите бактериального генеза.
- Глюкокортикоиды — для снижения интенсивности аутоиммунной реакции.
- Антигистаминные — для блокировки медиаторов воспаления.
- НПВС — для снижения воспаления. Не назначают при вирусной этиологии (это же касается глюкокортикоидов) в первые 2–3 недели, поскольку возможно ускорение репликации вирусов, снижение выработки интерферона, увеличение повреждений миокарда.
- Медикаменты для снижения АД и частоты сокращений сердца для уменьшения нагрузки на орган.
- Диуретики для уменьшения отечности.
- Тромболитические препараты.
Клинические проявления варьируют от бессимптомных форм до тяжелых нарушений в работе сердца – вплоть до внезапной смерти, которая чаще всего регистрируется в детском или юношеском возрасте во время физической нагрузки или сразу после нее.
Пациентов беспокоят следующие симптомы:
Рестриктивная кардиомиопатия
При заболевании стенки желудочков становятся жесткими, нерастяжимыми (не обязательно утолщенными), что препятствует нормальному заполнению сердца кровью между ударами.
Симптоматика определяется тяжестью сердечной недостаточности, и длительное время заболевание может протекать бессимптомно. Пациентов беспокоят слабость, повышенная утомляемость, одышка даже при незначительной физической нагрузке, кашель, который может усиливаться в положении лежа, отеки, увеличение живота, у детей отставание в физическом развитии.
Аритмогенная кардиомиопатия правого желудочка
Заболевание характеризуется прогрессирующим замещением клеток сердца правого желудочка жировой или фиброзно-жировой тканью, приводящим к атрофии и истончению стенки желудочка, его дилатации.
Длительное время аритмогенная кардиомиопатия протекает бессимптомно, хотя органическое повреждение, лежащее в основе заболевания, медленно прогрессирует. Клинические признаки заболевания (сердцебиение, пароксизмальная тахикардия, головокружение и/или обмороки) обычно появляются в подростковом возрасте. Ведущими клиническими проявлениями являются жизнеугрожающие аритмии и внезапная остановка кровообращения, которая наступает во время физических нагрузок или напряженной спортивной активности.
Ишемическая кардиомиопатия
Заболевание обусловлено диффузными морфофункциональными нарушениями, развивающимися в результате хронической и эпизодов острой ишемии миокарда.
К развитию ишемической кардиомиопатии может привести обширный инфаркт миокарда или многочисленные мелкоочаговые инфаркты.
В типичных случаях клиническая картина включает стенокардию напряжения, кардиомегалию (увеличение сердца), хроническую сердечную недостаточность (причем у части больных отсутствуют клинические и ЭКГ-признаки стенокардии).
Симптомы идентичны проявлениям сердечной недостаточности у больных с дилатационной кардиомиопатией.
Гипертензивная кардиомиопатия
Заболевание развивается на фоне неконтролируемого повышенного артериального давления в течение долгого времени.
Интенсивность симптомов зависит от степени тяжести заболевания и характера его течения. К самым частым жалобам пациентов можно отнести боль и ощущение сдавленности в груди, одышку, кашель, отсутствие аппетита, периферические отеки.
Метаболическая кардиомиопатия
Метаболическая кардиомиопатия — невоспалительное поражение миокарда, в основе которого лежит нарушение обмена веществ, приводящее к дистрофии миокарда и недостаточной сократительной функций сердца.
Клинические проявления многообразны и не являются специфичными, причем начальная стадия заболевания может протекать вовсе без симптомов, но со временем при отсутствии должного лечения развивается тяжелая сердечная недостаточность.
Воспалительная кардиомиопатия
Заболевание представляет собой сочетание миокардита и дисфункции миокарда. Пациенты жалуются на боль в груди, нередко иррадиирующую в левую руку, приступы учащенного сердцебиения, одышку при физической нагрузке, а затем и в покое, периферические отеки, быструю утомляемость.
Диагностика кардиомиопатии
Диагностика кардиомиопатии строится на сборе анамнеза и лабораторных и инструментальных обследованиях больного. Основной диагностический критерий кардиомиопатии - наличие дисфункции миокарда, выявляемой при ультразвуковом обследовании сердца.
Исследование, позволяющее оценить функциональные и органические изменения сердца, его сократимость, а также состояние клапанного аппарата.
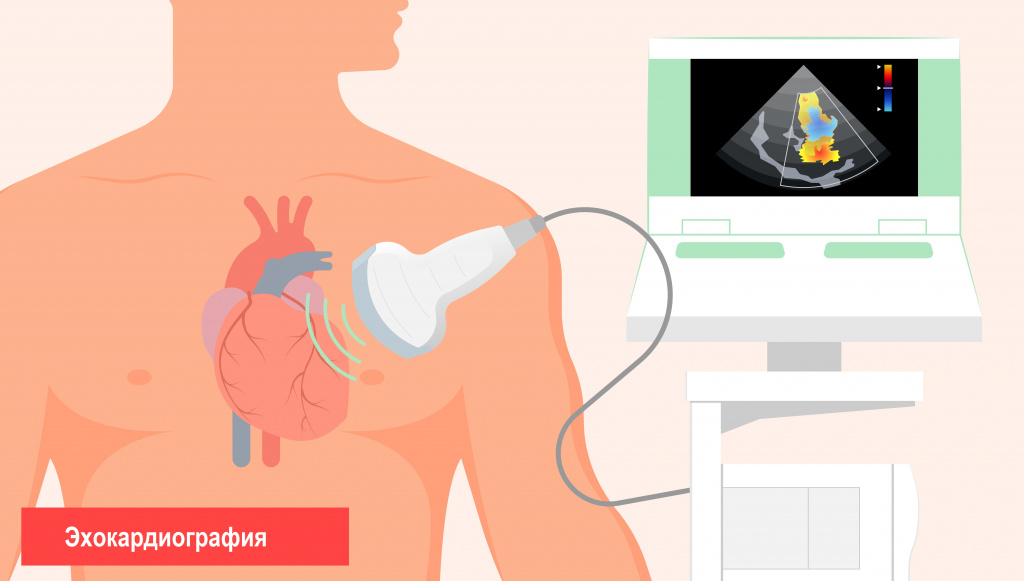
Кроме того, назначают следующие исследования:
-
Общий анализ крови.
Клинический анализ крови – одно из основных лабораторных исследований для количественной и качественной оценки всех классов форменных элементов крови. Включает цитологическое исследование мазка крови с подсчетом процентного содержания разновидностей лейкоцитов (определение общего количества лейкоцитов и процентного соотношения основных субпопуляций лейкоцитов: нейтрофилов, лимфоцитов, моноцитов, эозинофилов и базофилов) и определение скорости оседания эритроцитов.
Еще недавно метаболическим синдромом страдали преимущественно пожилые люди (старше 60 лет). Картина существенно изменилась за последние 20 лет. Динамика показала, что эта проблема молодеет и становится актуальной для более юного населения. В ряде стран доля взрослого населения, страдающая от этих симптомов, достигает 25%.
Метаболический синдром затрагивает как развитые страны (где высокотехнологичное производство избавило население от необходимости много двигаться), так и развивающиеся (большому проценту населения которых приходится экономить на продуктах питания и потреблять больше быстрых углеводов – макарон, хлеба, картофеля, кукурузы).
Есть и другая тенденция последних лет. От метаболического синдрома стали страдать женщины репродуктивного возраста. С чем это связано, до конца неясно. Предположительно, могут негативно влиять оральные контрацептивы.
Только представьте: за последние 20 лет число людей с метаболическим синдромом в мире выросло более чем на 100 млн – то есть на треть.
Особенно остро стоит проблема детского ожирения, а с ним и детского МС. Ученые связывают рост детского ожирения с частым отказом от грудного вскармливания. Грудное вскармливание исключает раннее введение прикорма, которое может привести к нездоровому увеличению веса. Потребление белка и общего количества энергии выше у детей, вскармливаемых смесями, что приводит к увеличению массы тела у младенцев. Также кормление смесью несколько увеличивает уровень инсулина, что в свою очередь способствует отложению жира и раннему развитию жировых клеток (адипоцитов).
В чем причины?
Главная причина, по которой развивается метаболический синдром, - внешние факторы: неправильное питание, малая подвижность. Эти вредные привычки в конечном счете нарушают нормальное функционирование жировой ткани и ведут к инсулинорезистентности.
Метаболический синдром имеет наследственную предрасположенность, которая, однако, в большей степени тоже объясняется внешними факторами. Люди, выросшие в одной семье, с большей вероятностью будут иметь схожие пищевые привычки и одинаковое отношение к спорту. Если на родительском столе бывает огромное количество быстрых углеводов и жиров и мало – овощей, зелени и фруктов, у ребенка с детства закладываются нездоровые отношения с едой. Так же и со спортом: ребенок с большей вероятностью будет активным, если у него активные родители.
Факторы риска
Осложнения
Диагностика метаболического синдрома
Диагностика МС состоит из визуального осмотра у врача и лабораторных и инструментальных исследований. В первую очередь врач оценивает абдоминальное ожирение. Но одного лишнего веса для постановки диагноза недостаточно. Оцениваются и другие симптомы и результаты анализов. Также важно обнаружить причину ожирения. Лишний вес может быть следствием эндокринных нарушений, гормональных сбоев или иных патологий.
Другой важный критерий при постановке диагноза – артериальное давление. При метаболическом синдроме оно обычно повышено.
ЭКГ – требуется, чтобы проверить работу сердца и вовремя обнаружить патологии, если заболевание уже запущенно.
Ангиография. Сложное исследование, которое позволяет оценить состояние сосудов. Проводится только по назначению врача.
Диагностика метаболического синдрома – непростая комплексная задача, которая осложняется разнообразием форм заболевания, его причинами и способами коррекции. Также это состояние опасно тем, что долгие годы человек не ощущает себя больным. Самочувствие начинает страдать, когда появляются значительные отклонения в работе организма и развиваются осложнения. Ни один человек не может ощутить повышенный уровень глюкозы в крови или нарушение обмена холестерина. О себе дают знать только уже очень серьезные проблемы, вызванные этими нарушениями, – например, гнойное воспаление пальцев ног или сердечный приступ.
Международная классификация болезней не выделяет метаболический синдром как отдельное заболевание, это целый комплекс заболеваний.
Ни один диагноз нельзя поставить самостоятельно, но любое отклонение в результатах исследований – повод не откладывать поход к врачу.
Лечение
В более запущенных формах может потребоваться применение препаратов, снижающих инсулинорезистентность, и лечащих артериальную гипертонию.
Миокардит — совокупность морфологических изменений тканей сердечной мышцы воспалительного характера. Протекает болезнь в острой и хронической форме и является чаще следствием инфекционных заболеваний, реже — неинфекционных. Отличается значительной вариабельностью клинических проявлений, выраженность которых во многом зависит от степени поражения миокарда, локализации патологического очага, особенностей протекания воспалительного процесса.
Общие сведения
Миокардит сердца развивается в разном возрасте (но чаще в 30-40 лет). Часто протекает под видом инфекционного процесса, которым был вызван, поэтому может оставаться незамеченным длительное время. В дальнейшем возможны рецидивы заболевания, развитие тяжелой острой симптоматики и серьезных осложнений.
Воспаление миокарда сопровождается повреждением кардиомиоцитов, в результате воздействия инфекционного или другого кардиотоксического агента. Помимо этого в воспалительный процесс могут быть вовлечены клетки соединительнотканной структуры, проводящей системы и пр.
Причины миокардита
Классификация миокардитов
По нозологической принадлежности миокардиты классифицируется на:
Симптомы миокардита
Степень поражения сердечной мышцы, локализация воспалительного очага, наличие распространения на перикард — во многом определяют клиническую картину. Симптомы миокардита заключаются в недостаточной сократительной способности сердечной мышцы и нарушениях ритма сердца.
Миокардит сердца может иметь слабовыраженные симптомы, протекать скрыто или остро. Чаще пациенты жалуются на боли в сердце, ощущение нехватки воздуха, повышенную потливость, быструю утомляемость. Внешние признаки: бледность эпидермиса с синим оттенком, увеличение вен шеи, отечность.
В результате обследования выявляется артериальная гипотония, увеличение сердца, нарушение пульса, кровоснабжения органов, внутрисердечной проводимости, аритмия, систолический шум на верхушке сердца, приглушенность I тона.
Осложнения миокардита
Следствием воспаления становится разрастание соединительной ткани, развитие кардиосклероза. При тяжелой форме развивается сердечная недостаточность (ухудшается доставка крови к тканям). Возможно развитие тромбоэмболии, приводящей к инсульту, инфаркту. Патология может стать причиной внезапного летального исхода.
Диагностика миокардита
Симптоматика неспецифична, что усложняет постановку диагноза. Врачи собирают анамнез, а также изучают данные лабораторных и инструментальных исследований.
Для постановки диагноза могут понадобиться данные следующих показателей/анализов:
Лечение миокардита
Терапия зависит от первопричины и стадии болезни. При легкой форме рекомендуется снижение двигательной активности, коррекция рациона (ограничение соли, воды, увеличение потребления витаминизированных, белковых продуктов).
В более тяжелых состояниях необходим постельный режим. Фармакотерапия может включать:
Лечение миокардита также может включать установку кардиостимулятора, трансплантацию сердца.
Прогноз при миокардите
При латентном и малосимптомном протекании патологии возможно самоизлечение. Если клиническая картина выражена, прогноз ухудшается: выздоровление наблюдается в половине случаев, в остальных — развивается дилатационная кардиомиопатия. Сердечная аритмия может спровоцировать летальный исход. В клинической практике имеются случаи тяжелого протекания патологии с быстрым прогрессированием сердечной недостаточности и внезапной смертью.
Профилактика миокардита
Специфической профилактики не существует. Но рекомендуется соблюдать ряд мер, которые помогут предупредить развитие патологии: своевременно и полностью лечить инфекционные заболевания, избегать укусов клещей, соблюдать правила личной гигиены, не пропускать плановую вакцинацию, вести ЗОЖ, периодически проходить профилактическое обследование у кардиолога.

1. Caforio A.L.P., Pankuweit S., Arbustini E., Basso C., Gimeno-Blanes J., Felix S.B., Fu M., Helio T., Heymans S., Jahns R., Klingel K., Linhart A., Maisch B., Kenna W.Mc., Mogensen J., Pinto Y. M., Ristic A., Schultheiss H-P., Seggewiss H., Tavazzi L., Thiene G., Yilmaz A., Charron P., Elliott P.M. Current state of knowledge on aetiology, diagnosis, management, and therapy of myocarditis: a position statement of the European Society of cardiology Working Group on Myocardial and Pericardial Diseases. European Heart Journal. 2013. Vol. 34. P. 2636–2648.
2. Gaaloul I., Riabiet S., Harrath R., Evans M., Salem H. N., Mlayeh S., Huber S., Aouni M. Sudden unexpected death related to enterovirus myocarditis: histopathology, immunohistochemistry and molecular pathology diagnosis at post-mortem. BMC Infectious Diseases. 2012. V. 12. P. 212.
3. Палеев Н.Р., Палеев Ф.Н., Санина Н.П., Макарков А.И., Москалец О.В., Островский Е.И., Хишова Н.Н. Сердечная недостаточность при миокардитах и роль иммунных механизмов в ее развитии // Русский медицинский журнал 2014. № (12). C. 878–882.
4. Kindermann I., Barth C., Mahfoud F., Ukena C., Lenski M., Yilmaz A., Klingel K., Kandolf R., Sechtem U., Cooper L.T., Bohm M. Update on myocarditis. J. Am. Coll. Cardiol. 2012. no.59. P. 779-792.
5. Lakdawala N.K., Funke B. H., Baxter S., Cirino A. L., Roberts A. E., Judge D. P., Johnson N., Mendelsohn N.J, Morel C., Care M., Chung W.K., Jones C., Psychogios A., Duffy E, Rehm H.L., White E., Seidman J.G., Seidman C.E., Ho C.Y. Genetic testing for dilated cardiomyopathy in clinical practice. Journal of Cardiac Failure. 2012. no.18 (4). P. 296-303.
6. Felker G.M., Thompson R.E., Hare J.M., Hruban R.H., Clemetson D.E., Howard D.L., Baughman K.L., Kasper E.K. Underlying causes and long-term survival in patients with initially unexplained cardiomyopathy. N. Engl. J. Med. 2000. no.342. P. 1077-1084.
7. Friedrich M.G., Sechtem U., Schulz-Manager J., Holmvang G., Alakija P., Cooper L. T., White J. A., Abdel-Aty H., Gutberlet M., Prasad S., Aletras A., Laissy J-P., Paterson I., Filipchuk N.G., Kumar A., Pauschinger M., Liu P. Cardiovascular Magnetic Resonance in Myocarditis: A JACC White Paper. 2009. no.53(17). P. 1475-1487.
8. Seif E., Chen L., Goldman B. Fulminant Myocarditis: A review of the current literature. US Cardiology Review. 2018. no.12(1). P. 13-6.
9. Скворцов В.В., Тумаренко А.В., Одинцов В.В., Орлов О.В., Скворцова Е.М. Миокардиты // Российский кардиологический журнал. 2009. №1 (75). С. 87-96.
10. Lurz P., Eitel I., Adam J., Steiner J., Grothoff M., Desch S., Fuernau G., de Waha S., Sareban M., Luecke C., Klingel K., Kandolf R., Schuler G., Gutberlet M., Thiele H. Diagnostic Performance of CMR Imaging Compared With EMB in Patients With Suspected Myocarditis. JACC: Cardiovascular Imaging. 2012. no.5 (5). P. 513-524.
11. Unterberg-Buchwald C., Ritter C.O., Reupke V., Wilke R.N., Stadelmann C., Steinmetz M., Schuster A., Hasenfuß G., Lotz J., Uecker M. Targeted endomyocardial biopsy guided by real-time cardiovascular magnetic resonance Journal of Cardiovascular Magnetic Resonance. 2017. no.19(1). P. 45.
Процессы воспаления в кардиомиоцитах можно выявить при различных повреждениях сердца, включая ишемические нарушения, механическую травму или генетические кардиомиопатии. В то же время остается неизменным тот факт, что для классического варианта миокардита характерно воспаление в результате воздействия бактерий, паразитов, вирусов или реже лекарственных препаратов либо вследствие запуска аутоиммунных реакций [1].
Чрезвычайно трудно установить и уровень распространенности данной патологии в связи с тем, что на практике используются разные критерии включения, сложности выявления бессимптомных и малосимптомных случаев и сохраняется высокий дефицит всех необходимых диагностических методов. На основании исследований ряда авторов заболеваемость миокардитами составляет от 8 до 10 случаев на 100 тыс. населения [1].
Цель исследования – выделить особенности развития данного заболевания и обсудить возможности своевременной постановки правильного диагноза.
Пациент С., 33 лет, 25.08.2016 г. бригадой скорой медицинской помощи был доставлен в стационар и госпитализирован в хирургическое отделение с жалобами на боли в эпигастральной области опоясывающего характера, тошноту, ощущение распирания в брюшной полости, чувство нехватки воздуха, затрудненное дыхание, повышение температуры тела до 37,5оC, сухость во рту, общую слабость.
Из анамнеза заболевания: больным себя считает с 15.07.2016 г., когда после переохлаждения стали беспокоить сухой, в дальнейшем влажный кашель с мокротой, повышение температуры до 38°С. 18.07.2016 г. обследовался в поликлинике по месту жительства у терапевта. В результате назначена и выполнена рентгенография органов грудной клетки, проведено обследование показателей периферической крови. Выявленные изменения были расценены как обострение хронического бронхита. Получал лечение: несколько курсов антибактериальных препаратов в связи с недостаточным противовоспалительным эффектом предыдущего курса (антибиотикотерапия – ципролет по 500 мг 7 дней, левофлоксацин 500 мг в сутки – 5 дней, в дальнейшем в/м цефтриаксон по 1000 мг 2 раза в день 3 дня), десенсибилизирующую и отхаркивающую терапию. В результате 10.08.2016 г. интенсивность кашля уменьшилась, но сохранялось повышение температуры в вечерние часы до 37,5°С, присоединились одышка при физической нагрузке, приступы затрудненного дыхания в ночные часы и общая слабость. С 20.08.2016 г. по 25.08.2016 г. появились жалобы на боли в эпигастральной области опоясывающего характера, ощущение распирания в брюшной полости, тошноту и сухость во рту.
На момент поступления: общее состояние удовлетворительное. Температура тела составляла 37,5оС. Кожные покровы бледные, цианоз губ. В легких дыхание везикулярное, выслушиваются единичные рассеянные сухие хрипы. Частота дыхания (ЧД) 20 в минуту в покое. Артериальное давление (АД) 140/ 90 мм рт. ст. Частота сердечных сокращений (ЧСС) 98 ударов в минуту. Живот симметричный, умеренно вздут, участвует в акте дыхания. При пальпации болезненный в верхних отделах живота, преимущественно в области эпигастрия. Перитонеальные симптомы отрицательные. В общем анализе крови (ОАК) от 25.08.2016 г.: Умеренный лейкоцитоз (лейкоциты 11,3×10*9/л), скорость оседания эритроцитов (СОЭ) 5 мм/ч. Общий анализ мочи (ОАМ) – без патологии. На ЭКГ от 25.08.2016 г.: Cинусовый ритм с частотой сердечных сокращений 102 в минуту. Электрическая ось сердца горизонтальная. Переходная зона в V4. В отведениях V3–V6 глубокие асимметричные (–) зубцы Т, дисметаболические изменения миокарда. При проведении ультразвукового исследования (УЗИ) органов брюшной полости от 25.08.2016 г.: Признаки умеренной гепатомегалии, диффузных изменений паренхимы печени, утолщение стенок желчного пузыря (отек), диффузных изменений поджелудочной железы по типу хронического панкреатита, в стадии обострения. Свободной жидкости в брюшной и плевральной полости не выявлено. Эзофагогастродуоденоскопия (ЭГДС) от 25.08.2016 г.: Поверхностный гастродуоденит. Дуодено-гастральный рефлюкс. На рентгенограмме органов грудной клетки от 25.08.2016 г. выявлено расширение всех границ сердца. В результате осмотра терапевта выставлен диагноз: Кардиомиопатия идиопатическая? Хроническая сердечная недостаточность (ХСН) 0 стадия. Хронический панкреатит, стадия обострения.
В период нахождения в стационаре получал инфузионную терапию (раствор Рингера 250 мл 1 раз в день в/в капельно, ежедневно цефтриаксон 1,0 г с раствором натрия хлорида 200 мл 1 раз в день в/в капельно, а также в/м анальгин, платифиллин) и таблетированные формы препаратов (антациды, ферменты и блокаторы протонной помпы). На фоне активной инфузионной терапии, которая проводилась с 25.08.2016 г. по 27.08.2016 г., самочувствие пациента ежедневно ухудшалось (нарастала одышка, появились удушье в горизонтальном положении, отеки на нижних конечностях), в связи с чем он самостоятельно покинул хирургическое отделение стационара.
02.09.2016 г. самостоятельно обратился к кардиологу в поликлинику по месту жительства. Предъявлял жалобы на одышку при незначительной физической нагрузке и в покое, чувство нехватки воздуха и удушье в горизонтальном положении, колющие и давящие боли в области сердца и сердцебиение при минимальной физической нагрузке, увеличение живота в объеме и отеки на нижних конечностях, головные боли, выраженную общую слабость. При более подробном сборе анамнеза заболевания было выявлено: артериальное давление повышается в течение 7 лет Максимальные цифры 175/130 мм рт. ст., адаптирован к цифрам АД 140–150/110 мм рт. ст. (более низкие цифры АД не регистрировал). Гипотензивные препараты регулярно не принимает, только периодически использует капотен. В течение последних 2 лет беспокоят колющие боли в области сердца и редкие приступы сердцебиения при значительной физической нагрузке, купирующиеся самостоятельно. Со слов пациента, ухудшение состояния возникло остро в течение последних двух недель. Обращает на себя внимание появление и прогрессирование в течение последней недели следующих симптомов: отеки нижних конечностей и увеличение живота в объеме. Из анамнеза жизни было выяснено, что пациент работает автомаляром (стаж около 10 лет, ежедневно контактирует с токсичными лакокрасочными и смазочными материалами, токсическими аэрозолями). Имеет вредные привычки: курит 0,5 пачки в день в течение 8 лет, алкогольные напитки употребляет редко, применение наркотических и запрещенных тонизирующих средств отрицает. Семейный анамнез ранних сердечно-сосудистых заболеваний не отягощен. Из перенесенных заболеваний: желтуха в детском возрасте, хронический обструктивный бронхит, хронический панкреатит и хронический холецистит. Общее состояние расценено как средней тяжести. Индекс массы тела (ИМТ) – 29. Цианоз губ. Акроцианоз. При переходе в горизонтальное положение – цианоз лица, ушей. Выраженные отеки голеней и стоп. В легких дыхание с жестким оттенком, в нижних отделах выслушиваются единичные влажные мелкопузырчатые хрипы. ЧД 20 в минуту (в покое). Границы относительной сердечной тупости смещены: правая на 1,0 см от правого края грудины, левая на 2,5 см кнаружи от левой срединно-ключичной линии по 5-му межреберью. Тоны сердца приглушены, систолический шум на верхушке, в 3-й точке аускультации – легочной артерии и в 4-й точке аускультации – проекции трикуспидального клапана. Ритм сердца правильный, ЧСС 95 в минуту, АД 168/109 мм рт. ст., пульс 95 в минуту. Живот увеличен в объеме за счет асцита, при пальпации безболезненный. Печень выступает на 2 см из-под края правой реберной дуги.
По рекомендации кардиолога 28.08.2016 г. выполнена ЭХО-КС, где впервые выявлены дилатация камер сердца (левое предсердие (ЛП) 4,3 см, левый желудочек (ЛЖ): конечный диастолический размер (КДР) 6,4 см, конечный систолический размер (КСР) 5,5 см; правый желудочек (ПЖ) 3,8 см, правое предсердие (ПП) 5,7×4,6 см), выраженное снижение фракции выброса (ФВ 26%), диффузный гипокинез стенок, признаки недостаточности относительного генеза митрального клапана (митральная регургитация (МР) II степени), трикуспидальная регургитация (ТР) II степени, легочная регургитация (ЛР) I–II степени, умеренная легочная гипертензия с систолическим давлением в легочной артерии (СДЛА) 52 мм рт. ст. (рис. 1). По мнению врача ультразвуковой диагностики, все указывало на признаки дилатационной кардиомиопатии, что и было указано в заключении.
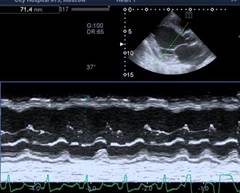
а)
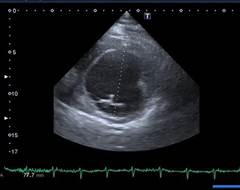
б)
Рис. 1. Эхокардиоскопия. а) М – модальный режим по длинной оси – КДР левого желудочка 6,4 cм,
б) Двухмерный режим по короткой оси – КСР левого желудочка
С 22.09.2016 г. по 3.10.2016 г. пациент проходил стационарное лечение в кардиологическом отделении. Учитывая ежедневный амбулаторный прием вышеперечисленных лекарственных препаратов, отмечал уменьшение одышки и отеков на нижних конечностях, живота в объеме, сохранялись редкие приступы колющих болей в области сердца только при физической нагрузке.
На ЭКГ от 22.09.2016 г. Ритм синусовый. ЧСС 69 ударов в минуту. Горизонтальное положение ЭОС. Гипертрофия миокарда левого желудочка с систолической перегрузкой. ЭХО-КС от 23.09.2016 г. Заключение: Дилатация всех камер сердца. Диффузный гипокинез. Снижение глобальной сократимости ЛЖ (УО 64 мл, ФВ 30%). Диастолическая дисфункция ЛЖ. Незначительная регургитация на МК, ТК, ЛК. Умеренная легочная гипертензия. Проведение офтальмоскопии, полного биохимического анализа крови, общего анализа мочи не выявило патологических изменений. И только в общем анализе крови от 22.09.2016 г. сохранялся лейкоцитоз до 10,4*109/л. При выписке было рекомендовано: ЭХО-КС в динамике, консультация ангиохирурга и кардиохирурга после проведения спиральной томограммы сердца. Продолжить прием лекарственных препаратов: Триметазидин 35 мг 2 раза в сутки (утром и вечером на 2 месяца), Верошпирон 25 мг утром или Эспиро 25 мг утром, Торасемид 10 мг утром, Дигоксин 0,00025 мг – по 1/2 таблетки утром 5 дней в неделю, Престанс (10 мг/5 мг) 1 таблетку утром и дополнительно Таурин 500 мг 2 раза в сутки в течение 3 месяцев.
11.12.2016 г. при оценке ограничений жизнедеятельности в учреждении медико-социальной экспертизы (МСЭ) пациенту установлена II группа инвалидности.
Учитывая длительный период наблюдения за пациентом и использование большого количества диагностических методов, для лучшего понимания положительной динамики по данным ЭХО-КС исследований более значимые показатели представлены в виде диаграмм на рисунках 2, 3 и 4.

Рис. 2. Изменение систолической функции (показателей ФВ) левого желудочка по данным ЭХО-КС с 08.2016 по 03.2017 г.

Рис. 3. Динамика размеров камер сердца по данным ЭХО-КС с 08.2016 по 03.2017 г.

Рис. 4. Динамика изменений систолического давления в легочной артерии по данным ЭХО-КС с 08.2016 по 03.2017 г.
И только в январе 2017 г. появилась возможность выполнения магнитно-резонансной томографии (МРТ) до и после введения контрастного препарата (рис. 5). При интерпретации результатов оценивались особенности накопления контрастного препарата поврежденным миокардом, локализация и масштаб изменений.

Рис. 5. Магнитно-резонансная томография сердца. Срез желудочков сердца по короткой оси (двухкамерная позиция) – восстановление через 15–20 мин после введения контрастного препарата. Мелкоочаговые включения контраста (указаны стрелкой) в толщу межжелудочковой перегородки (МЖП)
Визуализируются неяркие и без четких контуров мелкие расположенные по цепочке интрамуральные очаги на протяжении трех сегментов. Для выделения достоверно поврежденного участка миокарда использовали общепринятую схему сегментарного строения миокарда левого желудочка.
В связи с хорошим гемодинамическим приростом и отсутствием потребности в подборе более специфической терапии был снят вопрос о проведении эндомиокардиальной биопсии.
В октябре 2017 г. при повторном освидетельствовании в учреждении МСЭ инвалидность присвоена не была.
В настоящее время пациент предъявляет жалобы на редкие эпизоды головных болей в период подъемов АД (максимально до 150/80 мм рт. ст.), при объективном осмотре и по результатам дополнительных диагностических методов не имеет признаков сердечной недостаточности, а из лекарственных препаратов принимает нерегулярно Престанс (10 мг/5 мг) по 1 таблетке утром.
И только через один год, анализируя всю картину заболевания, где четко прослеживается уменьшение клинических проявлений гемодинамических нарушений на фоне значительного и достаточно эффективного увеличения систолической функции ЛЖ (ФВ до 56%), положительной составляющей в изменении полостей сердца, можно подчеркнуть, что при истинной (генетически обусловленной) ДКМП, в основе которой лежит необратимый прогрессирующий фиброз миокарда, подобных положительных моментов не отмечается. В результате изложенного можно сделать вывод о том, что в 2016 г. пациент перенес острый миокардит.
Поражает, насколько долго растягивается диагностический путь пациента и составляет порой от нескольких недель до нескольких месяцев и более, что также подтверждается многими исследованиями [9].
Связь клинических симптомов с предшествующими эпизодами респираторных, вирусных и бактериальных инфекций, эпизодами неясной лихорадки, контактом с токсичными веществами четко прослеживается только при подробном сборе анамнеза заболевания и уточнении особенностей профессиональной деятельности. Кроме того, многие медикаментозные препараты являются кардиотоксичными, поэтому следует уделять самое пристальное внимание расспросу обо всех принимаемых лекарственных и нелекарственных средствах, дозах, а также длительности приема.
Обязательно в диагностический поиск необходимо включать максимум дополнительных методов обследования, уделяя их динамике также особое внимание [10]. В данном примере сочетаются: яркая клиническая картина тяжелых проявлений сердечной недостаточности и скудная лабораторная панель положительных результатов – критериев воспалительного характера в процессе повреждения миокарда, так как был получен умеренный лейкоцитоз и повышение С-реактивного белка, хотя это сохранялось на протяжении нескольких месяцев.
В связи с возможностью перехода перенесенного острого миокардита в хроническую форму и постоянным присутствием угрозы возникновения отдаленных осложнений у данного пациента в дальнейшем требуется регулярный длительный контроль за гемодинамическими показателями по данным ЭХО-КС (систолической функцией ЛЖ и размерами полостей сердца) и состоянием проводящей системы сердца при выполнении ЭКГ.
В подобных клинических ситуациях (при длительном сохранении признаков СН) не стоит придерживаться классических правил, требующих в кратчайшие сроки постановки клинического диагноза, а следует в полном объеме продолжить реализацию всех лабораторных и инструментальных методов обследования дифференциально-диагностического ряда.
Читайте также:

