Как часто должны осуществлять во время анестезии контроль герметичности дыхательного контура при ивл
Обновлено: 30.06.2024
Проблема поражения легких при вирусной инфекции, вызванной COVID-19 является вызовом для всего медицинского сообщества, и особенно для врачей анестезиологов-реаниматологов. Связано это с тем, что больные, нуждающиеся в реанимационной помощи, по поводу развивающейся дыхательной недостаточности обладают целым рядом специфических особенностей. Больные, поступающие в ОРИТ с тяжелой дыхательной недостаточностью, как правило, старше 65 лет, страдают сопутствующей соматической патологией (диабет, ишемическая болезнь сердца, цереброваскулярная болезнь, неврологическая патология, гипертоническая болезнь, онкологические заболевания, гематологические заболевания, хронические вирусные заболевания, нарушения в системе свертывания крови). Все эти факторы говорят о том, что больные поступающие в отделение реанимации по показаниям относятся к категории тяжелых или крайне тяжелых пациентов. Фактически такие пациенты имеют ОРДС от легкой степени тяжести до тяжелой.
У больных с дыхательной недостаточностью принято использовать респираторную терапию. В настоящее время существует множество вариантов респираторной терапии: ингаляция кислорода (низкопоточная – до 15 л/мин, высокопоточная – до 60 л/мин), искусственная вентиляция легких (неинвазивная - НИМВЛ или инвазивная ИВЛ, высокочастотная вентиляция легких).
Общемировая практика свидетельствует о крайне большом проценте летальных исходов связанных с вирусной инфекцией вызванной COVID-19 при использовании инвазивной ИВЛ (до 85-90%). На наш взгляд данный факт связан не с самим методом искусственной вентиляции легких, а с крайне тяжелым состоянием пациентов и особенностями течения заболевания COVID-19.
Тяжесть пациентов, которым проводится инвазивная ИВЛ обусловлена большим объемом поражения легочной ткани (как правило более 75%), а также возникающей суперинфекцией при проведении длительной искусственной вентиляции.
Собственный опыт показывает, что процесс репарации легочной ткани при COVID происходит к 10-14 дню заболевания. С этим связана необходимость длительной искусственной вентиляции легких. В анестезиологии-реаниматологии одним из критериев перевода на спонтанное дыхание и экстубации служит стойкое сохранение индекса оксигенации более 200 мм рт. ст. при условии, что используются невысокие значения ПДКВ (не более 5-6 см. вод. ст.), низкие значения поддерживающего инспираторного давления (не более 15 см. вод. ст.), сохраняются стабильные показатели податливости легочной ткани (статический комплайнс более 50 мл/мбар), имеется достаточное инспираторное усилие пациента ( p 0.1 более 2.)
Достижение адекватных параметров газообмена, легочной механики и адекватного спонтанного дыхания является сложной задачей, при условии ограниченной дыхательной поверхности легких.
В условиях субтотального или тотального поражения дыхательной поверхности легких процент успеха терапии дыхательной недостаточности является крайне низким.
Собственный опыт показывает, что выживаемость пациентов на инвазивной ИВЛ составляет 15.3 % на текущий момент времени.
Алгоритм безопасности и успешности ИВЛ включает:
- Последовательное использование методов респираторной терапии.
- Обработка рук персонала перед и после манипуляций с пациентом.
- Смена бактериальных фильтров каждые 12 часов.
- Использование закрытых систем для санации трахеобронхиального дерева и адекватная регулярная санация трахеобронхиального дерева.
- Профилактика нарушений герметичности дыхательного контура.
- Использование систем согревания и увлажнения дыхательной смеси.
- Использование протективных параметров искусственной вентиляции легких.
- Регулярное использование прон-позиции и смены положения тела.
- Адекватный уход за полостью рта и регулярное измерение давления в манжете эндотрахеальной или трахеостомической трубки.
- Адекватный подбор схем антибактериальной терапии с учетом чувствительности возбудителя.
- Рестриктивная стратегия инфузионной терапии (ЦВД не более 9 мм рт. ст)
- Своевременное применение экстракорпоральных методов очищения крови.
- Регулярный лабораторный мониторинг параметров газообмена (КЩС артериальной крови) – не менее 4 р/сут.
- Регулярный контроль параметров ИВЛ и регулярная оценка параметров легочной механики.
- Хорошая переносимость пациентом ИВЛ (седация, миорелаксация, подбор параметров и чувствительности триггера, при условии, что больной в сознании и имеет собственные дыхательные попытки)
В связи с тем, что процент выживаемости пациентов при использовании инвазивной ИВЛ остается крайне низким возрастает интерес к использованию неинвазивной искусственной вентиляции легких. Неинвазивную ИВЛ по современным представлениям целесообразно использовать при ОРДС легкой степени тяжести. В условиях пандемии и дефицита реанимационных коек процент пациентов с тяжелой формой ОРДС преобладает над легкой формой.
Тем не менее, в нашей клинической практике у 23% пациентов ОРИТ в качестве стартовой терапии ДН и ОРДС применялась неинвазивная масочная вентиляция (НИМВЛ). К применению НИМВЛ есть ряд ограничений: больной должен быть в ясном сознании, должен сотрудничать с персоналом. Допустимо использовать легкую седацию с целью обеспечения максимального комфорта пациента.
Критериями неэффективности НИМВЛ являются сохранение индекса оксигенации ниже 100 мм рт.ст., отсутствие герметичности дыхательного контура, возбуждение и дезориентация пациента, невозможность синхронизации пациента с респиратором, травмы головы и шеи, отсутствие сознания, отсутствие собственного дыхания. ЧДД более 35/мин.
В нашей практике успешность НИМВЛ составила 11.1 %. Зав. ОАИР: к.м.н. Груздев К.А.
Безопасность пациента зависит от многих факторов: от его состояния и уровня профессиональной подготовки оказывающего ему помощь, используемых технических средств, уровня оснащенности рабочего места. Значимость этих факторов различна, человеческий фактор и мониторинг в обеспечении безопасности пациента при оказании анестезиологической и реаниматологической помощи являются основными.
Мониторинг следует проводить с целью контроля: 1) состояния больного (электрокардиография, пульсоксиметрия, капнография и др.); 2) лечебных действий (контроль нейромышечного блока, ЭЭГ); 3) окружающей среды (газового состава вдыхаемой смеси); 4) работы технических средств (аппарата ИВЛ и пр.). Мониторинг пациента – это контроль функций и процессов с целью выявления опасных их отклонений.
Мониторинг состояния пациента по степени сложности может включать в себя: 1) непрерывный контроль параметров; 2) непрерывный контроль с сигнализацией при выходе параметра за установленные пределы; 3) то же, что в п.2 + подсказка решения; 4) то же, что в п. 3 + проведение мер по нормализации функции.
Показания для мониторинга:
минимального - обязателен всегда при анестезии и интенсивной терапии;
углубленного (с использованием неинвазивных и инвазивных методов) - при значительных нарушениях функций организма, особенно при развитии у больного полиорганной недостаточности, в специализированных разделах медицины (кардиохиргия, неврология и пр.);
профилактического - при риске развития критического состояния (у больных с инфарктом миокарда).
Мониторинг может быть инвазивным и неинвазивным. Предпочтение отдают неинвазивному мониторингу, при котором отсутствует внедрение в организм электродов, катетеров и других средств через кожу, сосуды, желудочно-кишечный тракт и дыхательные пути. Однако в случае необходимости (прежде всего при операциях на сердце, крупных сосудах, в трансплантологии и пр.) используют инвазивные методы.
Мониторинг позволяет осуществлять: 1) своевременную диагностику нарушений и профилактику тяжелых осложнений, в том числе остановки сердца и дыхания; 2) более правильную тактику интенсивной терапии, что повышает эффективность лечения.
Стандарт минимального мониторига во время анестезии
Нахождение анестезиолога-реаниматолога и медицинской сестры-анестезиста рядом с больным
Измерение АД и частоты сердечных сокращений
Через каждые 5 мин
Мониторинг оксигенации, вентиляции и кровообращения (клиническая картина, пульсоксиметрия, капнография, волюмоспирометрия и пр.)
Контроль герметичности дыхательного контура при ИВЛ
Контроль концентрации кислорода в дыхательной смеси
Измерение температуры тела
Стандарт минимального мониторинга при проведении реанимации и интенсивной терапии
Нахождение анестезиолога-реаниматолога или медицинской сестры-анестезиста на посту
Измерение АД, частоты сердечных сокращений и частоты дыхания
Не реже 1 раза в час
Мониторинг вентиляции и кровообращения (клиническая картина, пульсоксиметрия, капнография, волюмоспирометрия и пр.)
Контроль герметичности дыхательного контура при ИВЛ
Контроль давления в дыхательном контуре при ИВЛ
Контроль концентрации кислорода в дыхательной смеси
Измерение температуры тела
Не реже 4 раз в сутки
Для обеспечения безопасности больного при интенсивной терапии нередко необходим расширенный мониторинг: контроль сердечно-сосудистой, дыхательной и нервной систем, функций печени, почек, желудочно-кишечного тракта, кроветворения, гемостаза, а также энергетического, водно-электролитного, кислотно-основного и онко-осмотического баланса. В равной степени имеет большое значение интенсивное наблюдение за проводимыми лечебными мероприятиями и их результатами. Немаловажную роль играет мониторинг наружного и внутреннего микробиологического статуса, а также применение прогностических критериев (например, APACHE III и др.) и оценка исходов.
Клинический мониторинг, т.е. наблюдение за клиническими признаками и симптоматикой, качественными данными, является не менее важным, чем количественные показатели, полученные с помощью сложной техники.
Мониторинг кровообращения предусматривает своевременную оценку функции сердца, тонуса сосудов, объема циркулирующей крови и в целом адекватности снабжения кровью жизненно-важных органов.
Аритмии сердца можно выявить с помощью ЭКГ по зубцу Р и комплексу ORS ЭКГ в IV и II стандартного биполярного отведения от конечностей или их модификаций. Микропроцессорные ЭКГ-мониторы могут автоматически регистрировать нарушения ритма, но нужна хорошая морфология зубца Р и комплекса ORS.
Об ишемии миокарда свидетельствует депрессия отрезка ST ЭКГ: 1) в отведении V5 или одной из ее модификаций - ишемия перегородки левой боковой стенки; 2) в биполярном отведении II от конечностей - ишемия нижней части миокарда в бассейне правой коронарной артерии. Косонисходящая депрессия ST (элевация) является индикатором ишемии под воздействием стресса. Горизонтальная депрессия имеет большее значение, чем его девиация.
Объем циркулирующей крови чаще всего определяют методом разведения красителя или по косвенным показателям (ЦВД в сочетании с объемными нагрузочными пробами - информация о степени наполнения сосудов).
Тонус сосудов оценивают на основании общего периферического сосудистого сопротивления (ОПСС), определяемого, например, методом интегральной реографии тела.
Контроль гемодинамики можно осуществлять путем: 1) измерения АД (неинвазивно или инвазивно); 2) длительной пальцевой плетизмографии; 3) измерения ЦВД в сочетании с объемными нагрузочными пробами; 4) определения давления в легочной артерии и давления заклинивания с помощью флотирующего катетера в легочной артерии (более точный метод для оценки внутрисосудистого объема, чем ЦВД, может также служить мерой преднагрузки левого желудочка); 5) оценки функции желудочков (SvO2 отражает тканевой баланс О2, а двухмерная чреспищеводная эхокардиография при анатомически правильном изображении позволяет определить размеры желудочков, используя автоматическую регистрацию, можно получить объем желудочков, фракцию выброса и др. показатели их работы); 6) определения сердечного выброса посредством термистера (термодилюционная методика), методом Фика (СВ= VO2 / (a-v)Co2), различными модификациями методики Доплера (пищеводная доплеровская эхокардиография); 7) определения показателей центральной гемодинамики (сердечного и ударного индекса, общего периферического сопротивления сосудов – ОПСС, объема клеточной и внеклеточной жидкости и др.), используя метод интегральной реографии тела по М. И. Тищенко и импедансометрию; 8) измерения индекса произведения частоты сердечных сокращений и АД систолического (ИПЧД = АДсист. * ЧСС; более 12000 - ишемия миокарда) и более точного показателя - соотношения среднего АД к частоте сердечных сокращений (ИСАДЧ= САД/ЧСС, САД= АДд * (АДс-АДд)/ЧСС; -1 ).
Мониторинг нейромышечной передачи осуществляют с помощью монитора типа TOF-GUARD или TOF-WATCH по показателям акцелерограммы: Tw1 (при однократной стимуляции, используемой при оценке блока деполяризующих миорелаксантов) и TOF (отношению величины четвертого ответа к первому на стимуляцию нерва, применяемой при недеполяризующих миорелаксантах). Диафрагма быстрее других периферических мышц восстанавливается после паралича. Вследствие этого даже полное исключение ответа на однократную и TOF-стимуляцию m. adductor pollicis не гарантирует от возможных движений диафрагмы, таких как икота, кашель. Поэтому для уверенности в параличе диафрагмы во время операции блокаду нужно поддерживать в такой степени, чтобы TOF в режиме РТС применительно к большому пальцу был равен нулю. При TOF=0,6 больной может поднять голову на 3 сек, но сила вдоха часто оказывается недостаточной; при TOF=0,7-0,75 больной может широко открыть глаза, удовлетворительно покашлять и поднять голову на 5 сек. При значениях TOF=0,8 и более жизненные возможности и сила вдоха в пределах нормы. Считают, что производить экстубацию и полностью переводить больного на спонтанное дыхание следует осуществлять, когда TOF составляет более 90%. Если экстубацию проводят при TOF 70%, частота легочных осложнений после операции существенно возрастает.
Вызванные потенциалы головного мозга представляют собой характерную для каждого вида стимула кривую, выделяемую с помощью компьютерной обработки из ЭЭГ в ответ на определенный стимул. В анестезиологии наибольшее применение нашли среднелатентные слуховые вызванные потенциалы (СЛСВП, middle latency auditory evoked potentials, MLAEP). Увеличение латентности и уменьшение амплитуды пиков СЛСВП происходит с увеличением концентрации анестетика и хорошо коррелирует со степенью седации пациента. Эти характерные изменения кривой ответа представляются в виде индексов AEPindex и AAI. В частности, AEPindex предсказывает движения больного в ответ на болевую стимуляцию. Это, возможно, связано с тем, что СЛСВП отражают активность не только коры головного мозга, но и подкорковых структур.
Мониторинг функции почек осуществляют чаще всего путем определения почасового диуреза. Диурез в пределах нормы (> 0,5 мл/кг ч., при отсутствии полиурического состояния, например, при сахарным и несахарным диабете, тубулярном некрозе), свидетельствует об адекватной почечной перфузии. Нормальная тубулярная функция почек подтверждается следующими показателями: 1) индекс почечной недостаточности 500 мосм/кг Н2О; 4) соотношение мочевина плазмы/креатинин - >100; 5) креатинин мочи/креатинин плазмы >40. Подъем креатинина плазмы запаздывает на 12-24 ч от клинического момента повреждения почек.
Выберите ОДИН правильный ответ
условия комфорта и безопасности, позволяющие эффективно удовлетворять все свои жизненно важные потребности пациенту и медицинскому работнику
улучшение качества медицинской помощи
комфортная палата для пациента
внимательное и вежливое обращение с пациентом
Выберите ОДИН правильный ответ
100-1000 раз
Выберите ОДИН правильный ответ
не позднее 30 минут после отсоединения от пациента
в конце рабочего дня
не позднее 3 часов после отсоединения от пациента
Выберите ОДИН правильный ответ
инфицирования медицинских работников в результате их профессиональной деятельности
инфекции, присоединившиеся к основному заболеванию у госпитализированных пациентов
инфекции, передающиеся половым путем
особо опасные инфекции
химическое загрязнение
травматизация
работа по графику
заболевания дыхательных путей
парентеральные вирусные гепатиты
неприятный запах из ротовой полости
локтевые дозаторы
дозаторы на фотоэлементах
Выберите ОДИН правильный ответ
использовании сосудистого катетера для введения лекарственных средств
внутривенном введении лекарственных средств
подкожном введении лекарственного препарата
переливании препаратов крови
цитотоксические лекарственные средства
моноклональные антитела
одевать маску, использовать защитный экран во время процедур
надевать перчатки при контакте с биологическими жидкостями и зараженными объектами
мыть руки после контакта с пациентом
надевать две пары перчаток
использование одноразовых дыхательных контуров
использование гидрофобных антибактериальных дыхательных фильтров-ТВО
применение антибиотиков широкого спектра действия
применение противопролежневого матраса
у входа в палату
у постели больного
комната отдыха медицинского персонала
повреждение липидов рогового слоя кожи
возможна контаминация одежды при разбрызгивании воды
повышение финансовых затрат
Выберите ОДИН правильный ответ
Выберите ОДИН правильный ответ
стерилизация инструментария, диагностической и лечебной аппаратуры
совершенствование методов обработки рук медицинского персонала
дезинфекция объектов внутрибольничной среды
применение антибиотиков широкого сектора действия
увеличение срока пребывания пациента в стационаре
положение пациента строго на спине
антибиотики
гормональные лекарственные средства
Выберите ОДИН правильный ответ
1 раз в три дня
при выявлении проблемы, связанной с катетером (боль, отёчность руки, промокание повязки)
при внутривенном введении лекарственного препарата или подсоединения инфузионной системы
Выберите ОДИН правильный ответ
подлежит дезинфекции и утилизации, как медицинские отходы класса Б
после высушивания, подлежит повторному использованию
его утилизируют как медицинские отходы класса А
Выберите ОДИН правильный ответ
подлежат дезинфекции и утилизации как медицинские отходы класса Б
после высушивания подлежат повторному использованию
утилизируют как медицинские отходы класса А
подлежат дезинфекции, ПСО и стерилизации согласно руководству по эксплуатации соответствующего аппарата
Выберите ОДИН правильный ответ
дезинфекция, предстерилизационная очистка, стерилизация
предстерилизационная очистка, стерилизация, дезинфекция
дезинфекция, стерилизация, предстерилизационная очистка
ополаскивание под проточной водой, дезинфекция
кончики пальцев
большой палец
межпальцевые промежутки
Выберите ОДИН правильный ответ
многократная обработка рук, с образованием трещин, сухостью кожи
чрезмерное ополаскивание рук водой
использование разнообразных антисептиков
увеличение сроков пребывания пациентов в ОРИТ
повышение риска летального исхода
ограничение применения антибиотиков
снижение стоимости лечения
Выберите ОДИН правильный ответ
Выберите ОДИН правильный ответ
введение в трахею интубационной трубки при помощи ларингоскопа
обследование ротовой полости при помощи шпателя
постановка трахеостомической трубки
выполнение манипуляций с соблюдением асептики и антисептики
использование средств индивидуальной защиты
работа в дневную смену
безопасность пациента
безопасность медицинского персонала
безопасность населения, проживающего на территории, прилегающей к медицинской организации
применение антибиотиков широкого спектра действия
увеличение заработной платы медицинским работникам
гигиеническая обработка рук путем мытья с мылом и водой
обработка рук кожным антисептиком
обработка рук хирурга
стрессовая ситуация
риск инфицирования
ситуация, не имеющая значения
Выберите ОДИН правильный ответ
приобретается медицинским персоналом во время работы (ВЕРНО)
условно-патогенные микроорганизмы (не верно)
присутствует на поверхности рук всегда
одноразовый непрокалываемый влагостойкий контейнер
плотно прилегающая крышка, исключающая возможность самопроизвольного вскрытия
размер не более 2 литров
лечащий врач с последующей отметкой в истории болезни
сотрудник анестезиологической службы с последующей отметкой в истории болезни
коротко подстриженные ногти
отсутствие искусственных ногтей
отсутствие повреждений на коже
снижение иммунного статуса организма
появление микроорганизмов устойчивых к воздействию антибиотиков и химических средств
применение наркотических анальгетиков с целью обезболивания
перевод пациента на парентеральное питание
защищает дыхательную аппаратуру от воздушно-капельной бактериальной и вирусной инфекции
является барьером на пути жидкостей (слюны, мокроты, конденсата)
снижает стоимость наркоза
усиливает действие наркотических анальгетиков
Выберите ОДИН правильный ответ
непреднамеренное воздействие опасных для здоровья лекарственных средств

К искусственной вентиляции легких (ИВЛ) прибегают для оказания помощи пациентам с острой или хронической дыхательной недостаточностью, когда больной не может самостоятельно вдыхать необходимый для полноценного функционирования организма объем кислорода и выдыхать углекислый газ. Необходимость в ИВЛ возникает при отсутствии естественного дыхания или при его серьезных нарушениях, а также во время хирургических операций под общим наркозом.
Что такое ИВЛ?
Искусственная вентиляция в общем виде представляет собой вдувание газовой смеси в легкие пациента. Процедуру можно проводить вручную, обеспечивая пассивный вдох и выдох путем ритмичных сжиманий и разжиманий легких или с помощью реанимационного мешка типа Амбу. Более распространенной формой респираторной поддержки является аппаратная ИВЛ, при которой доставка кислорода в легкие осуществляется с помощью специального медицинского оборудования.
Показания к искусственной вентиляции легких
Искусственная вентиляция легких проводится при острой или хронической дыхательной недостаточности, вызванной следующими заболеваниями или состояниями:
- хроническая обструктивная болезнь легких (ХОБЛ);
- муковисцидоз;
- пневмония;
- кардиогенный отек легких;
- рестриктивные патологии легких;
- боковой амиотрофический синдром;
- синдром ожирения-гиповентиляции;
- кифосколиоз;
- травмы грудной клетки;
- дыхательная недостаточность в послеоперационный период;
- дыхательные расстройства во время сна и т. д.
Инвазивная вентиляция легких
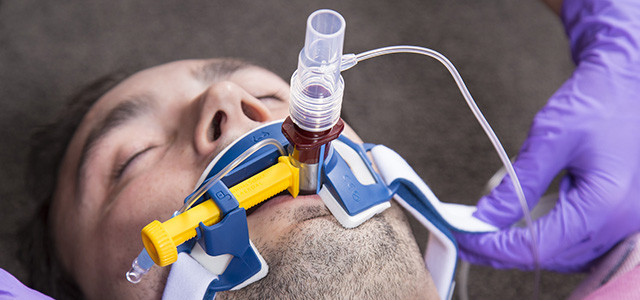
Эндотрахеальная трубка вводится в трахею через рот или через нос и подсоединяется к аппарату ИВЛ
При инвазивной респираторной поддержке аппарат ИВЛ обеспечивает принудительную прокачку легких кислородом и полностью берет на себя функцию дыхания. Газовая смесь подается через эндотрахеальную трубку, помещенную в трахею через рот или нос. В особо критических случаях проводится трахеостомия – хирургическая операция по рассечению передней стенки трахеи для введения трахеостомической трубки непосредственно в ее просвет.
Инвазивная вентиляция обладает высокой эффективностью, но применяется лишь случае невозможности помочь больному более щадящим способом, т.е. без инвазивного вмешательства.
Кому и когда необходима инвазивная ИВЛ?
Подключенный к аппарату ИВЛ человек не может ни говорить, ни принимать пищу. Интубация доставляет не только неудобства, но и болезненные ощущения. Ввиду этого пациента, как правило, вводят в медикаментозную кому. Процедура проводится только в условиях стационара под наблюдением специалистов.
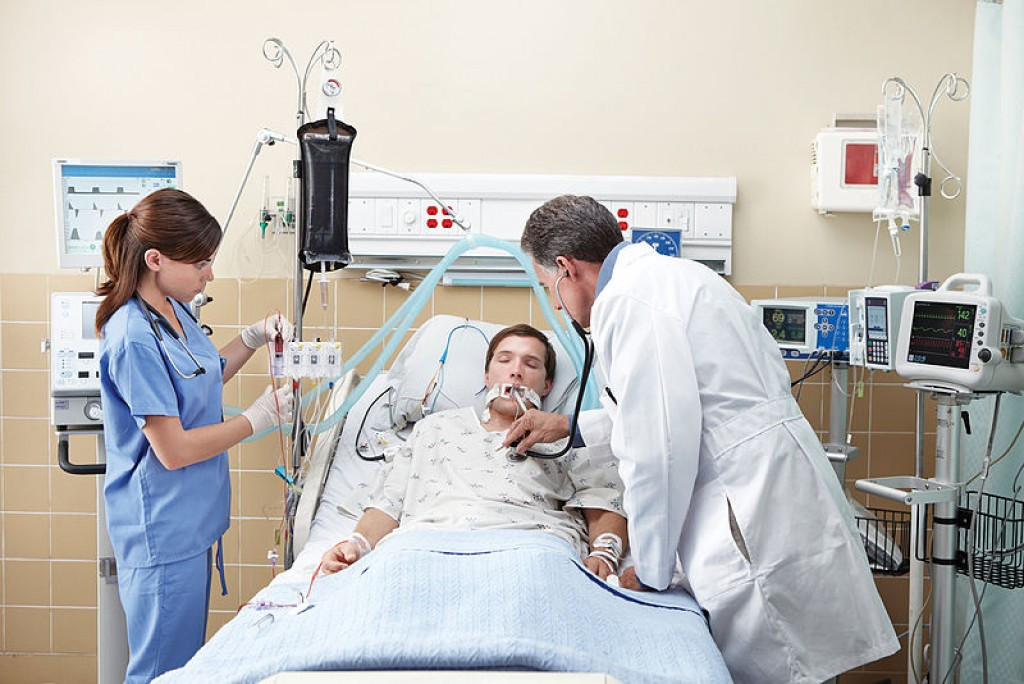
Инвазивная вентиляция легких отличается высокой эффективностью, однако интубация предполагает введение пациента в медикаментозную кому. Кроме того, процедура сопряжена с рисками.
Традиционно инвазивную респираторную поддержку применяют в следующих случаях:
- отсутствие эффекта или непереносимость НИВЛ у пациента;
- повышенное слюнотечение или образование чрезмерного количества мокроты;
- экстренная госпитализация и необходимость немедленной интубации;
- состояние комы или нарушение сознания;
- вероятность остановки дыхания;
- наличие травмы и/или ожогов лица.
Как работает аппарат инвазивной ИВЛ?
Принцип работы приборов для инвазивной ИВЛ можно описать следующим образом.
- Для краткосрочной ИВЛ эндотрахеальная трубка вводится в трахею больного через рот или нос. Для долгосрочной ИВЛ на шее пациента делается разрез, рассекается передняя стенка трахеи и непосредственно в ее просвет помещается трахеостомическая трубка.
- Через трубку в легкие подается дыхательная смесь. Риск утечки воздуха сведен к минимуму, поэтому больной гарантированно получает нужное количество кислорода.
- Состояние больного можно контролировать с помощью мониторов, на которых отображаются параметры дыхания, объем подаваемой воздушной смеси, сатурация, сердечная деятельность и др. данные.
Особенности оборудования для инвазивной вентиляции
Оборудование для инвазивной вентиляции легких имеет ряд характерных особенностей.
- Полностью берет на себя функцию дыхания, т.е. фактически дышит вместо пациента.
- Нуждается в регулярной проверке исправности всех клапанов, т.к. от работоспособности системы зависит жизнь больного.
- Процедура должна контролироваться врачом. Отлучение пациента от аппарата ИВЛ также предполагает участие специалиста.
- Используется с дополнительными аксессуарами – увлажнителями, откашливателями, запасными контурами, отсосами и т. д.
Неинвазивная вентиляция легких
За последние два десятилетия заметно возросло использование оборудования неинвазивной искусственной вентиляции легких. НИВЛ стала общепризнанным и широко распространенным инструментом терапии острой и хронической дыхательной недостаточности как в лечебном учреждении, так и в домашних условиях.
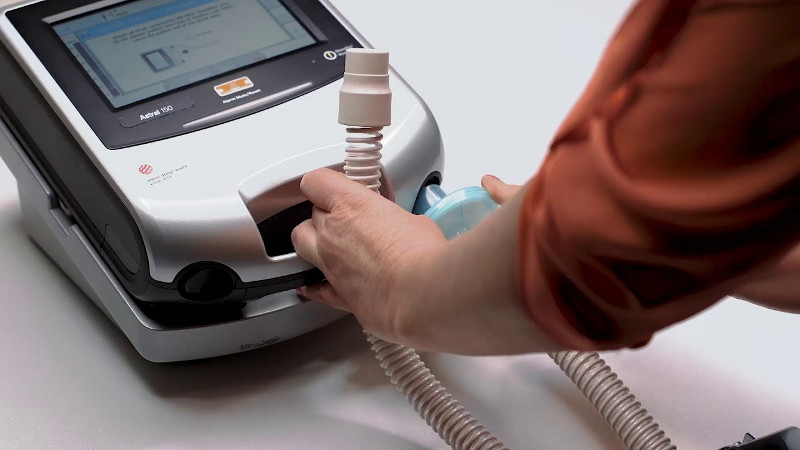
Одним из ведущих производителей медицинских респираторных устройств является австралийская компания ResMed
НИВЛ — что это?
Неинвазивная вентиляция легких относится к искусственной респираторной поддержке без инвазивного доступа (т.е. без эндотрахеальной или трахеостомической трубки) с использованием различных известных вспомогательных режимов вентиляции.
Оборудование подает воздух в интерфейс пациента через дыхательный контур. Для обеспечения НИВЛ используются различные интерфейсы – носовая или рото-носовая маска, шлем, мундштук. В отличие от инвазивного метода, человек продолжает дышать самостоятельно, но получает аппаратную поддержку на вдохе.
Когда применяется неинвазивная вентиляция легких?
Ключом к успешному использованию неинвазивной вентиляции легких является признание ее возможностей и ограничений, а также тщательный отбор пациентов (уточнение диагноза и оценка состояния больного). Показаниями для НИВЛ являются следующие критерии:
- одышка в состоянии покоя;
- частота дыхания ЧД>25, участие в респираторном процессе вспомогательной дыхательной мускулатуры;
- гиперкапния (PaC02>45 и его стремительное нарастание);
- уровень Ph

Успех реанимации во многом зависит от времени, прошедшего с момента остановки кровообращения до начала реанимации.
Показанием к проведению реанимационных мероприятий является состояние клинической смерти. Среди основных причин клинической смерти, требующих проведения реанимации ведущими являются: внезапная остановка кровообращения, обтурация дыхательных путей, гиповентиляция, апноэ, кровопотеря и повреждение мозга. Клиническая смерть — это период между жизнью и смертью, когда нет видимых признаков жизни, но еще продолжаются жизненные процессы, дающие возможность оживления организма. Длительность этого периода при обычной температуре тела составляет 5 – 6 минут, после чего развиваются необратимые изменения в тканях организма. В особых условиях (гипотермия, фармакологическая защита) этот период продлевается до 15—16 минут.
Признаками клинической смерти являются:
1. Остановка кровообращения (отсутствие пульсации на магистральных артериях) ;
2. Отсутствие самостоятельного дыхания (нет экскурсий грудной клетки) ;
3. Отсутствие сознания;
4. Широкие зрачки;
5. Арефлексия (нет корнеального рефлекса и реакции зрачков на свет):
6. Вид трупа (бледность, акроцианоз).
При проведении реанимации выделяется 3 стадии и 9 этапов. Символичная аббревиатура реанимационных мероприятий – первые буквы английского алфавита – подчеркивает принципиальную важность методичного и последовательного выполнения всех этапов.
Стадия I — элементарное поддержание жизни. Состоит из трех этапов:
A (airway open) — восстановление проходимости дыхательных путей;
В (breath for victim) — экстренная искусственная вентиляция легких и оксигенация;
С (circulation his blood) — поддержание кровообращения.
Стадия II — дальнейшее поддержание жизни. Заключается в восстановлении самостоятельного кровообращения, нормализации и стабилизации показателей кровообращения и дыхания. Стадия II включает в себя три этапа:
D (drug) — медикаментозные средства и инфузионная терапия;
Е (ECG) — электрокардиоскопия и кардиография;
F (fibrillation) — дефибрилляция.
Стадия III — длительное поддержание жизни в постреанимационном периоде. Заключается в послереанимационной интенсивной терапии и включает этапы:
G (gauging) — оценка состояния;
Н (human mentation) восстановление сознания;
I — коррекция недостаточности функций органов.
В настоящем пособии мы подробно разберем лишь I стадию реанимационных мероприятий (А, В, С), оставив остальные стадии и этапы для подробного изучения на следующих курсах.
Итак, этап А – восстановление проходимости дыхательных путей. При возникновении неотложных состояний проходимость дыхательных путей часто нарушена из-за западения языка, который прикрывает вход в гортань и воздух не может попасть в легкие. Кроме того, у больного в бессознательном состоянии всегда существует опасность аспирации и закупорки дыхательных путей инородными телами и рвотными массами.
1) запрокидывание (гиперэкстензия) головы,
2) выдвижение нижней челюсти вперед,
3) открывание рта. Для этого II— V пальцами обеих рук захватывают восходящую ветвь нижней челюсти больного около ушной раковины и выдвигают ее с силой вперед (вверх), смещая нижнюю челюсть таким образом, чтобы нижние зубы выступали впереди верхних зубов. При этой манипуляции происходит растяжение передних мышц шеи, за счет чего корень языка приподнимается над задней стенкой глотки.
При обструкции дыхательных путей инородным телом пострадавшему следует придать положение лежа на боку и в межлопаточной области произвести 3—5 резких ударов нижней частью ладони. Пальцем очищают ротоглотку, пытаясь удалить инородное тело, затем делают попытку искусственного дыхания. Если нет эффекта, производят попытку восстановления дыхательных путей приемом Греймлиха – форсированным надавливанием на живот. При этом ладонь одной руки прикладывают к животу по средней линии между пупком и мечевидным отростком. Вторую руку кладут поверх первой и надавливают на живот быстрыми движениями вверх по средней линии. После обеспечения проходимости дыхательных путей приступают к следующему этапу реанимации.
Этап В – искусственное дыхание. Искусственное дыхание — это вдувание воздуха или обогащенной кислородом смеси в легкие пациента, выполняемое без или с применением специальных устройств, то есть временное замещение функции внешнего дыхания. Выдыхаемый человеком воздух содержит от 16 до 18% кислорода, что позволяет его использовать для искусственного дыхания при проведении реанимации. Следует отметить, что у больных с остановкой дыхания и сердечной деятельности происходит спадение легочной ткани, чему в значительной степени способствует проведение непрямого массажа сердца. Поэтому необходимо проводить при массаже сердца адекватную вентиляцию легких. Каждое вдувание должно занимать 1—2 секунды, поскольку при более длительном форсированном вдувании воздух может попасть в желудок. Вдувание надо производить резко и до тех пор, пока грудная клетка пациента не начнет заметно подниматься. Выдох у пострадавшего при этом происходит пассивно, благодаря создавшемуся повышенному давлению в легких, их эластичности и массе грудной клетки. Пассивный выдох должен быть полным. Частота дыхательных движений должна составлять 12—16 в минуту. Адекватность искусственного дыхания оценивается по периодическому расширению грудной клетки и пассивному выдыханию воздуха.
Вспомогательную вентиляцию используют на фоне сохраненного самостоятельного, но неадекватного дыхания у больного. Синхронно вдоху больного через 1—3 дыхательных движения производится дополнительное вдувание воздуха. Вдох должен быть плавным и по времени соответствовать вдоху больного. Надо отметить, что восстановление самостоятельного дыхания быстро восстанавливает все остальные функции. Это связано с тем, что дыхательный центр является водителем ритма для мозга.
Этап С – поддержание кровообращения. После остановки кровообращения в течение 20 – 30 минут в сердце сохранены функции автоматизма и проводимости, что позволяет восстановить его насосную функцию. Независимо от механизма остановки сердечной деятельности, немедленно должна быть начата сердечно-легочная реанимация для предупреждения развития необратимого поражения тканей организма (мозга, печени, сердца и др. ) и наступления биологической смерти. Основной целью массажа сердца является создание искусственного кровотока. Следует понимать, что сердечный выброс и кровоток, создаваемый наружным массажем сердца, составляет не более 30% от нормы и только 5% нормального мозгового кровотока. Но, как правило, этого бывает достаточно для поддержания жизнеспособности центральной нервной системы во время сердечно-легочной и церебральной реанимации при условии достижения достаточной оксигенации организма на протяжении нескольких десятков минут. На догоспитальном этапе применяют только непрямой, или закрытый, массаж сердца (т. е. без вскрытия грудной клетки). Резкое надавливание на грудину ведет к сжиманию сердца между позвоночником и грудиной, уменьшению его объема и выбросу крови в аорту и легочную артерию, т. е. является искусственной систолой. В момент прекращения давления грудная клетка расправляется, сердце принимает объем, соответствующий диастоле, и кровь из полых и легочных вен поступает в предсердия и желудочки сердца. Ритмичное чередование сжатий и расслаблений в какой-то мере заменяет работу сердца, т. е. выполняется один из видов искусственного кровообращения. Техника проведения непрямого массажа сердца состоит в следующем. Больного укладывают на твердую ровную горизонтальную поверхность на спину (рис. 50). Проведение непрямого массажа сердца на панцирной кровати не имеет смысла – больной должен быть уложен на пол. Проводящий массаж
располагается сбоку от больного и кладет свои ладони (одну на другую) на нижнюю треть грудины выше основания мечевидного отростка на 2 – 3 см.
Следует обращать внимание на то, что на грудине располагается не вся ладонь, а только ее проксимальная часть в непосредственной близости к запястью (рис. 51). Собственно непрямой массаж сердца заключается в ритмичном (80 в минуту) надавливании на грудину пациента. При этом грудина должна опускаться не менее чем на 5 – 6 см.
Следует обращать внимание на то, что для правильного выполнения массажа руки следует почти полностью распрямить в локтевых суставах и давление на грудину производить всей массой туловища. Во многих руководствах рекомендуется начинать непрямой массаж сердца однократным сильным ударом в грудину больного, поскольку часто причиной нарушения сократимости миокарда является фибрилляция и прекардиальный удар способен купировать аритмию.
Собственно последовательность действий при сердечно-легочной реанимации следующая. Вариант I – реанимация проводится одним человеком:
- если пострадавший без сознания, ему максимально запрокидывают голову, поддерживая подбородок, чтобы рот был слегка приоткрыт. В случае необходимости выдвигают нижнюю челюсть. При подозрении на повреждение шейного отдела позвоночника используют умеренное запрокидывание головы только для поддержания проходимости дыхательных путей. Проверяют наличие самостоятельного дыхания (прослушивание и ощущение потока воздуха у рта, носа пострадавшего, наблюдение за экскурсией грудной клетки) ;
- если пострадавший не дышит, производят два глубоких раздувания легких (грудная клетка должна подняться). Каждое раздувание производят сравнительно медленно с течение 1-2 сек, затем делают паузу для осуществления полного пассивного выдоха;
- прощупывают пульс на сонной артерии (5-10с). При наличии пульса продолжают вентиляцию с частотой около 12 раздуваний в 1 мин у взрослых (одно раздувание каждые 5 с), 15 вдуваний в 1 мин у детей (около 4 с) и 20 вдуваний в 1 мин (одно каждые 3 с) у младенцев;
- если пульс отсутствует, приступают к непрямому массажу сердца;
- осуществляют 15 сдавлений грудины с частотой 80-100 в 1 мин. После 15 сдавлений производят два раздувания легких и продолжают чередовать 15 надавливаний на грудину с двумя раздуваниями легких;
- грудину прижимают к позвоночнику примерно на 4-5 см у взрослых, 2, 5-4 см у детей младшего возраста и 1-2 см у младенцев. Через каждые 1-3 мин проверяют восстановление спонтанного пульса.
Вариант II – реанимацию проводят два человека:
Реанимирующим следует находится с противоположных сторон пострадавшего, чтобы легче меняться ролями, не прерывая реанимации.
- если пострадавший без сознания, реаниматор (производящий вентиляцию) запрокидывает ему голову;
- если пострадавший не дышит, первый реаниматор делает два глубоких раздувания легких;
- проверяет пульс на сонной артерии;
- если пульс отсутствует, второй реаниматор начинает сдавление грудины с частотой 80-100 в 1 мин, первый реаниматор, проводящий вентиляцию, делает одно глубокое раздувание легких после каждых 5 компрессий грудины; во время раздувания легких второй реаниматор делает кратковременную паузу;
- затем продолжают чередование 5 надавливаний на грудину с одним раздуванием легких до появления самостоятельного пульса.
Признаками эффективности проводимого массажа являются сужение ранее расширенных зрачков, исчезновение бледности и уменьшение цианоза, пульсация крупных артерий (прежде всего сонной) соответственно частоте массажа, появление самостоятельных дыхательных движений. Непрямой массаж сердца не прекращают на срок более 5 с, проводить его следует до момента восстановления самостоятельных сердечных сокращений, обеспечивающих достаточное кровообращение. Показателем этого будут определяемый на лучевых артериях пульс и повышение систолического АД до 80-90 мм. рт. ст. Отсутствие самостоятельной деятельности сердца при несомненных признаках эффективности проводимого массажа есть показание к продолжению реанимации. Проведение массажа сердца требует достаточной выносливости; желательна смена массирующего каждые 5-7 мин, проводимая быстро, без нарушения ритмичности массажа сердца.
Читайте также:

