Эмбриологическое пособие что это
Обновлено: 04.07.2024
Дополнительной процедурой к вспомогательным репродуктивным технологиям является преимплантационная генетическая диагностика эмбрионов – ПГД (PGD) или преимплантационное генетическое тестирование – ПГТ. Главное преимущество данного метода - отсутствие селективного прерывания беременности, а также высокая вероятность рождения ребёнка без диагностируемого генетического заболевания.
ПГД — это проверка эмбриона, полученного с использованием экстракорпорального оплодотворения (ЭКО) на наличие генетических аномалий до его имплантации в полость матки. В этом случае возможно отобрать здоровые эмбрионы еще до стадии переноса.
Настоящая технология применяется почти 30 лет, и с каждым годом ее востребованность растет вместе с увеличением количества женщин, желающих родить после 35 лет. Манипуляция выполняется только при ЭКО, не предоставляет угрозы для женщины и не влияет на будущую беременность. Во время естественного зачатия провести такое исследование невозможно, но как альтернативный метод проводят пренатальную диагностику.
Однако, при получении негативных результатов обследования - паре будет предложено прервать беременность. Преимплантационная диагностика наследственных болезней позволяет избежать этого, так как манипуляция предоставляет максимум информации о зародыше, что дает возможность отобрать самые качественные клетки.
Процедуру проводят не всем, только, когда известно, что родители либо болеют, либо носители моногенного заболевания. Таким образом, можно определить, унаследует ли ребенок хромосомные патологии от родителей или нет. У пар, страдающих бесплодием, проводят не тестирование, а скрининг, поэтому потребность в таком исследовании небольшая.
Обследование выполняется для исключения мутаций или несбалансированной хромосомной перестройки. Перенос недиагностированных бластоцист не проводится.
В настоящее время известно более 40 моногенных генетических заболеваний. Самые распространенные:
Типы ПГД
ПГС – преимплантационный генетический скрининг.
ПГТ – преимплантационное генетическое тестирование – то же самое, что и диагностика. Под диагностикой понимают анализ методом FISH по определенному числу хромосом, а под тестированием – методом CGH/NGS с диагностикой всех хромосомных пар.
Несколько типов ПГТ исследований:
ПГТ-А – анализ анеуплоидий выявляет лишние или недостающие хромосомы в клеточном ядре, то есть направлен на выбор бластоцист с нормальным количеством хромосом. Он позволяет быстрее получить желаемую беременность (повышает шансы до 70-75%) и избежать переноса анеуплоидов, например, с синдромом Дауна.
ПГТ-М – тестирование на наличие наследственных болезней. Диагностика проводится только на выявление конкретной патологии, поэтому необходима дополнительная диагностика родителей для уточнения, в каком участке гена могла произойти мутация. Данный тип исследования гарантирует отсутствие конкретного дефекта, но не дает гарантии на отсутствие других нарушений в геноме.
ПГТ – SR – тестирование на наличие специфических перестроек в их ДНК, которые так же могут приводить к разным заболеваниям и передаваться по наследству.
Чтобы определить, какой метод диагностики будет наиболее эффективным для вашей пары, нужно записаться на консультацию к генетику.
Показания к проведению
Преимплантационное обследование рекомендуется парам с рисками передачи известных хромосомных аномалий своим детям. Наличие показаний для осуществления ПГД первоначально определяет репродуктолог, а решение о целесообразности такого исследования принимает врач-генетик. Оно может быть проведено в протоколе экстракорпорального оплодотворения за свой счет. Противопоказаний к проведению нет.
- Пары с Х-сцепленными нарушениями (риск для ребёнка 25%, половина из них мужского пола);
- Пары с хромосомными транслокациями, которые могут вызвать отсутствие имплантации, невынашивания беременности, или психические или физические нарушения у детей;
- Носители аутосомно-рецессивных расстройств (риск для ребёнка составляет 25%);
- Носители аутосомно-доминантный расстройств (риск для ребёнка составляет 50%).
Примерами распространенных заболеваний могут служить:
- муковисцидоз,
- фенилкетонурия,
- болезнь Тэй-Сакса,
- болезнь Гоше,
- пигментный ретинит,
- серповидно-клеточная анемия,
- талассемия,
- анемия Фанкони,
- гемофилия,
- миодистрофия Дюшенна,
- миодистрофия Бейкера,
- пузырчатка,
- поликистоз почек,
- болезнь Альцгеймера,
- ретинобластома,
- семейный рак груди,
- семейный аденоматозный полипоз,
- семейный канцероидный синдром,
- нейрофиброматоз,
- гидроцефалия,
- хорея Гентингтона,
- синдром Х-ломкой хромосомы,
- спиноцеребральная атаксия.
Делать ли ПГД?
Преимплантационное тестирование может потребоваться в следующих случаях:
- Возраст партнеров – женщин от 35 лет, а мужчины от 40;
- Невынашивание беременности, повторные самопроизвольные аборты, замершие беременности;
- Неудачные попытки ЭКО (две и более) в анамнезе;
- Генетические отклонения были ранее выявлены у детей или у плода;
- Причины мужского бесплодия;
- Тяжёлые нарушения сперматогенеза;
- Наличие у родителей наследственных болезней, имеющих половую принадлежность;
- Присутствие высокого риска рождения ребенка с моногенным заболеванием (например, с муковисцидозом, спинальной мышечной атрофией, фенилкетонурией и другими патологиями);
- Возможность резус-конфликта между матерью и будущим ребенком.
По желанию пар можно сделать ПГД эмбриона на:
- Определения пола
- Тестирования на совместимость по человеческим лейкоцитарным антигенам (HLA)
- Исключения болезней с поздним проявлением (болезнь Альцгеймера, РМЖ)
- Исключения болезней, не угрожающих жизни
- Тестирования наследственных предрасположенностей
Супружеские пары, которые не могут забеременеть естественным путем, получают консультацию генетика. Специалист при необходимости назначает анализы с целью определения кариотипа и дает индивидуальные рекомендации относительно необходимости проведения ПГД перед переносом.
ПГД эмбриона цена
Биопсия
Криоконсервация, витрификация, хранение
Генетика
ПГТ моногенного заболевания 1 категории сложности, включая подготовительный этап (заболевания, для которых разработаны элементы тест-системы).
ПГТ моногенного заболевания 1 категории сложности, включая подготовительный этап (заболевания, для которых разработаны элементы тест-системы)
Комбинированный тест ENDOMETRIO определение уровня рецептивности (тест ERA, микробиоты (тест EMMA) и патогенной микрофлоры эндометрия (тестАLICE)
Техника проведения манипуляции
Предимплантационное обследование рекомендуется парам с рисками передачи известных хромосомных аномалий своим детям. Наличие показаний для осуществления ПГД первоначально определяет репродуктолог, а решение о целесообразности такого исследования принимает врач-генетик. Оно может быть проведено в протоколе экстракорпорального оплодотворения за свой счет. Противопоказаний к проведению нет.
С чего начинается ПГД?
Подготовка к лечебному циклу ЭКО с ПГД практически не отличается от обычного лечебного цикла ЭКО:
- женщина принимает гормональные препараты для стимуляции суперовуляции;
- производится забор фолликулов с помощью пункции через влагалище;
- в условиях эмбриологической лаборатории проводится оплодотворение (ЭКО/ИКСИ) яйцеклеток сперматозоидами;
- культивирование в специальных условиях;
- тщательный отбор, отдается предпочтение нормально делящимся и морфологически полноценным зародышам;
- лабораторная биопсия трофэктодермы на 5-6 день культивирования (с помощью механического или лазерного метода), фиксация бластомера. Ранее ПГД проводилось на 3 день культивирования, однако проведение биопсии на этом этапе заметно снижает жизнеспособность эмбрионов. В то же время забор клеток на 5 день после оплодотворения не влияет на их дальнейшее развитие.
- криоконсервация после биопсии трофэктодермы;
- генетический тест зафиксированных клеток и получение результатов;
- эмбриотрансфер в полость матки эмбрионов без генетических дефектов;
- через две недели стандартная процедура диагностики беременности.
Сопутствующие риски и результаты исследования зависят от навыков и квалификации эмбриолога, проводящего биопсию. Такая процедура относится к высокотехнологичным и дорогим исследованиям. Поэтому предпочтительно сразу обращаться в крупные специализированные центры с возможностью проведения цитогенетического тестирования.
Результаты
По прошествии двух суток специалисты оценивают результаты и сопоставляют их с развитием соответствующего зародыша.
Если у него обнаружены отклонения, это означает обязательный отказ от переноса. В полость матки переносятся только те эмбрионы, у которых не было обнаружено патологий. Если исследование проводилось с цель рождения ребенка определенного пола (только по показаниям) или для предотвращения резус-конфликта, то подсаживаются соответствующие эмбрионы.
Схема ПГД применяется для конкретного случая своя. Если нарушение наследуется от женщины, то можно тестировать только полярные тельца. Можно также тестировать только бластомеры. Либо может проводиться последовательное изучение полярных телец, затем бластоцист. Какая именно схема будет применяться, определяется на консультации с врачом-генетиком.
Трофэктодерма: что это такое
В настоящее время предпочитают проводить биопсию трофэктодермы, а не забирать образцы еще не дифференцированной эмбриональной ткани. Такой подход позволяет увеличить жизнеспособность зародышей и минимизировать вред от манипуляции PGD.
Развитие эмбриона происходит по определенным закономерностям. После оплодотворения образуется зигота, которая начинает активно делиться, и количество зародышевых клеток растет в геометрической прогрессии. Продолжительность этого этапа до 3–4 суток. Затем происходит разделение клеток на 2 порции: наружную и внутреннюю. В толще эмбриональной клеточной массы формируется эксцентричная внутренняя полость – бластоцель, а достигшие этого этапа называются бластомерами. Трофэктодерма – наружный слой бластомера. Она является предшественником внезародышевых тканей, необходимых для нормальной имплантации эмбриона и последующего формирования плаценты. А внутренняя клеточная масса бластомера дает начало самому зародышу.
Внешний и внутренний листки бластоцисты имеют практически идентичный генный и хромосомный состав, поэтому информативность анализа трофэктодермы такая же высокая, как и при исследовании на более ранних этапах развития зародыша.
На какой день выполняют диагностику
На этапе подготовке к ЭКО у пар часто возникают вопросы: сколько делается ПГД и когда следует эмбриоперенос. Во многих клиниках, преимплантационная генетическая диагностика эмбрионов выполняется на 3 сутки. После оплодотворения яйцеклеток сперматозоидами в условиях эмбриологической лаборатории эмбрион развивается — клетки делятся. На третий день количество клеток достигает 6-8, что позволяет провести генетический анализ эмбриона без ущерба для дальнейшего развития зародыша.
В этот день происходит биопсия, то есть извлечение одного бластомера с помощью специальных микроинструментов. При стандартном протоколе без криоконсервации исследование выполняется за короткое время, так как эмбрион не может продолжать развиваться вне организма матери далее стадии бластоцисты (5-е сутки после оплодотворения). Пока выполняется генетическая диагностика, эмбрионы продолжают развиваться в соответствующей культуральной среде, после чего переносятся в полость матки на 5-е сутки развития. К этому времени эмбрион достигает стадии бластоцисты. Альтернативный подход – анализ ПГД в криоцикле. В этом случае биопсия производится на 5 день развития, а затем они подвергаются криоконсервации. Если в протоколе без верификации у эмбриологов остается не больше 48 часов для анализа, то в криоцикле специалист в течение месяца проводит генетическую диагностику.
Практика разобщённого цикла по сравнению со стандартным протоколом без криконсервации характеризуется: меньшим риском гиперстимуляции, большим количеством материала и временем для анализа, а также менее травматичной для эмбриона процедурой биопсии. В зависимости от вида протокола ЭКО специалисты индивидуально выбирают сроки проведения ПГС.
Используемые методы ПГД
У каждого метода свои преимущества и недостатки. Основные различия связаны с хромосомным числом, точностью результата и ценой процедуры.
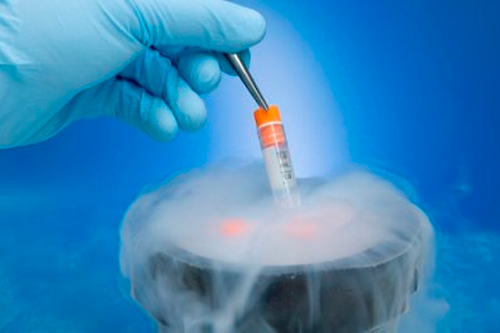
Криоконсервация – это метод замораживания и длительного сохранения биологического материала при очень низкой температуре. В таких условиях биологические процессы живых клетках останавливаются до момента размораживания.
Технологии криоконсервации биологического материала являются неотъемлемой частью современной репродуктивной медицины и широко используются при лечении бесплодия.
В рамках программ ВРТ, в нашей эмбриологической лаборатории успешно применяется замораживание сперматозоидов, яйцеклеток и эмбрионов.
Как осуществляют криоконсервацию и хранение замороженных эмбрионов, яйцеклеток, сперматозоидов?
Криоконсервация (замораживание) биологического материала подразумевает его длительное хранение при низкой температуре. Перед тем, как поместить эмбрионы, яйцеклетки или сперму в криохранилище, их обрабатывают специальными веществами – криопротекторами. Криопротекторы защищают живые объекты от отрицательного воздействия низких температур при замораживании и хранении.
Замороженные эмбрионы, яйцеклетки и сперматозоиды содержатся при температуре -196°С в индивидуальных контейнерах, помещаемых в специальные промаркированные ёмкости с жидким азотом. В состоянии глубокой заморозки половые клетки и эмбрионы могут храниться на протяжении многих лет. При этом все их биологические функции сохраняются.
На базе нашего отделения функционирует надежный и эффективный криобанк – специализированный комплекс оборудования, обеспечивающего возможность бережного замораживания, хранения и размораживания яйцеклеток, эмбрионов и спермы. Высококвалифицированный медицинский персонал осуществляет строгий контроль условий хранения и ведет непрерывный учет хранящегося биоматериала. Специалисты лаборатории эмбриологии обладают большим практическим опытом и успешно прошли стажировки на международных тренингах по криоконсервации эмбрионов и половых клеток с получением соответствующих сертификатов. Для обеспечения работы криобанка мы используем только высококачественное сертифицированное оборудование и материалы ведущих мировых производителей, соответствующие всем современным медицинским стандартам и требованиям.
Для замораживания эмбрионов и яйцеклеток в лаборатории эмбриологии ПУДП № 3 применяется самая передовая и безопасная технология сверхбыстрой заморозки – витрификация. Криоконсервированные таким способом яйцеклетки сохраняют свою способность оплодотворяться, а размороженные эмбрионы ничем не отличаются от эмбрионов до витрификации. Дети, рожденные после размораживания криоконсервированных половых клеток или эмбрионов, не имеют никаких отличий от детей, зачатых естественным путем.
Современные технологии криоконсервации не только с успехом применяются при лечении бесплодных пациентов, но и обеспечивают уникальную возможность планирования семьи для здоровых людей.
Что такое криоконсервация эмбрионов?
Криоконсервация эмбрионов – замораживание и сохранение эмбрионов при очень низкой температуре.
Для чего необходимо замораживать эмбрионы?
В большинстве случаев при проведении программы экстракорпорального оплодотворения созревает большое количество яйцеклеток. После их оплодотворения, как правило, получают достаточно много эмбрионов, однако в полость матки переносят не более 1 – 2-х. Если в текущем протоколе ЭКО удается получить больше эмбрионов, чем необходимо для переноса в данном цикле, или их перенос по медицинским показаниям невозможен, то такие эмбрионы могут быть заморожены. В дальнейшем они могут быть использованы для повторной попытки в том случае, если беременность в текущем цикле не наступит, или для рождения второго и последующих детей.
Преимущества замораживания эмбрионов
В каких случаях производится криоконсервация эмбрионов?
Криоконсервация эмбрионов производится в следующих случаях:
получение большего, чем требуется для переноса в полость матки, количества эмбрионов хорошего качества (для их использования в последующих попытках ЭКО);
высокий риск развития синдрома гиперстимуляции яичников;
снижение вероятности имплантации эмбриона в матку (например, при обнаружении полипа эндометрия, при недостаточной толщине эндометрия, при дисфункциональном маточном кровотечении);
ухудшение самочувствия женщины (обусловленное обострением бактериальной или вирусной инфекции, синдромом гиперстимуляции яичников, необходимостью выполнения экстренной операции и т.д.);
рубцовая деформация шейки матки, анатомическое сужение цервикального канала (стеноз), последствия оперативных вмешательств, препятствующие переносу эмбрионов в текущем цикле ЭКО;
участие в программе суррогатного материнства;
прохождение процедуры преимплантационной генетической диагностики эмбрионов;
неоднократные неудачные попытки ЭКО;
запланированное проведение химиотерапии или радиотерапии при онкологическом заболевании.
Все ли эмбрионы, полученные в цикле ЭКО, могут быть заморожены?
Следует отметить, что заморозке подлежат не все эмбрионы, полученные в цикле ЭКО, а лишь эмбрионы хорошего качества. Окончательное решение о необходимости и возможности криоконсервации принимается врачом и эмбриологом индивидуально для каждой пациентки.
Требуется ли специальная подготовка к переносу эмбрионов после криоконсервации?
В зависимости от особенностей репродуктивной системы пациентки (состояние эндометрия, гормональный фон и т.п.), подсадка размороженных эмбрионов может осуществляться в естественном цикле, либо в цикле с использованием заместительной гормональной терапии. Подготовка к переносу эмбрионов после криоконсервации выполняется под наблюдением врача.
Как долго можно хранить замороженные эмбрионы?
Замороженные эмбрионы могут храниться столько, сколько необходимо – от нескольких месяцев до нескольких десятков лет. При этом важно, чтобы пациенты поддерживали постоянную связь с учреждением, в котором хранятся криоконсервированные эмбрионы. По окончании каждого оплаченного периода хранения необходимо информировать сотрудников криобанка о дальнейшей судьбе хранящихся эмбрионов. У пациентов имеется возможность продлить договор хранения замороженного биоматериала; перенести эмбрионы в полость матки; утилизировать или дать разрешение на проведение научных исследований; а также донировать эмбрионы для бесплодных семей.
Влияет ли криоконсервация эмбрионов на результат ЭКО и развитие детей в будущем?
Криоконсервация эмбрионов не оказывает влияния ни на их качество, ни на развитие плода во время беременности. Дети, рожденные в результате беременности с использованием размороженных эмбрионов, ничем не отличаются от других детей.
Криоконсервация эмбрионов – это надежная и высокоэффективная методика, успешно применяемая в нашем отделении. Использование только самых эффективных и безопасных достижений мировой практики лечения бесплодия, а также высокий профессионализм и многолетний успешный опыт наших специалистов определяет высочайшее качество всех выполняемых нами процедур и помогает нам воплощать в реальность мечту наших пациентов о рождении здорового ребенка!
Известно, что репродуктивный возраст женщины ограничен – после 35 лет шансы забеременеть и родить здорового ребенка снижаются. Это связано с тем, что с годами увеличивается вероятность возникновения генетических мутаций в яйцеклетках. Кроме того, с возрастом женский организм начинает менее эффективно вырабатывать яйцеклетки, и их количество постепенно уменьшается. В результате забеременеть становится все сложнее. Однако, несмотря на то, что оптимальным для зачатия и рождения ребенка является возраст до 35 лет, многие женщины, в силу разных причин, вынуждены откладывать период создания семьи на более поздний срок.
Метод отсроченного материнства заключается в сохранении здоровых яйцеклеток. При этом возраст клеток остается таким, каким был возраст женщины к моменту их забора. Для получения необходимого количества яйцеклеток женщине, как правило, назначают гормональную стимуляцию, что позволяет получить несколько клеток одновременно. В том случае, если пациентке противопоказана гормональная стимуляция, возможно использование тактики накопления яйцеклеток, собранных в естественном цикле. Полученные яйцеклетки замораживают методом витрификации и хранят в криобанке до тех пор, пока пациентка, проконсультировавшись с врачом, не примет решение использовать их в программе ЭКО.
В каких случаях рекомендуется заморозить яйцеклетки?
Замораживание яйцеклеток рекомендовано в следующих случаях:
- планирование зачатия ребенка в более позднем возрасте;
- предстоящий курс лечения с применением лучевой, радио- или химиотерапии; серьезное оперативное вмешательство и любая другая необходимость в лечении с побочными эффектами, способными вызвать нарушение репродуктивной функции (в частности при наличии онкологических заболеваний);
- отсутствие возможности получения сперматозоидов на момент необходимости оплодотворения яйцеклеток (при отсутствии сперматозоидов в эякуляте, при невозможности получения эякулята, а также при отсутствии мужа или донора в день пункции);
- сохранение части яйцеклеток, полученных после пункции, для использования в следующих циклах ЭКО (если пациенты по каким-либо причинам не желают производить их оплодотворение и хранить криоконсервированные эмбрионы).
Как долго можно хранить замороженные яйцеклетки?
Замороженные яйцеклетки могут храниться в криобанке в течение неограниченного времени. При этом пациенткам необходимо регулярно продлевать договор хранения.
Отделение вспомогательных репродуктивных технологий ПУДП № 3 оснащено всем необходимым для криоконсервации яйцеклеток методом витрификации. Использование этой передовой технологии открывает новые возможности в планировании беременности и позволяет сохранить шанс испытать радость материнства в будущем!
Стоимость криоконсервации спермы: 6 000 руб.
Стоимость одного месяца хранения спермы: 1000 руб.
Если Вы решили сохранить сперму:
Анализ крови на ВИЧ, сифилис, гепатиты В и С (срок действия – 2 недели). Криоконсервация спермы производится при наличии отрицательного анализа на перечисленные инфекции.
Оформление необходимых документов. Перед сдачей биоматериала для криоконсервации в отделении ВРТ необходимо заполнить регистрационную анкету и информированное согласие на проведение услуги. Все документы можно оформить в день сдачи спермы для криоконсервации. При себе следует иметь паспорт.
Сбор биоматериала. Сдать материал можно в отделении ВРТ в день оформления документов.
Подготовка к криоконсервации спермы
За 3-5 дней до сдачи спермы для криоконсервации необходимо соблюдать воздержание от половых контактов и мастурбации. Рекомендуется отказаться от приема алкогольных напитков и сократить употребление выкуриваемых сигарет. Также следует воздержаться от принятия горячей ванны, посещения сауны или парной. Перед началом подготовки необходимо связаться с нашими специалистами и записаться на процедуру криоконсервации спермы.
Что такое криоконсервация спермы?
Криоконсервация спермы – метод хранения эякулята, который подразумевает его замораживание и хранение в жидком азоте при температуре -196°С. При такой низкой температуре все метаболические процессы в сперматозоидах останавливаются, а все их биологические функции сохраняются.
В каких случаях рекомендуется замораживание спермы?
Замораживание спермы рекомендовано в следующих случаях:
Отсутствие возможности или значительные затруднения в получении эякулята на момент необходимости оплодотворения яйцеклеток или при отсутствии мужа в день забора яйцеклеток (пункции) у супруги.
Необходимость в подстраховке при участии в программе ЭКО в случае тяжелого мужского бесплодия: выраженная олигозооспермия (снижение количества сперматозоидов в эякуляте), астенозооспермия (снижение числа подвижных сперматозоидов), тератозооспермия (повышенное содержание патологических сперматозоидов). При перечисленных патологиях эякулят сдают несколько раз, с перерывом в несколько дней, для накопления достаточного количества сперматозоидов.
Получение сперматозоидов путем биопсии яичка или его придатка.
Предстоящий курс лечения с применением лучевой, радио- или химиотерапии; хирургическое вмешательство и любая другая необходимость в лечении с побочными эффектами, способными вызвать нарушение репродуктивной функции.
Профессиональная деятельность, связанная с риском для здоровья/жизни или с воздействием на организм негативных факторов (химические соединения, ионизирующее излучение, высокие или низкие температуры).
Кроме того, заморозить сперму можно при отсутствии специальных показаний, по желанию пациента.
Как долго можно хранить криоконсервированную сперму?
Срок хранения криоконсервированной спермы в криобанке не ограничен, при этом пациентам необходимо регулярно продлевать договор хранения. После размораживания сперматозоиды сохраняют свою оплодотворяющую способность и, в зависимости от качества замороженной спермы, могут быть использованы для внутриматочной инсеминации, ЭКО или ИКСИ.
Каковы шансы на успешную беременность при использовании замороженных сперматозоидов в программе ЭКО?
Вероятность наступления успешной беременности с использованием замороженной спермы в программе ЭКО сопоставима с результатами экстракорпорального оплодотворения без использования криоконсервированного биоматериала.
Криоконсервация является надежным способом сохранения собственного генетического материала, доступным для наших пациентов нашего отделения. Современное материально-техническое оснащение и высокий профессионализм наших специалистов обеспечивает максимальное качество и безопасность как при выполнении процедуры криоконсервации, так и при дальнейших высокотехнологичных манипуляциях, связанных с экстракорпоральным оплодотворением.

Эмбриологическая лаборатория — в прямом смысле слова зона особого значения, образно говоря, святая святых: доступ в нее ограничен. Кроме специалистов-эмбриологов в лабораторию может попасть только лечащий врач.Такие меры необходимы, потому что именно здесь происходит самый ответственный этап экстракорпорального оплодотворения. Здесь, в условиях имитирующих внутреннюю среду организма человека оплодотворяются и выращиваются эмбрионы.
За дверями эмбриологической лаборатории происходят естественные процессы, предусмотренные самой Природой. Эмбриолог выполняет функции контролера-наблюдателя и его основная задача — содействие. Во время проведения процедуры Оплодотворения Вне Организма (иначе это называется ЭКО — экстракорпорального оплодотворения) эмбриолог помогает создать все благоприятные условия и добиться тем самым успешного результата.
В Шотландии много лет назад появилась своеобразная командная игра — керлинг. Игроки запускают тяжелую каменную биту по льду — кто дальше. И в то время, когда бита неспешно скользит к цели, вся команда дружно расчищает путь, полируя лед специальными метелочками: на результат может повлиять любая шероховатость.
Сначала с пациенткой работает врач-репродуктолог. При помощи гормональных препаратов он выращивает в яичниках женщины яйцеклетки, отслеживает рост клеток на УЗИ и готовит матку к подсадке эмбриона. Гинеколог специальными иглами извлекает яйцеклетки из организма будущей матери, находящейся в это время под общей анестезией. После этого их отправляют в эмбриологическую лабораторию.

Эмбриолог должен работать очень быстро, чтобы как можно скорее поместить очищенные яйцеклетки в специальную чашечку с теплой питательной средой. Эта чашечка с яйцеклетками будет храниться в инкубаторе при температуре 37 С и пятипроцентной концентрации углекислого газа в воздухе. На этом первый этап завершен.
Через час после извлечения яйцеклеток приходит время участия мужчины.
Сданная им сперма сначала проходит специальную обработку. Прежде всего эмбриолог должен перевести сперматозоиды из семенной жидкости в особый раствор, затем отобрать самые подвижные и активные спермии. А их сравнительно немного даже в норме — всего около 30%.

Присутствие мужчины в день оплодотворения в принципе не обязательно, он может сдать сперму и заранее — в этом случае она будет заморожена в жидком азоте при температуре −196 С. В таком виде сперма сохраняет свои свойства долгие годы. В нужный день ее разморозят и используют.
Для повышения эффективности оплодотворения используют технологию ИКСИ МАКС (ICSI — intracytoplasmic sperm injection), эмбриолог отбирает лучший сперматозоид и стеклянным микрокапилляром вводит его в яйцеклетку.
Через несколько часов мужское и женское ядра сольются в одно ядро, отцовские и материнские гены соединятся, и оплодотворенная яйцеклетка будет называться эмбрионом, или зародышем.

В течение дней эмбриолог наблюдает развитие эмбриона, контролируя условия культивирования.
Отобранные бластоцисты вместе с питательной средой помещают в пластиковый катетер, с помощью которого гинеколог переносит их в матку пациентки. Процедура безболезненная и анестезия для нее не требуется.
Судьба неподсаженных в матку матери хороших эмбрионов зависит от воли родителей. Они могут быть заморожены и сохранены в жидком азоте. При неудачной попытке они будут разморожены и перенесены в полость матки. Или же в случае удачной попытки и рождения ребенка подсажены матери — например, если супружеская пара, нуждающаяся в ЭКО, захочет завести еще одного ребенка.

Эффективность ЭКО в многом зависит от того, как протекает эмбриологический этап: от качества полученных женских и мужских половых клеток, от того, как произошло оплодотворение яйцеклеток, а потом как происходит развитие эмбрионов при культивировании. На каждом этапе может произойти сбой, который явится причиной неудачи ЭКО. Рассмотрим основные моменты.
1. "Ооцитарный фактор" - это получение в цикле ЭКО яйцеклеток плохого качества. Общеизвестный факт, что с возрастом женщины качество ооцитов стремительно ухудшается.
У пациенток младше 35 лет, довольно редко, но также возможно получение яйцеклеток низкого качества. В таких ситуациях крайне сложно ответить на вопрос, с чем может быть это связано, но, как правило, с генетикой, с гормональной стимуляцией, эндометриозом, с различными эндокринными нарушениями (особенно часто с ожирением).
Сейчас активно ведутся исследования по изучению данного фактора бесплодия. Но, к сожалению, пока они не завершены и не имеют практического значения.
В случае установления ооцитарного фактора (а понять это возможно только при получении ооцитов при пункции фолликулов) предлагается замена протокола гормональной стимуляции, переход на ЭКО в естественном цикле. При неэффективности этих схем, переход на ЭКО с донорскими ооцитами.
Плохое качество сперматозоидов не так прямо связано с возрастом мужчины, больше с различными внутренними и внешними неблагоприятными факторами, но также может быть причиной неудач ЭКО.
2. Неправильное оплодотворение
В яйцеклетке и сперматозоиде в норме содержится по 23 хромосоме. В процессе оплодотворения в яйцеклетке формируется 2 клеточных ядра (пронуклеуса) - 2 pn - женское и мужское. Оплодотворённая яйцеклетка (зигота) содержит в норме 46 хромосом (23 от матери и столько же от отца).
Пронуклеусы в оплодотворённой яйцеклетке становятся видны через 12-14 ч после проникновения в неё сперматозоида. Через 19-22 часа пронуклеусы исчезают и формируется метафазная пластинка, а ещё через 3-4 часа начинается деление зиготы.
Послее дробления зиготы с аномалиями оплодотворения могут быть неотличимы от нормально оплодотворённых ооцитов. Поэтому наблюдение пронуклеусов имеет важное значение - по их количеству оценивается правильное формирование эмбриона.
Встречаются следующие патологии формирования пронуклеусов:
- 1 pn - присутствие в зиготе одного пронуклеуса может говорить об активации яйцеклетки без участия сперматозоида, реже - о слиянии ядер гамет и образование диплоидной зиготы с одним пронуклеусом;
- 3 pn - наличие 3-х пронуклеусов возможно при :
- * оплодотворении одной яйцеклетки 2-мя сперматозоидами;
- * формирование 3-го пронуклеуса из материала невыделившегося второго полярного тельца;
- * формирование 3-го пронуклеуса путём аномального формирования ядерной мембраны ;
- реже встречаются >3 pn.
В неправильном оплодотворении могут играть роль следующие факторы:
- повышенные уровни эстрогенов в стимулированном цикле;
- продолжительность гормональной стимуляции;
- качество ооцита ("гигантские" ооциты предрасположены к неправильному оплодотворению);
- поздний репродуктивный возраст женщины (по данным американских учёных H. J. Kang, Z. Rosenwaks частота оплодотворения и 3 pn достоверно выше у пациенток после 39 лет, несмотря на метод оплодотворения)
3. Остановка развития эмбрионов после правильного оплодотворения
В современных эмбриологических лабораториях процесс культивирования эмбрионов отработан до мелочей и тщательно соблюдается: индивидуальное культивирование эмбриона в планшетных инкубаторах; постоянный многоуровневый контроль условий культивирования; своевременная смена питательных сред, если культивирование происходит в двухступенчатых средах.
Поэтому при стабильных условиях культивирования, причину плохого развития остается искать только в качестве самого материала.
На остановку эмбриогенеза влияет качество как самих яйцеклеток, так и качество сперматозоидов.
Как правило, основное влияние на ход эмбриогенеза оказывает возраст родителей. Хотя и в молодом возрасте может наблюдаться снижение качества яйцеклеток, например, при эндометриозе, неясном генезе бесплодия. Причиной могут быть аномалии в хромосомном наборе самих родителей.
Принято считать, что до 3 дня развития эмбрион живет и развивается на материнских запасах, то есть, остановка или ухудшение развития до 3 суток указывает на плохое качество яйцеклетки.
На 3 сутки развития начинает работать сам геном эмбриона. И здесь добавляются факторы, привнесенные в эмбрион сперматозоидом. К сожалению, очень многие отклонения от нормы в качестве сперматозоидов и хроматина внутри них оказывают влияние на развитие эмбриона и могут вызывать анеуплоидии или недостаточность генома эмбриона. Качество конденсации и организации ДНК сперматозоида является важным фактором развития эмбриона, даже при выполнении ИКСИ.
Но есть данные, что некоторое количество материнской мРНК сохраняется до стадии бластоцисты и может также участвовать в остановке развития.
Хромосомные аномалии, несомненно, вызывают большой процент потерь эмбрионов. Генетические факторы регулируют скорость предимплантационного развития эмбриона. Существует тенденция к увеличению количества анеуплоидных эмбрионов с увеличением возраста. Большая часть анеуплоидий летальна для эмбриона на ранних стадиях развития. Но некоторые анеуплоидии не мешают эмбриону стать бластоцистой хорошего качества, например, при трисомии по 21 хромосоме, или синдроме Дауна.
В связи с этим, пациентам позднего репродуктивного возраста рекомендуется проведение предимплантационного генетического скрининга до переноса эмбриона в полость матки.
Кроме того, у пар более молодого возраста, если в нескольких циклах ЭКО при переносе эмбриона хорошего качества на стадии бластоцисты в однородный, достаточной толщины и хорошо кровоснабжающийся эндометрий беременность не наступает, необходимо выполнение предимплантационного генетического скрининга на все хромосомы. И, соответсвенно, переносить в полость матки эмбрион только с полным хромосомным набором.
Читайте также:
- Какие функции осуществляет живое существо в биосфере
- Кто платит дополнительные взносы в пфр за вредность
- В условиях цифровизации уголовного судопроизводства возможна ли полная замена эксперта участника
- Тип правопонимания сторонники которого рассматривают переживание личного права как реальное право
- В каком случае ооо обязано проводить обязательный аудит годовой бухгалтерской отчетности за 2020 год

