Боковой амиотрофический склероз берут ли в армию
Обновлено: 04.07.2024
Боковой амиотрофический склероз (БАС) — хроническое прогрессирующее нейродегенеративное заболевание, характеризующееся поражением двигательных нейронов головного и спинного мозга и дегенерацией их аксонов. Частота • Из 100 000 населения страдают около пяти человек • В среднем один новый случай на 100 000 человек населения в год. Преобладающий возраст • Средний возраст начала заболевания — 55 лет • Вероятность возникновения увеличивается с возрастом. Преобладающий пол — мужской (1,5–2:1).
Классификация • Спорадический БАС, наиболее частая форма заболевания • Семейный БАС — заболевание, клинически подобное спорадическим формам БАС — 5–10% случаев • Комплекс острова Гуам (комплекс БАС-деменция-паркинсонизм) — редкий синдром, подобный БАС, как правило (но не всегда), связанный с паркинсонизмом и деменцией. Относительно часто встречается у коренного населения тихоокеанского острова Гуам.
Этиология и патогенез • Этиология спорадической формы БАС неизвестна. По ходу развития заболевания происходит дегенерация мотонейронов головного (в коре и стволе) и спинного (в передних рогах) мозга и их аксонов (в составе кортикобульбарных, кортикоспинальных трактов и периферических нервов). В патогенезе заболевания предполагают роль глутамата • Часть случаев семейной формы БАС обусловлена доминантными мутациями гена, кодирующего образование фермента Cu/Zn супероксиддисмутазы (SOD-1, локус 21q22.1–q22.2). В норме SOD-1 ингибирует ИЛ-1 b -конвертирующий фермент. Под действием последнего образуется ИЛ-1 b , инициирующий гибель нейронов после связывания со своим мембранным рецептором. Продукт дефектного гена SOD-1 не способен к ингибированию ИЛ-1 b -конвертирующего фермента, образующийся ИЛ-1 b индуцирует гибель мотонейронов на различных уровнях нервной системы. Учитывая наличие рецессивной формы, семейный БАС имеет более чем 1 локус в геноме. Рецессивная форма встречается редко и больше распространена в Тунисе (205100), характеризуется ранним началом (средний возраст — 12 лет) • Этиология комплекса острова Гуам неизвестна. В качестве причин заболевания рассматривают генетические факторы и факторы внешней среды. В типичных случаях синдром характеризуется сочетанием БАС, паркинсонизма и деменции у представителей одной семьи.
Генетические аспекты: • недостаточность супероксид дисмутазы 1, 147450, SOD1, 21q22.1, ALS1, 105400; • ALS2, 205100, 2q33 q35.
Патоморфология • Атрофия или отсутствие мотонейронов, сопровождающиеся умеренным глиозом без признаков воспаления •• Утрата гигантских пирамидных клеток (клетки Беца) двигательной коры •• Гибель мотонейронов в передних рогах спинного мозга, наиболее выраженные изменения происходят в шейных и поясничных сегментах •• Гибель клеток в двигательных ядрах ствола мозга, наиболее выраженные изменения происходят в ядре подъязычного нерва • Дегенерация боковых пирамидных путей спинного мозга • Атрофия передних корешков • Атрофия групп мышечных волокон (в составе двигательных единиц).
Клиническая картина
• Различные варианты сочетаний следующих основных симптомов: •• Признаки дисфункции мотонейронов передних рогов спинного мозга — слабость и атрофия мышц — наиболее часто начинаются на руках и, реже, ступнях, прогрессируют асимметрично и приводят к затруднению выполнения движений •• Болезненные спазмы (крампи), могут предшествовать мышечной слабости •• К симптомам дисфункции мотонейронов спинного мозга вскоре присоединяются признаки поражения кортикоспинальных трактов: видимые мышечные фасцикуляции, спастичность, усиление глубоких сухожильных (включая жевательный) и разгибательных подошвенных рефлексов (рефлекс Бабински) •• Дизартрия (нарушение речи) и дисфагия (нарушение глотания) •• Чувствительность, произвольные движения глаз и вегетативные функции сохранены.
• Сопутствующие симптомы •• Необъяснимая потеря массы тела •• Эмоциональная неустойчивость.
Диагностические критерии • Начало в среднем или пожилом возрасте, обычно после 40 лет • Прогрессирующая слабость мышц, генерализованное поражение • Отсутствие нарушений чувствительности.
Диагностические процедуры • Электромиография: фибрилляции, положительные волны, фасцикуляции даже в клинически непоражённых мышцах • Биопсия мышц: групповая атрофия мышечных волокон • Скорость проведения нервных импульсов сохранена вплоть до поздних стадий болезни.
Дифференциальная диагностика • Интоксикация свинцом • Спинальная мышечная атрофия (у взрослых) • Первичный боковой склероз • Семейный спастический парапарез • Спинальный множественный склероз • Тропический спастический парапарез • Миопатии • Грыжа межпозвонкового диска • Опухоли спинного мозга • Сирингомиелия • Врождённые аномалии шейного отдела позвоночника • Диабетическая амиотрофия • Полиомиелит.
ЛЕЧЕНИЕ
Физическая активность. Пациент должен по мере своих возможностей поддерживать физическую активность • По мере прогрессирования заболевания возникает необходимость в кресле-каталке и других специальных приспособлениях.
Диета • Дисфагия создаёт опасность попадания пищи в дыхательные пути • Иногда возникает необходимость в питании через зонд или в гастростомии.
Лекарственная терапия • Баклофен — для уменьшения спастичности • Хинин или фенитоин — для уменьшения болезненных спазмов • ТАД (амитриптилин по 10 мг 4 р/сут).
Наблюдение • Каждые 3 мес • По мере развития заболевания и необходимости симптоматической терапии — чаще.
Течение и прогноз • Заболевание неизлечимо, летальность составляет 100%, средняя продолжительность жизни — около 5 лет с момента установления диагноза • 50% пациентов умирают в течение 3 лет, 20% живут 5 лет, 10% — 10 лет с момента возникновения заболевания • При семейной доминантной форме — неполная пенетрантность, к возрасту 85 лет только приблизительно 80% носителей мутации имеют клинические проявления.
Возрастные особенности • Спинальные мышечные атрофии у детей и подростков клинически и патологически отличаются от БАС • Симптомы БАС иногда ошибочно приписывают пожилому возрасту.
Синонимы • Шарко болезнь • Болезнь Лоу Герига.
МКБ-10 • G12.2 Болезнь двигательного неврона
Код вставки на сайт
Боковой амиотрофический склероз (БАС) — хроническое прогрессирующее нейродегенеративное заболевание, характеризующееся поражением двигательных нейронов головного и спинного мозга и дегенерацией их аксонов. Частота • Из 100 000 населения страдают около пяти человек • В среднем один новый случай на 100 000 человек населения в год. Преобладающий возраст • Средний возраст начала заболевания — 55 лет • Вероятность возникновения увеличивается с возрастом. Преобладающий пол — мужской (1,5–2:1).
Классификация • Спорадический БАС, наиболее частая форма заболевания • Семейный БАС — заболевание, клинически подобное спорадическим формам БАС — 5–10% случаев • Комплекс острова Гуам (комплекс БАС-деменция-паркинсонизм) — редкий синдром, подобный БАС, как правило (но не всегда), связанный с паркинсонизмом и деменцией. Относительно часто встречается у коренного населения тихоокеанского острова Гуам.
Этиология и патогенез • Этиология спорадической формы БАС неизвестна. По ходу развития заболевания происходит дегенерация мотонейронов головного (в коре и стволе) и спинного (в передних рогах) мозга и их аксонов (в составе кортикобульбарных, кортикоспинальных трактов и периферических нервов). В патогенезе заболевания предполагают роль глутамата • Часть случаев семейной формы БАС обусловлена доминантными мутациями гена, кодирующего образование фермента Cu/Zn супероксиддисмутазы (SOD-1, локус 21q22.1–q22.2). В норме SOD-1 ингибирует ИЛ-1 b -конвертирующий фермент. Под действием последнего образуется ИЛ-1 b , инициирующий гибель нейронов после связывания со своим мембранным рецептором. Продукт дефектного гена SOD-1 не способен к ингибированию ИЛ-1 b -конвертирующего фермента, образующийся ИЛ-1 b индуцирует гибель мотонейронов на различных уровнях нервной системы. Учитывая наличие рецессивной формы, семейный БАС имеет более чем 1 локус в геноме. Рецессивная форма встречается редко и больше распространена в Тунисе (205100), характеризуется ранним началом (средний возраст — 12 лет) • Этиология комплекса острова Гуам неизвестна. В качестве причин заболевания рассматривают генетические факторы и факторы внешней среды. В типичных случаях синдром характеризуется сочетанием БАС, паркинсонизма и деменции у представителей одной семьи.
Генетические аспекты: • недостаточность супероксид дисмутазы 1, 147450, SOD1, 21q22.1, ALS1, 105400; • ALS2, 205100, 2q33 q35.
Патоморфология • Атрофия или отсутствие мотонейронов, сопровождающиеся умеренным глиозом без признаков воспаления •• Утрата гигантских пирамидных клеток (клетки Беца) двигательной коры •• Гибель мотонейронов в передних рогах спинного мозга, наиболее выраженные изменения происходят в шейных и поясничных сегментах •• Гибель клеток в двигательных ядрах ствола мозга, наиболее выраженные изменения происходят в ядре подъязычного нерва • Дегенерация боковых пирамидных путей спинного мозга • Атрофия передних корешков • Атрофия групп мышечных волокон (в составе двигательных единиц).
Клиническая картина
• Различные варианты сочетаний следующих основных симптомов: •• Признаки дисфункции мотонейронов передних рогов спинного мозга — слабость и атрофия мышц — наиболее часто начинаются на руках и, реже, ступнях, прогрессируют асимметрично и приводят к затруднению выполнения движений •• Болезненные спазмы (крампи), могут предшествовать мышечной слабости •• К симптомам дисфункции мотонейронов спинного мозга вскоре присоединяются признаки поражения кортикоспинальных трактов: видимые мышечные фасцикуляции, спастичность, усиление глубоких сухожильных (включая жевательный) и разгибательных подошвенных рефлексов (рефлекс Бабински) •• Дизартрия (нарушение речи) и дисфагия (нарушение глотания) •• Чувствительность, произвольные движения глаз и вегетативные функции сохранены.
• Сопутствующие симптомы •• Необъяснимая потеря массы тела •• Эмоциональная неустойчивость.
Диагностические критерии • Начало в среднем или пожилом возрасте, обычно после 40 лет • Прогрессирующая слабость мышц, генерализованное поражение • Отсутствие нарушений чувствительности.
Диагностические процедуры • Электромиография: фибрилляции, положительные волны, фасцикуляции даже в клинически непоражённых мышцах • Биопсия мышц: групповая атрофия мышечных волокон • Скорость проведения нервных импульсов сохранена вплоть до поздних стадий болезни.
Дифференциальная диагностика • Интоксикация свинцом • Спинальная мышечная атрофия (у взрослых) • Первичный боковой склероз • Семейный спастический парапарез • Спинальный множественный склероз • Тропический спастический парапарез • Миопатии • Грыжа межпозвонкового диска • Опухоли спинного мозга • Сирингомиелия • Врождённые аномалии шейного отдела позвоночника • Диабетическая амиотрофия • Полиомиелит.
ЛЕЧЕНИЕ
Физическая активность. Пациент должен по мере своих возможностей поддерживать физическую активность • По мере прогрессирования заболевания возникает необходимость в кресле-каталке и других специальных приспособлениях.
Диета • Дисфагия создаёт опасность попадания пищи в дыхательные пути • Иногда возникает необходимость в питании через зонд или в гастростомии.
Лекарственная терапия • Баклофен — для уменьшения спастичности • Хинин или фенитоин — для уменьшения болезненных спазмов • ТАД (амитриптилин по 10 мг 4 р/сут).
Наблюдение • Каждые 3 мес • По мере развития заболевания и необходимости симптоматической терапии — чаще.
Течение и прогноз • Заболевание неизлечимо, летальность составляет 100%, средняя продолжительность жизни — около 5 лет с момента установления диагноза • 50% пациентов умирают в течение 3 лет, 20% живут 5 лет, 10% — 10 лет с момента возникновения заболевания • При семейной доминантной форме — неполная пенетрантность, к возрасту 85 лет только приблизительно 80% носителей мутации имеют клинические проявления.
Возрастные особенности • Спинальные мышечные атрофии у детей и подростков клинически и патологически отличаются от БАС • Симптомы БАС иногда ошибочно приписывают пожилому возрасту.

Боковой амиотрофический склероз (БАС) представляет собой идиопатическое нейродегенеративное заболевание, развивающееся в результате избирательного поражения периферических мотонейронов передних рогов спинного мозга и двигательных ядер ствола мозга, а также корковых мотонейронов и боковых столбов спинного мозга. Имеет прогрессирующее хроническое течение, сопровождающееся парезом конечностей, с последующей атрофией мышц.
Манифестация болезни происходит у лиц в возрасте 40–60 лет (в среднем 56 лет). Чаще болеют представители мужского пола. Данная болезнь считается взрослой и не встречается у лиц младше 16 лет. Однако в последнее время рядом авторов отмечает учащение заболеваемости лиц молодого возраста (до 40 лет)
Несмотря на то, что данное заболевание изучается более ста лет, вопросы этиологии и патогенеза остаются открытыми. Примерно в 5–10 % случаев представляет сбой семейные или наследственные формы заболевания, остальные же (95–90 % случаев) спорадическими проявлениями заболевания. Считается, что они вызываются вирусами, и протекают по типу медленной инфекции.
В развитии БАС ключевую роль играет повышение активности глутаматергической системы. Избыток глутаминовой кислоты вызывает перевозбуждение и гибель нейронов. При этом оставшиеся двигательные нейроны могут спонтанно деполяризироваться, что клинически проявляется фасцикуляциями.
Различают следующие формы БАС
– высокая или же центральная
Данная классификация построена на основании того, какие мотонейроны преимущественно поражаются в начале заболевания. В дальнейшем она утрачивает свою значимость, т. к. в дальнейшем в патологический процесс вовлекаются все новые и новые мотонейроны на различных уровнях. Однако такое разделение необходимо для установки диагноза и определении прогноза.
Вначале заболевания, независимо от формы БАС, определяются общие симптомы. Преобладают двигательные нарушения, но чувствительность полностью сохраняется. Расстройств со стороны органов мочеиспускания и дефекации отсутствуют. Наблюдается прогрессирование болезни с захватом все новых и новых мышечных массивов, которая может привести к полной обездвиженности. Больных мучают периодических болезненные судороги в пораженных частях тела, так называемые крампи.
При пояснично-крестцовой форме заболевания возможно два варианта:
– В первом случае все начинается с мышечная слабость в одной ноге, затем она появляется и в другой. Связано это с только с поражения периферического двигательного нейрона, расположенного в передних рогах пояснично-крестцового отдела спинного мозга. У больных снижаются сухожильные рефлексы (коленный, ахиллов), снижается тонус мышц в ногах, постепенно формируются атрофии. Параллельно с этим, в ногах наблюдаются непроизвольные мышечные подергивания с небольшой амплитудой (фасцикуляции). Затем поражаются мышцы рук, в них также снижаются рефлексы, происходит их атрофии. Процесс поднимается, и поражается бульбарная группа двигательных нейронов. Вследствие этого развивается бульбарный синдром.
– Во втором случае, выявляются признаки одновременное поражение как центральных, так и периферических мотонейронов, обеспечивающих движение ног. При этом слабость в ногах сочетается с гиперрефлексией, мышечным гипертонусом и атрофиями мышц. Выявляются патологические рефлексы Бабинского, Гордона, Шеффера, Жуковского и др. Затем такие же изменения возникают и в руках. Затем поражаются мотонейроны, расположенные в головном мозге. Появляются дизартрия, дисфагия, атрофия и подергивания языка. Присоединяются насильственный смех и плач.
Шейно-грудная форма проявляется так же двумя способами:
– С одновременным поражением центральных и периферических двигательных нейронов. В верхних конечностях единовременно присутствует атрофии и гиперрефлексия, с патологическими кистевыми признаками, в нижних конечностях наблюдается гиперрефлексия, снижение мышечной силы, присоединяются патологически стопные рефлексы, при отсутствии атрофий. Позднее вовлекается бульбарный отдел.
При Бульбарной форме заболевания первыми симптомами поражения периферического мотонейрона в стволе мозга становятся расстройства артикуляции, дисфагия, афония, атрофия и фасцикуляции языка. Движения языка затруднены. При поражении центрального мотонейрона присоединяются усиленный глоточный и нижнечелюстной рефлекс, насильственный смех и плач. Усиливается рвотный рефлекс.
В результате прогрессирования болезни в руках выявляется парез, с атрофическими изменениями, гиперрефлексия, гипертонус мышц и патологические рефлексы. Такие же изменения возникают и в ногах, но позднее.
При высокая форме БАС преимущественно поражается центральный двигательный нейрона. При этом во всех группах мышц формируются парезы с повышенным мышечным тонусом и патологическими рефлексами.
Кроме нарушений в двигательной сфере, выявляются патологии и психическом состоянии больного БАС, такие как: нарушение памяти, мышление, интеллектуальные способности снижаются, доходящая вплоть до деменции, хотя и встречается очень редко.
При БАС высокая и бульбарная форма имеют более тяжелое течение, которое значительно ухудшает качество и продолжительность жизни по сравнению с шейно-грудной и пояснично-крестцовой формами.
Независимо от того, в какой форме в начале проявляется БАС, оно неуклонно прогрессирует, нарушается способность к самостоятельному передвижению, самообслуживанию. Если в процесс вовлекается дыхательная мускулатура, присоединяется одышка, наблюдаются приступы острой нехватки воздуха. При дальнейшем прогрессировании заболевания, больных переводят на ИВЛ, т. к. самостоятельно больной дышать уже не может.
Из-за поражение бульбарного отдела, нарушается жевание и глотание, нарушается герметичность ротовой полости, нижняя челюсть и голова свисают, что сопровождается постоянным слюнотечением, создается впечатление психически больного человека. Учитывая тот факт, что самосознание сохраняется до терминальной стадии, у больных развивается депрессия.
При БАС также формируются вегетативные расстройства: повышается потливость и сальность кожи, изменяется окраска кожи, конечности становятся холодными на ощупь.
Прогноз дальнейшей жизни зависит степени поражения бульбарного отдела и наличия дыхательных расстройств. Средняя продолжительность жизни составляет от 2 до 10 лет. Бульбарная форма, считается наиболее неблагоприятной, приводящей к смерти больного через 1,5–2 года. Причина смерти — паралич дыхательного центра. При шейно-грудной форме средняя продолжительность жизни составляет от 4 до 8 лет, а при пояснично-крестцовой форме 8–10 лет. В терминальную стадию болезни больные полностью прикованы к постели, дыхание поддерживается с помощью ИВЛ. Причиной смерти больных становится остановка дыхания, присоединение осложнений в виде пневмонии, тромбоэмболии, инфицирования пролежней с генерализацией инфекции.
В настоящее время Боковой амиотрофический склероз считается неизлечимым заболеванием, не разработано препаратов, которые могут остановить или замедлить прогрессирование данного заболевания на длительное время. Единственным препаратом, который оказывает терапевтический эффект, является Рилузол, блокирующий выброс глутамата, при использовании которого средняя продолжительность жизни увеличивается на 3 месяца. В последнее время активно ведутся разработки лечения стволовыми клетками. Этот метод обещает быть перспективным, но все же пока находится на стадии научных экспериментов.
Всем больным, страдающим БАС, показана симптоматическая терапия, основной целью которой является облегчение страдания, улучшение качества жизни.
- Бакулин И. С., Закройщиков И. В., Супонева Н. А., Захарова М. Н. Боковой амиотрофический склероз: клиническая гетерогенность и подходы к классификации. Нервно-мышечные болезни.
- Хондкариан О. А., Бунин Т. Л., Завалишин И. А., Боковой амиотрофический склероз,М.: Медицина 1978 264 с.
- Боковой амиотрофический склероз,Под ред.: Завалишин И. А., М.: Евразия+ 2007 г.
- Попова Л. М. Боковой амиотрофический склероз в условиях продленной жизни, М.: Медицина 1998,144 с.
- Алексеева Т. М., Стручевская Т. Р., Демешонок В. С. Боковой амиотрофический склероз: механизмы патогенеза и новые подходы к фармакотерапии (обзор литературы). Нервно-мышечные болезни.
Основные термины (генерируются автоматически): бульбарный отдел, продолжительность жизни, атрофия, БАС, спинной мозг, Боковой амиотрофический склероз, бульбарная форма, головной мозг, насильственный смех, одновременное поражение.
Боковой, или латеральный амиотрофический склероз (БАС, англ. ALS) – хроническое быстро прогрессирующее заболевание из обширной группы нейродегенеративных процессов. Как видно из общего названия, такие заболевания поражают паренхиматозные (функционально специализированные), в данном случае нейронные ткани. Нарушения клеточного питания (дистрофия) приводят к необратимым изменениям в нейронах – упрощению и распаду структуры с утратой функций (дегенерация), а затем к их массовому отмиранию с сокращением объема нервной ткани (атрофия). Учитывая роль нервной системы как высшего контрольно-аналитического и регуляторного центра, нетрудно видеть всю катастрофичность нейродегенеративных процессов, – какой бы характер они ни носили и каких бы ни касались нервных структур.
Боковой амиотрофический склероз поражает нейроны моторных (двигательных) полей коры головного мозга, а также мотонейроны передних и боковых рогов (столбов) спинного мозга. Таким образом, нейродегенерации и атрофии подвергаются структурные зоны и отделы центральной нервной системы, отвечающие за мышечный тонус, регуляцию и контроль мышечной активности в самом широком спектре, от напряжения мощной мускулатуры конечностей, спины, брюшной стенки – до мимических, дыхательных, артикуляторных движений, тонкой моторики пальцев и т.д.
Интересно отметить, что полноценных наблюдений у Ж.М.Шарко было чрезвычайно мало, – если сравнивать с современными представлениями об обязательном статистическом обосновании любых научных выводов и гипотез: он курировал пять пациентов лично, и еще полтора десятка описаний почерпнул из работ других специалистов. Повторилась ситуация с работой Джеймса Паркинсона о дрожательном параличе, основанной всего на шести наблюдениях за больными (причем троих из них Паркинсон наблюдал даже не в клинической практике). Однако необходимо учитывать, что оба заболевания относятся к категории, которую принято называть редкими болезнями.
Безусловно, этому всплеску общественного интереса и участия способствовала судьба Стивена Хокинга, всемирно известного британского физика и популяризатора науки, одному из двоих известных науке больных БАС с атипично долгой для этого заболевания продолжительностью жизнью (вторым является американский гитарист-виртуоз Дж.Беккер). При том, что официальный диагноз был установлен Хокингу в 21 год (гораздо раньше, чем в подавляющем большинстве случаев), а средняя продолжительность жизни после манифестации БАС составляет 2-4 года, Стивен Хокинг прожил исключительно долгую, необычайно активную (даже на этапе полной неподвижности), насыщенную и продуктивную жизнь, буквально до последних дней, – он умер в 2018 году в возрасте 76 лет, – обнаруживая истинно британскую стойкость духа в запредельно тяжелых обстоятельствах. Впрочем, история знает и другие подобные случаи: как правило, при БАС интеллект не страдает, и в абсолютно иммобилизованном теле остается порой очень и очень сильный разум, душа, воля, личность. Такова была история немецкого философа Франца Розенцвейга, который уже на смертном одре, прекрасно сознавая свои перспективы, заранее оговоренными движениями глаз надиктовывал жене свою последнюю работу. Розенцвейгу на момент смерти не было и 43 лет; с момента установления диагноза прошло около 7 лет, и даже такие темпы прогрессирования БАС можно считать атипично медленными. Случай же Стивена Хокинга настолько уникален и необъясним, что еще при жизни (и особенно после смерти) высказывались сомнения в правильности диагноза, – некоторые специалисты предполагали, например, что в действительности имел место полиомиелит , эпидемическая вспышка которого наблюдалась в Великобритании примерно в тот же период, на который пришлась манифестация нейромышечного синдрома у Хокинга.
Однако на сегодняшний день диагноз бокового амиотрофического склероза, атипично рано стабилизировавшегося и прогрессировавшего феноменально медленно, для данного случая считается однозначно доказанным. Да и это ли важно, по большому счету, когда речь идет о биографии таких людей, как Франц Розенцвейг или Стивен Хокинг; светлая им память, и пусть их пример придаст всем тем, кто страдает этим страшным заболеванием, воли и силы дождаться появления эффективной этиопатогенетической терапии.
Причины
В некоторых случаях БАС носит явно наследственный характер, однако доля таких случаев не превышает 5-8%. Генетические механизмы наследования и запуска патологического процесса остаются предметом исследований.
Высказывается масса гипотез касательно этиопатогенеза спорадического, ненаследственного БАС: экзотоксическая, генно-мутационная, вирусная и т.д.; согласно одной из них, в частности, амиотрофия объясняется накоплением продуктов клеточной жизнедеятельности при нарушении механизмов их переработки.
Однако все эти гипотезы нуждаются в подробном изучении и подтверждении (чего пока нет). Представление о боковом амиотрофическом склерозе как о мультифакторном и полиэтиологическом заболевании также, по сути, не объясняет ничего. Одним из важнейших вопросов, требующих ответа и препятствующих созданию этиотропной терапии, остается вопрос о том, почему избирательно поражается именно моторный тип нейронов и именно в тех участках, которые страдают при БАС.
Симптоматика
В зависимости от преимущественной локализации процесса, выделяют четыре основные формы:
Боковой амиотрофический склероз на сегодняшний день является неостановимым прогредиентным процессом и всегда приводит к летальному исходу, – как правило, на фоне отказа дыхательной мускулатуры. При бульбарной форме это может произойти раньше, чем паралич распространится на все отделы тела.
Диагностика
Первоочередной задачей является дифференциация бокового амиотрофического склероза от прочих нейродегенеративных заболеваний (той же сирингомиелии или сирингобульбии, например) и опухолевых процессов. Помимо детально проработанных клинических критериев, назначаются электромиография, МРТ головного мозга, лабораторные исследования. В качестве подтверждающего метода применяют, в частности, молекулярно-генетический анализ.
Лечение
Терапия во всех случаях паллиативна и направлена исключительно на облегчение симптоматики: миорелаксанты, антидепрессанты, специальные кресла и подушки, электронные устройства коммуникации, неинвазивная вентиляция легких; в терминальной стадии жизнь может быть продлена только с помощью ИВЛ и парентерального питания.
Препарат, который достоверно тормозит прогрессирование амиотрофии при БАС, носит название рилузол или рилутек. Он утвержден для применения с 1995 года, и новых лекарств не появлялось свыше 20 лет. В 2017 году получил одобрение FDA новый орфанный препарат для лечения больных БАС – эдаравон, – и еще два лекарства в настоящее время проходят клинические испытания. Однако ни одно из этих средств не является этиотропным и не может остановить процесс. Кроме того, такое лечение стоит очень дорого.
Основные надежды в плане победы над боковым амиотрофическим склерозом связываются с проводимыми сейчас интенсивными исследованиями и разработками в области генной терапии и терапии стволовыми клетками.

Photo: Erwin Nowak / Pixabay
Рилузол продлевает жизнь, дыхательная гимнастика увеличивает жизнеемкость легких, а музыкальная терапия положительно влияет на речь. Что еще нужно знать о методах помощи при БАС?
Время чтения: 8 мин.

Photo: Erwin Nowak / Pixabay
Лечение, адекватное конкретной ситуации
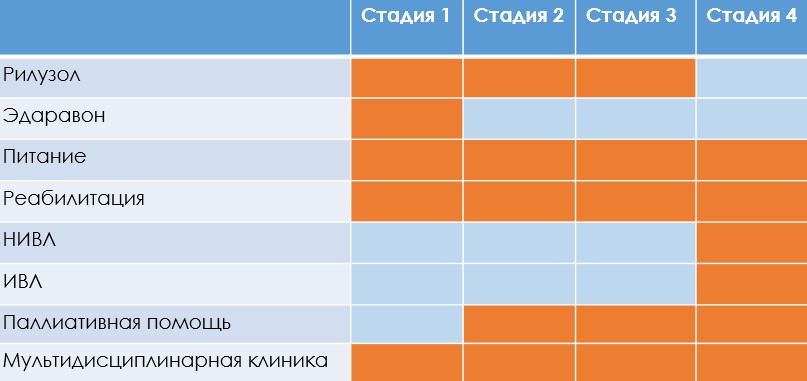
На сегодняшний день БАС не излечивается, однако существуют методы, позволяющие продлить жизнь пациента и улучшить ее качество. Но надо понимать, что каждый метод должен быть релевантен стадии болезни, ее течению, состоянию и желаниям самого больного и его родных.
Течение заболевания у разных людей — разное, стадии болезни — тоже. Сейчас заболевание БАС условно разделяют на 4 стадии , они характеризуются степенью вовлечения в болезнь групп мышц — рук, ног, мышц, отвечающих за речь, глотание.
Важно четко понимать, какой результат пациент получит от конкретного вида помощи: нужен ли ему препарат в его состоянии? Улучшит ли он качество его жизни? Или качество жизни останется прежним, но течение заболевания замедлится? Подходит ли лично ему этот метод? Какая помощь ему может понадобиться в будущем? По каждому конкретному виду помощи нужно обращаться к профессионалу, который на нем специализируется и сможет ответить на ваши вопросы: это может быть специалист по питанию, по вентиляции легких и т.д.
Ниже перечислены методы для улучшения прогноза и качества жизни, которые имеют определенную доказательную базу и вошли в Руководство помощи пациентам с БАС — в других странах и в России (у нас в стране такое руководство сейчас проходит процедуру утверждения, но сегодня рекомендации по БАС можно найти в Национально м руководстве по неврологии).
Препараты, применяемые при БАС
Первый метод — прием препаратов, использующихся для лечения бокового амиотрофического склероза.
Препарат Рилузол

ДНК-тесты при БАС: какими они бывают и стоит ли их делать? Кандидат биологических наук Федор Коновалов рассказывает о современных генетических тестах на мутации при боковом амиотрофическом склерозе, их целях и интерпретации результатов
Сейчас он выпускается в таблетках и в сиропе. В сиропе его можно давать через гастростому, если к этому моменту она уже установлена. Рилузол надо принимать по 50 мг два раза в день и контролировать при этом анализы крови, чтобы выявить на ранней стадии вероятность повреждения печени.
Однако этот препарат не должен назначаться всем больным автоматически. Рилузол рекомендуется людям, которые на момент назначения болеют менее 5 лет, а жизненная емкость их легких — более 60%. Дело в том, что Рилузол следует принимать как минимум 1,5 года, тогда он сможет продлить жизнь на несколько месяцев, а при более раннем начале приема — на 6-9 месяцев. Поэтому на поздних стадиях не имеет смысла начинать принимать препарат.
Если ваша цель — замедлить течение болезни, продлить жизнь, то Рилузол имеет смысл, так как его основное назначение — именно продление жизни.
В таком случае надо принимать этот препарат не менее 18 месяцев — именно в течение такого срока проводились основные исследования. Но необходимо понимать, что качество жизни при приеме Рилузола, по сути, не меняется. Недавно было опубликовано исследование, которое говорит о том, что прирост длительности жизни при приеме Рилузола происходит на четвертой, самой тяжелой стадии заболевания. Это тоже важно знать, когда вы решаетесь потратить определенные ресурсы на то, чтобы покупать этот препарат, контролировать безопасность его использования, проводить анализы.
Препарат Эдаравон
Говоря об эффективности препарата Эдаравон, мы опираемся лишь на одно небольшое исследование, проведенное в Японии и специально сконструированное таким образом, чтобы максимизировать вероятность получения положительного результата. В исследовании принимали участие пациенты, полностью независимые в самообслуживании, их жизненная емкость легких составляла более 80%, а длительность болезни — не более двух лет (от начала проявления симптомов — не с момента постановки диагноза). Они получали этот препарат внутривенно, по сложной схеме, большинство из них — параллельно с Рилузолом. Длительность лечения составила 24 недели. У этой группы людей препарат замедлил скорость прогрессирования заболевания на 33%.
Однако по более длительному использованию этого препарата исследований нет: никто не может сказать, какой эффект у него будет через год, два, три после начала приема. Отдельное исследование, куда включили более широкую группу пациентов, не показало его эффективности. Это довольно редкий случай, когда FDA — американское управление по санитарному надзору за качеством пищевых продуктов и медикаментов — вдруг, неожиданно для всех, зарегистрировало препарат, несмотря на узкие показания в самом исследовании.
Где искать достоверную информацию о препаратах?
Чтобы узнавать о других медикаментах, которые назначаются врачами и используются людьми при БАС, можно обращаться к ресурсу ALSUntangled. Он был придуман Ричардом Бэдлаком (Richard Bedlack), американским неврологом, который решил проанализировать и систематизировать все препараты, используемые людьми при этом заболевании. К каждому препарату прилагается табличка с итогами исследований, где в сжатом виде перечислены результаты испытаний на животных, на людях, обоснованность применения препарата и его безопасность. Эти данные Ричард Бэдлак получает от неврологов, которые занимаются БАС по всему миру.
Большая часть обзоров с ресурса ALSUntangled переведена на русский язык.
Немедикаментозное лечение
Питание
Модификация питания так или иначе нужна всем людям с БАС, так как у многих снижается масса тела или нарушается глотание.
Есть распространенное мнение, что раз мы мало двигаемся, мы должны меньше есть. Это не совсем так. На основании нескольких исследований по поводу питания при БАС специалисты пришли к выводу, что при этой болезни пациентам подходит как раз гиперкалорическая диета, при которой человек должен получать больше калорий, чем тратит.
Если давать универсальную рекомендацию по питания для людей с БАС, то за основу нужно брать массу тела человека — ее нужно стабилизировать с помощью гиперкалорической диеты. Актуальные данные указывают на то, что должна быть подобрана диета с повышенным содержанием жиров и углеводов (данных насчет повышенного содержания белков нет).
Установка гастростомы пациентам с БАС: взгляд невролога Показания к установке гастростомы пациентам с боковым амиотрофическим склерозом, риски и ограничения к операции
Гипохолестеринемические препараты — статины — лучше отменять при этом заболевании, если нет жестких показаний от кардиологов.
Важно сказать и про гастростому — она позволяет человеку с БАС питаться, когда нарушается глотание. Имея большой собственный опыт в установке гастростом, мы считаем, что устанавливать ее нужно до того, как жизнеемкость легких станет меньше 50%. Дело в том, что при меньшей жизненной емкости легких люди плохо переносят эту манипуляцию, несмотря на ее простоту: это 10-минутная манипуляция, которая проводится под поверхностной анестезией.
Вовремя установленная гастростома улучшает качество жизни — и не только самого человека с БАС, но и его семьи, поскольку ухаживающие тратят меньше времени на то, чтобы накормить человека.
Поддерживающая реабилитация
Поддерживающая реабилитация позволяет стабилизировать состояние на определенных участках болезни, на коротких промежутках времени, а в некоторых случаях — даже улучшать. Например, если говорить о дыхательных упражнениях, они могут на определенных участках времени увеличивать жизнеемкость легких.
К поддерживающей реабилитации относятся:
- физическая терапия; ;
- логопедия;
- музыкальная терапия (мы сейчас проводим исследование по изучению ее эффекта на больных БАС).
Проще говоря, есть два способа улучшить качество жизни человека с БАС, сделать его более самостоятельным в самообслуживании. Первый заключается в том, чтобы восстановить определенный объем утраченных движений, научить человека вставать, ходить. Этим занимается физическая терапия — дыхательные упражнения, упражнения для улучшения и поддержания костно-мышечной системы на начальных стадиях болезни и — для профилактики осложнений на более поздних стадиях.
Второй способ — это эрготерапия. Когда у человека уже не получается вставать, его можно научить пользоваться специальным креслом, научить пересаживаться в него, передвигаться, готовить еду и т.д., в том числе, адаптируя окружающее пространство.
Что касается музыкальной терапии, в конкретных протоколах по БАС ее пока нет. Но смысл музыкальной терапии в том, что она, используя по определенным протоколам музыку, музыкальные инструменты, голос, взаимодействие с терапевтом, позволяет корректировать определенные физиологические параметры — речь, дыхание.
Доказательств того, что поддерживающая терапия замедляет течение БАС при длительном применении, пока нет. Однако она улучшает качество жизни, так что ее нельзя игнорировать при ведении пациентов с этой болезнью.

Физическая терапия при БАС: в чем отличия от ЛФК? Врач-невролог Тимур Иванов — о том, что дает физическая терапия и как правильно пациенту с неврологическими проблемами ей заниматься
Неинвазивная вентиляция легких (НИВЛ)
Неинвазивной вентиляцией легких (НИВЛ) пользуется чуть меньше половины пациентов с БАС. Этот метод лечения подходит не всем людям с боковым амиотрофическим склерозом, либо используется не всеми: кто-то не переносит его, кто-то — просто не имеет доступа к аппаратуре.
Основным показанием для использования неинвазивной масочной вентиляции является наличие жалоб: недомоганий, связанных с нехваткой кислорода. Использование этого метода увеличивает продолжительность жизни и улучшает самочувствие пациента с БАС. Процент жизнеемкости легких здесь не столь важный фактор: первичны не цифры, а именно облегчение, которое испытывает человек от использования этого оборудования. Такого мнения придерживаются многие специалисты, в том числе зарубежные коллеги.
Если человек при длительной вентиляции испытывает серьезные неудобства, и его самочувствие при этом не улучшается, то убедить его продолжать пользоваться аппаратом очень сложно. Его смогут использовать только мотивированные люди, которые ощущают эффект.
Если мы все правильно сделали , в начале использования НИВЛ качество жизни улучшается, а затем — и это надо иметь в виду — оно может снижаться. Если вентиляция становится длительной, и человек беспрерывно находится в маске, это вызовет проблемы, о которых не всегда говорят в начале лечения, но о которых важно знать. Когда маска постоянно на лице, человеку может быть неприятно общаться, неудобно есть, говорить, у него даже могут возникать пролежни на лице, маску надо периодически менять, ухаживать за кожей лица. Кроме того, для пациентов с БАС характерно слюнотечение, надо периодически вытирать слюну, и здесь маска мешает. А у некоторых людей ношение маски вызывает клаустрофобию.
Инвазивная вентиляция легких (ИВЛ)
Инвазивная вентиляция легких (ИВЛ) может существенно продлить жизнь человека с БАС — но этот метод сильно ухудшает ее качество. Крошечный процент людей, не более 10% — при должном обсуждении заранее и объяснении всех моментов, связанных с этим видом вентиляции, — соглашается на ИВЛ.
Паллиативная помощь
Паллиативная помощь сильно недооценена в нашей стране, а раньше она и не была показана людям с боковым амиотрофическим склерозом. Сейчас пациент с БАС может получить такую помощь, но надо понимать, что в нашей стране существует предубеждение против паллиатива: люди тяжело реагируют, воспринимают назначение паллиативной помощи как приговор, как вестника скорой смерти или как отказ врача от дальнейшей медицинской помощи пациенту.

Паллиативная медицинская помощь пациентам с БАС Нарушения дыхания и глотания, трудности коммуникации и другие симптомы при боковом амиотрофическом склерозе
В Англии, к примеру, совсем иная картина. В Лондоне я присутствовал на приеме пациента с БАС у врача. Врач еще не был до конца уверен, какой тип БАС у этого человека, но порекомендовал ему обратиться в паллиативную службу — не потому, что отказался от него как врач. А потому, что помогать такому пациенту должны одновременно неврологи, пульмонологи и все остальные специалисты — в том числе, по паллиативной медицине. Они лучше разбираются в ситуациях, связанных с принятием решений в сложные жизненные моменты: эти специалисты не увеличивают время жизни пациента, но знают, как существенно улучшить ее качество, как лечить тягостные симптомы.
Мультидисциплинарная клиника
Для того, чтобы скоординировать лечение БАС, нужна мультидисциплинарная клиника со специалистами разного профиля.
Есть исследования, которые показывают, что ведение пациентов в таких мультидисциплинарных клиниках продлевает им жизнь, улучшает прогноз и качество жизни больного и его семьи. Такие мультидисциплинарные команды понимают, что на разных стадиях заболевания нужна различная помощь.
Вам может быть интересно:
Читайте также:
- Чего ждал евгений онегин от предстоящей поездки приключений наследства скуки
- Реструктуризация и реорганизация как инструменты финансового оздоровления коммерческой организации
- Какие проявления экстремизма носят протестный характер
- Какие формы участия общественности в исправлении несовершеннолетних осужденных закреплены в уик рф
- Какой оклад у повара в детском саду