Декапептил при эко в длинном протоколе для чего
Обновлено: 08.07.2024
вспомогательные вещества: натрия хлорид, кислота уксусная ледяная, вода для инъекций.
Описание
Прозрачный бесцветный раствор.
Фармакотерапевтическая группа
Противоопухолевые гормональные препараты. Гормоны и их производные.
Гонадотропин-рилизинг гормона аналоги. Трипторелин.
Код АТХ L02AE04
Фармакологические свойства
После подкожного введения Декапептила системная биодоступность трипторелина составляет около 100 %. Период полувыведения трипторелина составляет примерно 3-5 ч, что свидетельствует о том, что трипторелин будет выведен из организма в течение 24 ч, и, соответственно, он будет отсутствовать в кровообращении на момент переноса эмбрионов. Метаболизм с образованием более простых пептидов и аминокислот в основном происходит в печени и почках. Трипторелин главным образом выводится с мочой.
Клинические исследования свидетельствуют о том, что риск накопления трипторелина у пациентов с серьезными нарушениями функции печени и почек является незначительным (период полувыведения у таких пациентов составляет приблизительно 8 ч).
Угнетение функции гипофиза с помощью Декапептила может предотвратить повышение уровня ЛГ и, таким образом, преждевременную овуляцию и (или) лютеинизацию фолликулов. Лечение с помощью агониста ГнРГ позволяет снизить частоту отмены циклов и повысить частоту наступления беременности в циклах вспомогательных репродуктивных технологий (ВРТ).
Показания к применению
– предупреждение преждевременного повышения уровня лютеинизирующего
гормона (ЛГ) у женщин, которым проводят контролируемую
гиперстимуляцию яичников в рамках вспомогательных репродуктивных
- предоперационное уменьшение размера миомы, с целью уменьшения
кровопотери и боли во время хирургического вмешательства
- симптоматическое лечение эндометриоза
Способ применения и дозы
Лечение Декапептилом следует начинать под контролем врача, имеющего опыт в лечении бесплодия у женщин. Декапептил предназначен для подкожного введения один раз в сутки в нижнюю часть брюшной стенки. После первой инъекции рекомендуется наблюдать за пациенткой в течение 30 мин для выявления симптомов возможной аллергической/псевдо-аллергической реакции на инъекцию. При этом необходимо обеспечить наличие надлежащих условий и лекарственных средств для возможного лечения таких реакций. Дальнейшие инъекции пациенты могут проводить самостоятельно при условии получения соответствующих инструкций врача о признаках и симптомах, которые могут свидетельствовать о реакции повышенной чувствительности, о последствиях такой реакции и необходимости немедленного медицинского вмешательства. Для профилактики липодистрофии следует постоянно менять место введения препарата.
Предупреждение преждевременного повышения уровня лютеинизирующего
гормона (ЛГ) у женщин, которым проводят контролируемую гиперстимуляцию яичников в рамках вспомогательных репродуктивных технологий (ВРТ)
Лечение можно начинать в начале фолликулярной фазы (2-й или 3-й день менструального цикла) или посередине лютеиновой фазы (21-й - 23-й день менструального цикла или за 5-7 дней до ожидаемого начала менструаций). Контролируемую гиперстимуляцию яичников гонадотропинами следует начинать примерно через 2-4 недели после начала лечения Декапептилом. Необходимо контролировать реакцию яичников методами, которые включают или только УЗИ яичников, или, желательно, УЗИ яичников в сочетании с измерением концентрации эстрадиола, и в случае необходимости корректировать дозу гонадотропинов. После того как соответствующее количество фолликулов достигнет нужного размера, лечение Декапептилом и гонадотропинами прекратить и одноразово ввести инъекцию человеческого хорионического гонадотропина (чХГ) для индукции окончательного созревания фолликулов. Если через 4 недели не будет подтверждена эффективность метода (что определяется либо только подтверждением при УЗИ отслойки эндометрия или, желательно, методом УЗИ в сочетании с определением концентрации эстрадиола), следует рассмотреть вопрос о прекращении лечения Декапептилом. Общая длительность лечения обычно составляет от 4 до 7 недель. При применении Декапептила следует обеспечить поддержку лютеиновой фазы согласно с утвержденными схемами лечения.
Пациентам с нарушениями функции почек или печени не требуется коррекция дозы.
Миома матки, эндометриоз
Побочные действия
Очень часто (≥1/10)
- снижение полового влечения, нарушение сна
- вульвовагинальная сухость, вагинальное кровотечение
Часто (от ≥1/100 до
Противопоказания
- повышенная чувствительность к трипторелину или другим компонентам
- повышенная чувствительность к гонадотропин-рилизинг гормону (ГнРГ) или
к любому другому аналогу ГнРГ
- беременность и период лактации
- детский возраст до 18 лет
Лекарственные взаимодействия
Необходимо очень осторожно применять трипторелин вместе с препаратами, влияющими на гипофизарную секрецию гонадотропных гормонов, при этом рекомендуется контролировать гормональное состояние пациента.
Нельзя исключать вероятность взаимодействий с обычно используемыми лекарственными препаратами, включая препараты, высвобождающие гистамин.
Особые указания
Применение агонистов ГнРГ может вызвать снижение минеральной плотности костей. С особой осторожностью следует применять препарат для лечения пациентов с дополнительными факторами риска развития остеопороза (например, хроническое злоупотребление алкоголем, курение, длительная терапия препаратами, снижающими минеральную плотность костей, такими как, противосудорожные средства или кортикостероиды, остеопороз в семейном анамнезе, нарушения питания, нервная анорексия).
По имеющимся на данный момент данным, у большинства женщин после отмены лечения костная масса восстанавливается.
Поскольку уменьшение минеральной плотности костей у пациентов с дополнительными факторами риска развития остеопороза может быть более опасным, решение о терапии трипторелином следует взвешенно принимать в каждом отдельном случае и терапию следует начинать только тогда, когда по результатам тщательной оценки определено, что польза от лечения преобладает над риском. При этом следует применять дополнительные меры противодействия снижению минеральной плотности костей.
В редких случаях терапия агонистами ГнРГ может выявить наличие ранее не диагностированной гонадотропной аденомы гипофиза. У таких больных может развиваться гипофизарная апоплексия, характеризующаяся внезапной головной болью, рвотой, нарушением зрения и офтальмоплегией.
У пациентов, получающих терапию агонистами ГнРГ, такими как, трипторелин, наблюдается повышенный риск развития депрессивных состояний. Пациентов необходимо проинформировать об этом и назначать необходимое лечение в случае возникновения соответствующих симптомов.
Стимуляцию яичников необходимо осуществлять под тщательным медицинским наблюдением.
У пациентов с нарушением функции почек или печени конечный период полувыведения трипторелина составляет 7-8 ч по сравнению с 3-5 ч у здоровых пациентов. Несмотря на такое более продолжительное действие, ожидается, что трипторелин будет выведен из кровообращения до момента переноса эмбрионов.
С особой осторожностью следует применять препарат для лечения женщин с признаками и симптомами активных аллергических состояний или известной склонностью к аллергическим реакциям в анамнезе. Не рекомендуется применять Декапептил для лечения женщин с тяжелыми аллергическими состояниями в анамнезе. Женщин репродуктивного возраста необходимо тщательно обследовать до начала лечения, чтобы исключить возможность беременности.
Применение ВРТ связано с повышенным риском развития многоплодной беременности, смерти плода в период беременности, внематочной беременности и врожденных пороков развития. Эти риски сохраняются в случае применения Декапептила в качестве вспомогательной терапии при контролируемой гиперстимуляции яичников. Применение Декапептила при контролируемой гиперстимуляции яичников может повысить риск развития синдрома гиперстимуляции яичников (СГЯ) и кист яичников.
Стимуляция фолликулов, вызванная применением аналогов ГнРГ и гонадотропинов, может заметно усиливаться у небольшого числа предрасположенных пациенток, особенно при наличии синдрома поликистозных яичников.
Подобно другим аналогам ГнРГ, сообщалось о случаях развития синдрома гиперстимуляции яичников (СГЯ) в связи с применением трипторелина в сочетании с гонадотропинами.
Синдром гиперстимуляции яичников (СГСЯ)
СГСЯ включает значительное увеличение размера яичников, высокие уровни половых стероидов в сыворотке крови, а также повышение сосудистой проницаемости, что может привести к накоплению жидкости в брюшной, плевральной и, в редких случаях, перикардиальной полостях.
В тяжелых случаях СГСЯ может наблюдаться следующая симптоматика: абдоминальная боль, вздутие живота, значительное увеличение размера яичников, увеличение массы тела, диспноэ, олигурия и желудочно-кишечные проявления, включая тошноту, рвоту и диарею. При клиническом обследовании могут быть обнаружены гиповолемия, сгущение крови, нарушение баланса электролитов, асцит, гемоперитонеум, плевральный выпот, гидроторакс, острый легочный дистресс-синдром и тромбоэмболические явления.
Чрезмерная реакция яичников на лечение гонадотропинами редко вызывает развитие СГСЯ, кроме случаев, когда для стимуляции овуляции применяют человеческий хорионичекий гонадотропин (чХГ). Соответственно, в случаях развития СГСЯ целесообразно отменить введение чХГ и посоветовать пациентке воздержаться от половых контактов или использовать барьерные методы контрацепции в течение не менее 4 дней. СГСЯ может быстро прогрессировать (от 24 ч до нескольких дней) и стать серьезным медицинским осложнением; соответственно, за состоянием пациенток следует наблюдать в течение не менее двух недель после введения чХГ.
СГСЯ может приобретать более тяжелую и более продолжительную форму в случае наступления беременности. Чаще СГСЯ наблюдается после прекращения гормонального лечения и достигает максимальной тяжести примерно через 7-10 дней после лечения. Обычно СГСЯ проходит самостоятельно с наступлением менструации.
Если наблюдается СГСЯ в тяжелой форме, лечение гонадотропинами необходимо прекратить (если оно еще продолжается), пациентку следует госпитализировать и начать специфическую терапию СГСЯ, которая включает покой, внутривенные вливания растворов электролитов или коллоидов и гепарина.
Этот синдром чаще наблюдается у пациенток с синдромом поликистозных яичников. Риск развития СГСЯ может быть выше в случае применения агонистов ГнРГ в сочетании с гонадотропинами по сравнению с применением только гонадотропинов.
На начальном этапе лечения агонистами ГнРГ могут образовываться кисты яичников. Обычно они бессимптомные и нефункциональные.
Миома матки и эндометриоз
Дальнейшее маточное кровотечение во время лечения возникать не должно (кроме первого месяца), в противном случае необходимо проверить уровень эстрогена в плазме крови. Если этот уровень ниже 50 пг/мл, следует искать возможные органические поражения. После прекращения лечения функция яичников восстанавливается, менструальные кровотечения возобновляются через 7-12 недель после последней инъекции.
В течение первой недели лечения следует использовать негормональные контрацептивы, поскольку первичная секреция гонадотропинов может стимулировать овуляцию. Также их следует использовать, начиная с 4-ой недели после последней инъекции до восстановления менструации или до назначения нового метода контрацепции.
Во время лечения миомы матки необходимо регулярно определять размер матки и миомы. Непропорционально быстрое уменьшение размера матки по сравнению с сокращением тканей миомы в отдельных случаях приводило к кровотечению и сепсису.
Беременность и период лактации
Перед началом лечения женщины детородного возраста должны пройти тщательное обследование для исключения вероятности беременности.
Имеющиеся ограниченные данные о применении трипторелина во время беременности не свидетельствуют о повышенном риске врожденных пороков развития. Тем не менее, количество длительных проспективных исследований развития слишком ограничено. Данные исследований на животных не указывают на прямое или косвенное вредное воздействие на течение беременности или послеродовое развитие плода, но есть данные о фетотоксичности и задержке родов. Согласно данным о фармакологическом действии, нельзя исключать неблагоприятное влияние на беременность и на плод, поэтому применение Декапептила во время беременности не рекомендуется.
Во время лечения препаратом и до восстановления менструаций женщинам детородного возраста рекомендуется использовать негормональные методы контрацепции.
Неизвестно, выделяется ли трипторелин в грудное молоко. В связи с потенциальными побочными реакциями на трипторелин у грудных детей рекомендуется прекратить грудное вскармливание до начала и во время применения препарата.
Особенности влияния лекарственного средства на способность управлять транспортным средством или потенциально опасными механизмами
Учитывая побочные действия препарата, следует соблюдать осторожность при управлении транспортным средством или потенциально опасными механизмами.
Передозировка
Симптомы передозировки могут быть вызваны длительным применением препарата. О каких-либо побочных эффектах вследствие передозировки не сообщалось.
Лечение: следует временно прекратить лечение Декапептилом.
Форма выпуска и упаковка
По 1 мл препарата помещают в стеклянные шприц-ампулы с иглами, снабженными защитными колпачками.
По 7 шприц-ампул помещают в пластиковую ячейковую упаковку.
По 1 ячейковой упаковке вместе с инструкцией по медицинскому применению на государственном и русском языках помещают в картонную упаковку.
Экстракорпоральное оплодотворение
Именно ЭКО стало прорывной технологией в лечении бесплодия. В настоящее время это словосочетание известно большинству людей, ибо получило широкое распространение. Означает оно оплодотворение вне тела матери: эмбрион получают в лаборатории (не в пробирке, как считают многие, а в специальной чашке с лунками), культивируют его 72-144 часа и затем переносят в матку, где он и развивается.
Как известно, в естественных условиях в организме женщины созревает одна яйцеклетка (крайне редко – две). Именно они и получает шанс на продолжение рода – оплодотворение и образование эмбриона. С этого и начиналось ЭКО: поначалу получали ту самую единственную яйцеклетку из единственного фолликула (пузырька на яичнике, в котором яйцеклетка зреет), оплодотворяли и переносили эмбрион в матку. Результаты, конечно, были неважными: процент забеременевших был низким. Однако, для женщин, которые первыми шли на процедуру, это был единственный шанс, так как новая процедура предлагалась тм, у кого не было маточных труб и, соответственно, никаких шансов забеременеть естественным путем.
С тех пор развитие фармакологии привело к появлению гонадотропинов – гормонов, способных стимулировать рост не одного, а нескольких (иногда десятков) фолликулов и получению большего количества яйцеклеток (ооцитов). Параллельно развивалась и эмбриология, получившая возможность длительного (до 5-6 дней) культивирования эмбрионов, замораживания, проведения генетических исследований и т.д. появилось множество разновидностей ЭКО: от ЭКО в естественном цикле до длительных схем с генетической диагностикой по определенным генам родителей с целью исключения возможности рождения ребенка с наследственными и спонтанными генетическими заболеваниями.

Какие ооциты получают при стимуляции
С момента достижения величины 2-5 мм фолликулы становятся чувствительными к ФСГ (фолликулостимулирующему гормону, он вырабатывается в нашем организме) и вступают в фазу гормонозависимого роста. В естественном менструальном цикле в ходе гормонзависимой фазы роста антральные фолликулы имеют различное количество рецепторов к ФСГ и ЛГ. Из многих фолликулов происходит отбор 5-10 (иногда и десятков) фолликулов, несущих достаточное количество гормональных рецепторов. Эти фолликулы и составляют когорту потенциально овуляторных (будущих доминантных) фолликулов. Именно эти фолликулы можно простимулировать, вводя в организм ФСГ. При естественном развитии событий фолликул, клетки которого несут наибольшее количество рецепторов к ФСГ, становится доминантным и ооцит, содержащийся в нем получает шанс к опллодотворению. Каждый цикл рекрутируется (начинает расти) множество фолликулов (до 8 000), среди них выбирается один доминантный, а остальные подвергаются атрезии, то есть отмирают.
Виды стимуляции при ЭКО
В данной статье мы рассмотрим ЭКО со стимуляцией (есть варианты без стимуляции, но это другая история). Итак, пациентка обследована и подготовлена к ЭКО. Стимуляция должна быть начата с 1-2го дня менструального цикла (редко позже), ибо именно в этот момент и идет выбор доминантного фолликула (помните, как всё устроено?). Любая стимуляция – это введение гормона ФСГ. Репродуктологу необходимо определить:
- можно ли начать стимуляцию без предварительной подготовки организма или подготовка нужна;
- какой/какие из гонадотропинов (гормональных лекарств для стимуляции) назначить;
- в какой ежедневной дозировке нужно вводить препарат пациентке;
- Как часто проводить ультразвуковой контроль роста фолликулов (т.н мониторинги).
Если гонадотропины назначаются без предварительной подготовки организма, протокол называется коротким, если подготовка проводится и стимуляция назначается только после неё – протокол называют длинным.
Цель стимуляции – получение возможно большего количества ооцитов. Но на этом пути возможны проблемы: если один из фолликулов (обычно это тот, который готов был стать доминантным) совулирует (лопнет), это нарушит состояние остальных, и поучение из них ооцитов станет проблематичным, либо полученные ооциты будут повреждены. Для предотвращения этой ситуации вводят лекарство (тоже гормональное), которое предотвращает нежелательную овуляцию.
Таких препаратов 2 класса:
1.Антагонисты релизинг-фактора. Это вещества, которые подавляют овуляцию, назначаются по достижении фолликулами размера 14мм (раннее назначение может остановить рост).
2.Агонисты релизинг фактора. Вещества другого профиля назначаются одновременно с гонадотропинами для стимуляции и в начале усиливают их действие. Но ближе к концу стимуляции они оказывают обратное действие – тормозят овуляцию. Применяются как в коротком, так и в длинном протоколе.

Отличия длинного протокол ЭКО
Показания к длинному протоколу
Длинный протокол – эдакий эталон стимуляции, дающий наилучшие результаты. Его целесообразно применять у пациентов, у которых нет риска гиперстимуляции. Существуют, однако, общепризнанные показания к назначению длинного протокола.
- эндометриоз, миома матки;
- большой разброс в размерах антральных фолликулов во II фазе менструального цикла, предшествующего стимуляции;
- неудачный исход стимуляции в коротком протоколе.
Как проводится длинный протокол

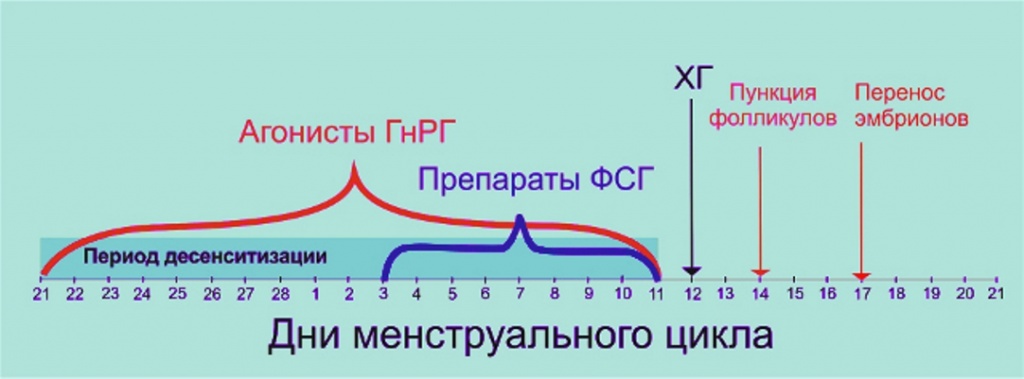
Длинный протокол ЭКО.
ТВРП – пункция, ЭТ – перенос эмбрионов, аГнРГ – агонисты.
Недостатки длинного протокола
- Риск гиперстимуляции: главное противопоказание к назначению длинного протокола – мультифолликулярные яичники, при которых гиперстимуляция вероятна;
- Длительность протокола. Безусловно, общая продолжительность в 22-24 дня многим кажется излишней;
- Не всегда отличная переносимость: крайне редко может отмечаться ухудшение самочувствия, связанное с введением агонистов;
- Удорожание протокола (некритичное) по сравнению с коротким протоколом.


Аншина Маргарита Бениаминовна
Скидка 50% на первичный прием репродуктолога
Заполнив анкету для будущих родителей, вы сэкономите время врача на первичном приеме, поэтому он будет для вас стоить 50% от обычной цены.

Чтобы экстракорпоральное оплодотворение прошло успешно, требуется достаточное количество яйцеклеток. Например, по некоторым данным, чтобы получить один эмбрион, у женщины в возрасте до 35 лет в среднем нужно 9 половых клеток, после 35 лет – 12, после 37 лет – 16.
Однако во время естественной овуляции созревает лишь один фолликул с ооцитом. Чтобы получить больше, нужна стимуляция гормональными препаратами.
Можно, конечно, обойтись и без гормонов – провести ЭКО в естественном цикле. Но шансы на наступление беременности при этом будут очень малы.
В зависимости от схемы введения препаратов существуют два основных протокола ЭКО – длинный и короткий. Их продолжительность, соответственно, составляет около 6 и 4 недель. Часто женщины спрашивают у врачей-репродуктологов: какой протокол лучше?
Видимо, если бы один из них был идеален во всех отношениях, то в клиниках применяли бы только его. Но на деле в каждой схеме есть свои нюансы, преимущества и недостатки. Давайте разбираться.
Длинный протокол
Ключевая особенность этой схемы гормональной стимуляции в том, что в ней есть подготовительный этап – регулирующая фаза. Она начинается за неделю до последнего дня менструального цикла. Во время нее вводят препарат, подавляющий выработку фолликулостимулирующего и лютеинизирующего гормонов. Применяют агонисты гонадотропин-рилизинг-гормона (ГнРГ): бусерелин, лейпрорелин, трипторелин, либо его агонисты: цетрореликс, ганиреликс. С помощью этих препаратов останавливают менструальный цикл.
Обычно регулирующая фаза продолжается 10–15 дней. Когда она завершается, выполняют ультразвуковое исследование яичников и анализ крови на эстрадиол. Нужно, чтобы в яичниках не было фолликулов диаметром более 15 мм, и чтобы уровень эстрадиола не превышал 50 пг/мл.
На 2–7-й день менструального цикла начинается фаза стимуляции. Женщине вводят препараты фолликулостимулирующего гормона. Они способствуют созреванию фолликула в яичнике. При этом женщина продолжает получать агонисты ГнРГ, но их доза снижается. По-прежнему периодически проводят УЗИ и анализы на уровень эстрадиола. Фаза стимуляции продолжается 8–12 дней, и во время нее выполняют от 4 до 6 ультразвуковых исследований.
Признаки того, что можно переходить к следующему этапу:
- если взять любые три фолликула, то их средний диаметр будет больше 20 мм;
- толщина эндометрия (слизистой оболочки матки) более 8 мм;
- достаточно высокий уровень эстрадиола.
Преимущества и недостатки длинного протокола
Длинный протокол позволяет полностью контролировать процесс созревания фолликулов. При этом удается избежать преждевременной лютеинизации – состояния, из-за которого ухудшается качество ооцитов и эмбрионов, снижается вероятность наступления беременности после оплодотворения. С помощью длинного протокола можно получить максимальное количество яйцеклеток. Он является оптимальным выбором для женщин с некоторыми гинекологическими заболеваниями, а также при плохом качестве яйцеклеток, полученных во время короткого протокола.
Есть и некоторые недостатки. При длинном протоколе существенно повышается риск развития синдрома гиперстимуляции яичников, когда они слишком сильно реагируют на высокие уровни гормонов. Чаще всего это осложнение протекает в легкой форме: беспокоят небольшие боли в животе, отмечается вздутие живота, женщину беспокоит тошнота, рвота, диарея. Тяжелый синдром гиперстимуляции яичников по время ЭКО встречается крайне редко.
Риск этого осложнения минимален, если гормональную стимуляцию проводит опытный врач, который применяет современные препараты и тщательно подбирает их дозы.
Кроме того, препараты, которые применяются во время регулирующей фазы, могут вызвать такие симптомы, как перепады настроения, приливы, постоянное чувство усталости, нарушение сна, головные боли, потливость по ночам.
В каких случаях применяют длинный протокол?
Длинный протокол ЭКО с регулирующей фазой оптимален в следующих случаях:
- возраст женщины младше 35 лет;
- избыточная масса тела;
- низкий риск синдрома гиперстимуляции яичников;
- избыток мужских половых гормонов в организме (гиперандрогения);
- миома матки, эндометриоз и некоторые другие гинекологические заболевания;
- низкое качество яйцеклеток, полученных во время короткого протокола.
Короткий протокол

Короткий протокол ЭКО совпадает с естественным менструальным циклом. Его главное отличие от длинного в том, что нет регулирующей фазы – начинают сразу со стимуляции суперовуляции. Весь протокол занимает 4 недели (25–32 дней), а гормональная стимуляция продолжается 10–12 дней.
Стимуляцию начинают на 3–5-й день менструального цикла. Проводят ультразвуковое исследование, чтобы убедиться, что слизистая оболочка матки истончилась после менструации, затем женщина начинает получать препараты фолликулостимулирующего гормона. Одновременно назначают агонисты ГнРГ, обычно в виде спрея для носа. В процессе стимуляции женщина каждые 2–3 дня проходит контрольные УЗИ и сдает анализы на гормоны.
Показатели того, что стимуляция прошла успешно в короткой фазе:
- средний размер фолликулов более 18 мм;
- толщина слизистой оболочки матки более 8 мм;
- уровень прогестерона увеличился в три раза по сравнению с начальным значением.
После этого можно вводить ХГЧ и переходить к сбору ооцитов.
Преимущества короткого протокола
В ходе короткого протокола женщина получает меньше препаратов, снижается стоимость гормональной стимуляции. Ниже риск развития синдрома гиперстимуляции яичников.
Недостаток короткого протокола в том, что во время него удается получить меньшее количество ооцитов. Фолликулы могут созревать в разное время, может произойти преждевременная лютеинизация.
В каких случаях применяют короткий протокол?
Этой схеме отдают предпочтение в следующих случаях:
- возраст женщины старше 35 лет;
- высокий риск синдрома гиперстимуляции яичников;
- синдром поликистозных яичников;
- отсутствие ответа или низкое качество яйцеклеток в длинном протоколе;
- желание женщины снизить продолжительность гормональной стимуляции и риск побочных эффектов.
Как видите, однозначного ответа на вопрос о том, какой протокол ЭКО лучше – длинный или короткий – нет. Тут нужен индивидуальный подход, важно учитывать некоторые нюансы. Оптимальный выбор поможет сделать врач после консультации и обследования. Важно найти хорошего репродуктолога, который предоставит всю необходимую информацию, подробно опишет плюсы и минусы. Современные гормональные препараты, оптимальный выбор их дозировок и схем введения делают гормональную стимуляцию максимально безопасной процедурой.
ЭКО может протекать по нескольким сценариям. Длинный протокол ЭКО имеет продолжительность не менее 40 дней (35-50). При его использовании посредством специальных препаратов полностью останавливается естественная выработка половых гормонов и создается искусственный гормональный фон, необходимый для роста яйцеклеток.
Преимущества и недостатки длинного протокола ЭКО
В ходе длинного протокола ЭКО врач имеет возможность полностью контролировать рост и развитие фолликулов и получить большое количество качественных яйцеклеток. Это и есть основное преимущество данной медицинской технологии. К минусам длинного протокола ЭКО можно отнести:
- невозможность его использования для пациенток старше 30 лет;
- нарушения менструального цикла;
- высокий риск развития синдрома гиперстимуляции яичников;
- психологический и физический дискомфорт пациенток – женщины испытывают жар, приливы, насыщенная и долгая терапия может вызвать стресс, раздражительность, упадок сил.
Окончательное решение о необходимости длинного протокола ЭКО принимает врач.
Показания к применению
Длинный протокол ЭКО используют при:
- миоме – доброкачественное новообразование в полости матки;
- избыточной массе тела, ожирении;
- синдроме поликистозных яичников – состояние, при котором в яичниках образуются множественные кисты;
- возрасте пациентки до 30 лет;
- эндометриозе – заболевание, при котором клетки эндометрия разрастаются за пределы полости матки;
- гиперандрогении – повышенной выработке мужских половых гормонов;
- ситуации, когда в ходе короткого протокола были получены яйцеклетки низкого качества.
Этапы длинного протокола ЭКО
- подавление работы гипофиза и яичников;
- стимуляцию суперовуляции;
- пункцию яичника;
- оплодотворение и выращивание эмбрионов;
- подсадку эмбрионов в полость матки, гормональную поддержку беременности.
На 19-21 день цикла женщине вводят гормональный препарат, прекращающий синтез гонадотропных гормонов в гипофизе и женских половых гормонов в яичниках. Затем наступает фаза суперовуляции, которая длится около 2 недель. Все это время женщина принимает строго по инструкции врача указанные препараты. С 5 дня регулярно проводится УЗИ (таким образом контролируется рост фолликулов) и тестируется уровень эстрадиола в крови. Если по истечении двух недель размер фолликул и уровень эстрадиола не соответствуют желаемым показателям, гормонотерапию продляют. Далее пациентке вводится стимулирующий выход яйцеклетки препарат. Через 36 часов производится пункция яичников. Огромное значение в длинном протоколе ЭКО придается временным промежуткам и точности выполнения необходимых манипуляций. Женщине расписывают буквально каждый день и даже час приема препаратов, и она должна неукоснительно придерживаться этого плана. Огромное значение имеет правильное определение времени пункции: если забор материала произвести раньше срока, фолликулы окажутся пустыми, позже – яйцеклетки станут непригодными для оплодотворения. В указанный день пункции женщина должна приехать в клинику вовремя и подготовленной: рекомендуется воздержаться от приема пищи, за два часа лучше не пить, так как процедура проходит под наркозом. В это же время супруг должен сдать сперму. После выполнения пункции женщина некоторое время находится в клинике, после чего ее отпускают домой. Возможно ухудшение самочувствия, головокружение, тошнота, боли внизу живота, небольшие кровянистые выделения. В течение суток неприятные симптомы постепенно проходят.
Взятые в ходе пункции яйцеклетки и полученная сперма используются для выращивания эмбрионов в лабораторных условиях. После культивирования в течение 3-5 дней производится подсадка эмбрионов в матку; женщине назначают поддерживающую гормональную терапию. Через 2 недели выполняется анализ крови на ХГЧ, по результатам которого определяют наступление/ненаступление беременности.
Вся информация носит ознакомительный характер. Если у вас возникли проблемы со здоровьем, то необходима консультация специалиста.
Читайте также:

