При каких условиях дрожжи осуществляют глицериновую форму спиртового брожения
Обновлено: 04.07.2024
Наряду с главными продуктами брожения - спиртом и углекислым газом - образуются и вторичные продукты.
К числу вторичных продуктов относятся глицерин (г), янтарная кислота (я), уксусная кислота (у), ацетальдегид (а), 2,3-бутиленгликоль (б), ацетоин (ац), лимонная кислота (л), пировиноградная кислота (п), изоамиловый спирт (и), изопропиловый спирт (пр), эфиры.
В. 3. Гваладзе и Л. Женевуа было выведено уравнение, выражающее зависимость между отдельными компонентами вторичных продуктов спиртового брожения: г=п+а+2у+5я+2ац+б+9л+3и+3пр.
Если учесть только основные компоненты, то уравнение можно упростить: г=п+а+2у+5я+б+2ац+9л.
Сумма вторичных продуктов составляет в среднем 80-92% от содержания глицерина.
Образование глицерина может быть объяснено, исходя из второй формы брожения Нейберга, называемой глицеропировиноградным брожением. Эта форма предусматривает брожение глюкозы в присутствии гидросульфита натрия, который связывает уксусный альдегид, выключая его из дальнейших реющий. Его место занимает 3-фосфоглицериновый альдегид, который, восстанавливаясь водородом, полученным от НАД•Н2, превращается в 1-глицерофосфат:
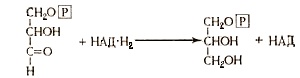 | ||||
| 3-Фосфоглицериновый альдегид | 1-Глицерофосфат | |||
1-Глицерофосфат дефосфорилируется при участии фосфатазы, образуя глицерин.
Другим путем образования глицерина является третья форма брожения Нейберга в щелочной среде. По этой форме вместо этилового спирта образуется глицерин.
Образование уксусной кислоты объясняется окислением уксусного альдегида кислородом воды:
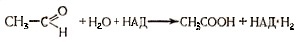
В дальнейшем путем конденсации двух молекул уксусной кислоты образуется янтарная кислота (реакция Тунберга):
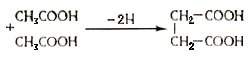
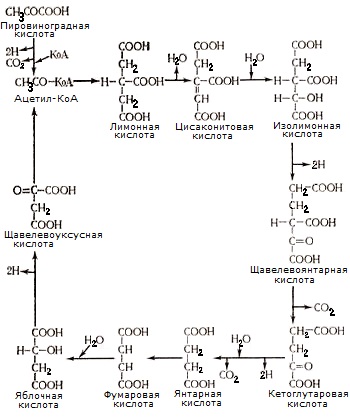
Янтарная кислота, дегидрируясь, образует фумаровую кислоту, которая путем гидратации превращается в яблочную кислоту; последняя дегидрируется в щавелевоуксусную кислоту. Щавелевоуксусная кислота, конденсируясь с новой молекулой ацетил-КоА, образует лимонную кислоту. Следовательно, образование лимонной кислоты связано с циклом Кребса, или циклом трикарбоновых кислот:
Образование молочной кислоты при спиртовом брожении происходит путем восстановления пировиноградной кислоты в присутствии НАД•Н2: СН3–СО–СООН+НАД•Н2 → → СН3–СНОН–СООН+НАД.
Уксусный альдегид образуется из сахара при нормальном спиртовом брожении. Он может также образовываться за счет окисления этилового спирта алкогольдегидрогеназой в присутствии НАД:

Уксусный альдегид образуется также за счет дезаминирования аминокислот.
Вновь полученный ацетальдегид претерпевает различные превращения:
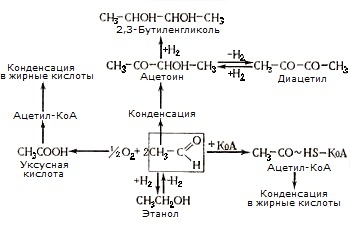
Высшие спирты синтезируются дрожжами в процессе брожения. В их состав входит около 50 высших спиртов, образующих 90-95% сивушного масла. Главными компонентами являются изоамиловый, изобутиловый и н -пропиловый спирты, составляющие 85-93%.
Высшие спирты синтезируются следующим путем:
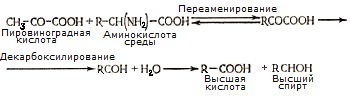
Образование вторичных продуктов происходит неравномерно в процессе спиртового брожения.
Так, накопление глицерина наиболее интенсивно в начале спиртового брожения, пока в среде мало ацетальдегида. Всего в этот период используется 6-7% сахара, в том числе 2,5,% на образование глицерина.
Содержание ацетальдегида быстро возрастает в первый период брожения (до 100-150 мг/л), после чего устанавливается равновесие между его образованием и расходованием.
Уксусная кислота образуется более интенсивно в начале брожения. Это объясняется возрастом дрожжей: молодые дрожжи образуют больше уксусной кислоты, чем старые.
На соотношение между вторичными продуктами брожения влияют аэрация, рН среды, температура брожения, первоначальный состав сусла. Образование янтарной кислоты возрастает при аэрации сусла и уменьшается в анаэробных условиях. Наоборот, образование уксусной кислоты, 2,3-бутиленгликоля и ацетоина возрастает в анаэробных условиях и уменьшается при аэрации сусла.
При рН>3,0 увеличивается интенсивность глицеропировиноградного брожения, что приводит к уменьшению выхода этилового спирта. С увеличением рН образование глицерина, а также уксусной и янтарной кислот возрастает. При этом янтарной кислоты образуется меньше, чем уксусной.
При рН 14 С, показали способность винных дрожжей использовать вторичные продукты брожения. При этом оказалось, что наиболее интенсивно они используют уксусную кислоту, ацетальдегид и этиловый спирт, менее энергично молочную кислоту, углекислый газ и янтарную кислоту и наименее энергично - глицерин. При этом из уксусной кислоты и уксусного альдегида образуются этиловый спирт, янтарная, фумаровая и гликолевая кислоты, 2,3-бутиленгликоль и глицерин и совсем не образуются молочная и яблочная кислоты.
По данным С. В. Дурмишидзе, некоторые вторичные продукты брожения (ацетальдегид, уксусная и янтарная кислоты, а также этиловый спирт) могут частично превращаться в трегалозу дрожжей, которая в свою очередь подвергается эндогенным (внутриклеточным) превращениям. При размножении и росте дрожжей ацетальдегид, этиловый спирт, уксусная и янтарная кислоты включаются в аминокислоты, а впоследствии и в белки. Это свидетельствует о важной роли вторичных продуктов в обмене веществ дрожжевой клетки. Правильным выбором расы дрожжей и регулированием аэрации, температуры и других условий можно обеспечить оптимальное соотношение вторичных продуктов в вине.
Спиртовое брожение – микробиологический процесс превращения углеводов в спирт и углекислый газ. Вызывается аскомицетовыми дрожжами рода Saccharomyces, некоторыми бактериями и отдельными представителями мукоровых грибов.
Суммарное уравнение реакции:
С 6 H 12 O 6 → 2 СНзCH 2 ОН + 2 СО 2 + Е
глюкоза этиловый спирт
Как и любое брожение, это сложный многоступенчатый процесс (см. раздел 7.3), который протекает при участии комплекса ферментов. Наряду со спиртом, могут образовываться побочные продукты: глицерин, уксусный альдегид, уксусная, яблочная кислоты, сивушные масла (смесь высших кислот).
Основными возбудителями спиртового брожения являются дрожжи – сахаромицеты.
Это факультативно-анаэробные микроорганизмы. В аэробных условиях дрожжи получают энергию путем полного окисления моно- и дисахаридов до углекислого газа и воды, т.е. путем аэробного дыхания. При этом интенсивно накапливается биомасса (эффект Пастера). Поэтому производство хлебопекарных дрожжей ведут в аэробных условиях. Ацидофилы. Мезофилы.
Естественным местообитанием дрожжей является поверхность плодов и ягод, сок и поверхность листьев, нектар, вода, почва, кожные покровы и пищеварительный тракт людей и животных.
Условия проведения спиртового брожения
1. Источники питания. В качестве источника углерода используют глюкозу, фруктозу, сахарозу, мальтозу. Крахмал дрожжи не сбраживают, так как амилолитические ферменты у них отсутствуют. Поэтому крахмалсодержащее сырье подвергают осахариванию при участии амилаз различного происхождения. Концентрация сахара 10–15% наиболее благоприятна для большинства дрожжей. В качестве источника азота используются аммонийные соли органических кислот и аминокислоты.
2. Анаэробные условия.
3. Температура. По отношению к температуре сахаромицеты делятся на низовые и верховые дрожжи. Дрожжи верхового брожения вызывают бурное и быстрое брожение при температуре 20–28 °С. При этом они всплывают на поверхность под действием выделяющегося диоксида углерода. Низовые дрожжи осуществляют более спокойное брожение, которое ведут при 5–10 °С.
4. Концентрация этилового спирта. Этиловый спирт, накапливающийся в среде, оказывает неблагоприятное действие на дрожжи. Угнетающее действие спирт оказывает уже при концентрации в среде 2–5 % об., а при 12–15 % об. брожение прекращается.
5. Активная кислотность среды (рН). Спиртовое брожение протекает в кислой среде (рН 4–4,5). При подщелачивании среды до рН 8 дрожжи в качестве основного продукта брожения накапливают не спирт, а глицерин. Это так называемая глицериновая форма спиртового брожения:
2С 6 Н 12 0 6 → 2CН 2 0HCHOHСН 2 0Н+СНзСН 2 0Н+СНзСООН+2С0 2 + Е
глюкоза глицерин этиловый уксусная
Практическое использование спиртового брожения
Спиртовое брожение лежит в основе производства этилового спирта, пива, вина, используется в хлебопечении. Совместно с молочнокислым брожением оно используется при производстве кваса, кефира, кумыса. Основными потребителями этилового спирта являются пищевая и химическая промышленность, а также медицина.
11.2 Молочнокислое брожение: гомо- и гетероферментативное.
Химизм процесса. Характеристика молочнокислых бактерий. Практическое значение молочнокислого брожения
Молочнокислое брожение – процесс превращения углеводов молочнокислыми бактериями в молочную кислоту.
Возбудители молочнокислого брожения подразделяются на 2 группы:
гомоферментативные и гетероферментативные, которые, в свою очередь, вызывают гомоферментативное и гетероферментативное молочнокислое брожение. В основу этого деления положены конечные продукты, образуемые при гомо- и гетероферментативном молочнокислом брожении.
Гомоферментативное молочнокислое брожение и его возбудители. При гомоферментативном молочнокислом брожении образуется преимущественно молочная кислота.
С 6 H 12 О 6 → 2 СНзСНОНСООН + Е
глюкоза молочная кислота
К гомоферментативным молочнокислым бактериям относятся молочнокислые стрептококки: Streptococcus lactis, Streptococcus cremoris, Streptococcus thermophilus, а также молочнокислые палочки: Lactobacillus delbrueckii, Lactobacillus acidophilus, Lactobacillus bulgaricus, Lactobacillus ptantarum.
Гетероферментативное молочнокислое брожение и его возбудители. Конечными продуктами при этом брожении являются не только молочная кислота, но и побочные продукты: уксусная кислота, этиловый спирт, янтарная кислота, диоксид углерода, водород. Суммарное уравнение процесса имеет вид:
С 6 H 12 О 6 → СНзСНОНСООН + СООНСН 2 СН 2 СООН + СНзСООН +
глюкоза молочная кислота янтарная кислота уксусная кислота
+СНзСН 2 ОН + C0 2 +Н 2 +Е
К гетероферментативным молочнокислым бактериям относятся бактерии рода Streptococcus: Streptococcus diacetilactis, Streptococcus acetoinicus; бактерии рода Lactobacillus: Lactobacillus brevis, Lactobacillus helveticus, а также бактерии рода Leuconostoc: Leuconostoc mesenteroides, Leuconostoc cremoris.
Характеристика молочнокислых бактерий
Все молочнокислые бактерии грамположительные, факультативные анаэробы. Среди молочнокислых бактерий есть мезофилы (предпочитают температуру около 30 °С) и термофилы (Streptococcus thermophilus, Lactobacillus bulgaricus), оптимальной температурой для которых является температура около 40–50 °С.
Молочнокислые бактерии отличает высокая требовательность к питательной среде: они нуждаются в полном наборе готовых аминокислот, в витаминах группы В 12 , в компонентах нуклеиновых кислот, что и определяет их распространение в природе.
Молочнокислые бактерии обитают в основном на растениях, плодах, овощах, в желудочно-кишечном тракте, в молоке и молочных продуктах, а также в местах разложения растительных остатков.
В качестве источника углерода используют лактозу, мальтозу.
Оптимальное значение рН для развития молочнокислых бактерий около 4. Молочнокислые бактерии образуют от 1 до 3,5 % молочной кислоты.
Практическое значение молочнокислого брожения
Оно находит широкое применение при изготовлении кисломолочных продуктов, сливочного масла, маргарина, используется в хлебопечении, при квашении овощей, силосовании кормов и производстве молочной кислоты.
Многие мезофильные гетероферментативные молочнокислые бактерии и лейконосток являются вредителями в производстве спирта, пива, вина, безалкогольных напитков, сахара и др.
11.3 Пропионовокислое брожение. Химизм процесса, возбудители. Практическое использование пропионовокислого брожения
Пропионовокислое брожение вызывается пропионовокислыми бактериями, относящимися к роду Propionibacterium.
Единственным источником энергии для пропионовокислых бактерий является процесс сбраживания различных веществ: моносахаридов (гексоз, пентоз), молочной, яблочной кислот, глицерина и других в пропионовую и уксусную кислоту, диоксид углерода и воду.
Химизм пропионовокислого брожения:
ЗС 6 H 12 О 6 → 4СНзCH 2 СООН + 2СНзСООН + 2CO 2 + 2H 2 O +Е
глюкоза пропионовая уксусная
Пропионовокислые бактерии – небольшие, неподвижные грамположительные палочки, не образующие спор, факультативные анаэробы. Обитают в основном в кишечном тракте жвачных животных и в молоке.
Практическое применение пропионовокислого брожения
У пропионовокислых бактерий обнаружена способность к активному синтезу витамина В 12 , поэтому они используются в качестве продуцента в микробиологической промышленности для получения этого витамина.
11.4 Маслянокислое брожение. Химизм процесса. Возбудители. Практическое использование и роль в процессах порчи пищевых продуктов
Маслянокислое брожение – анаэробное окисление органических веществ маслянокислыми бактериями в масляную кислоту.
С 6 H 12 О 6 → СНзСН 2 СН 2 СООН + 2 С0 2 + 2Н 2 +Е
глюкоза масляная кислота
Возбудители маслянокислого брожения
Маслянокислые бактерии относятся к роду Clostridium. Это крупные, подвижные грамположительные палочки, образующие устойчивые споры, при образовании которых клетка приобретает форму веретена или теннисной ракетки, облигатные (строгие) анаэробы.
Маслянокислые бактерии широко распространены в природе. Обитают там, где много органических веществ и нет доступа воздуха – в иловых отложениях водоемов, навозе, почве и т.д.
Эти бактерии могут сбраживать многие углеводы, в т.ч. (крахмал, гликоген, пектиновые вещества, целлюлозу), спирты (этиловый, маннит, глицерин) и аминокислоты. По характеру используемых субстратов маслянокислые бактерии делятся на две группы: сахаролитические клостридии, которые сбраживают в основном углеводы (Ctostridium butyricum), и протеопитические клостридии, которые разлагают белки и пептоны до аминокислот и затем их сбраживают (Clostridium sporogenes, Clostridium subterminalis, Clostridium perfringens, Clostridium botulinum).
Практическое значение маслянокислого брожения. Маслянокислое брожение используется в промышленности для получения масляной кислоты (продуцент Clostridium butyricum). Хотя масляная кислота обладает резким, неприятным запахом прогорклого масла, ее эфиры отличаются приятным ароматом: метиловый эфир имеет яблочный запах, этиловый – грушевый, амиловый – ананасный. Эфиры масляной кислоты используют в кондитерской, безалкогольной, парфюмерной промышленности.
Маслянокислые бактерии участвуют в круговороте веществ в природе. С другой стороны, маслянокислые бактерии могут вызвать массовую гибель картофеля и овощей, вспучивание сыров, порчу консервов, прогоркание масла и маргарина, увлажненной муки и других продуктов, чем наносят большой урон народному хозяйству. Борьба с маслянокислыми бактериями затруднена из-за высокой устойчивости спор.
11.5 Уксуснокислое брожение. Химизм процесса. Возбудители. Практическое использование и роль в процессах порчи пищевых продуктов
Уксуснокислое брожение – аэробное окисление углеводов и спирта уксуснокислыми бактериями в уксусную кислоту. Таким образом, это брожение относится к неполным окислениям или окислительным брожениям. Суммарное уравнение процесса имеет вид:
С 6 H 12 O 6 + 2 0 2 → 2СНзСООН + 2CO 2 + 2Н 2 0 + Е или
глюкоза уксусная кислота
СНзСН 2 ОН + O 2 → СНзСООН + Н 2 О + Е
этиловый спирт уксусная кислота
Возбудителями уксуснокислого брожения являются уксуснокислые бактерии, относящиеся к двум родам: Gluconobacter и Acetobacter. Это короткие, подвижные грамотрицательные палочки, не образующие спор. Оптимальная температура развития – 30˚ С. Бактерии кислотоустойчивы, оптимальное значение рН для развития 5,4–6,3. Обитают на цветах, зрелых фруктах, ягодах, овощах, в прокисших соках, пиве, вине, квашенных овощах.
Практическое значение уксуснокислого брожения
Используется в промышленности для получения натурального спиртового уксуса (продуцент Acetobacter aceti). Кроме того, производят также винный уксус (из вина) и яблочный уксус (из яблочного сока).
С другой стороны, уксуснокислые бактерии являются вредителями спиртового, пивоваренного, консервного производств, виноделия, производства безалкогольных напитков
11.6 Окисление жиров и высших жирных кислот микроорганизмами. Микроорганизмы - возбудители порчи жиров
Жиры представляют собой сложные эфиры глицерина и высших жирных кислот.
Так как жиры – высокомолекулярные соединения, то в неизменном виде внутрь клетки они попасть не могут. Поэтому вначале происходит гидролиз жира при участии фермента липазы, которая имеется у многих микроорганизмов. В результате образуются глицерин и высшие жирные кислоты. Этот процесс не обеспечивает клетки энергией, поэтому образовавшиеся продукты гидролиза используются различными микроорганизмами в качестве энергетического материала. Процесс протекает только в аэробных условиях.
Глицерин подвергается окислению уксуснокислыми бактериями до диоксиацетона и далее микроскопическими грибами до углекислого газа и воды.
Высшие жирные кислоты окисляются труднее и медленнее. В процессе окисления образуются промежуточные продукты: кетоны, альдегиды, оксикислоты и др., которые придают окисленному жиру прогорклый вкус.
Возбудители. Наиболее активными микроорганизмами в процессе разложения жира являются бактерии рода Pseudomonas, особенно флуорисцирующие (продуцирующие пигменты) и мицелиальные грибы: Oidium lactis, многие виды Aspergillus, Penicillium.
Практическое значение процесса
Процесс разложения жиров отмерших животных и растений происходит постоянно и имеет большое значение в круговороте веществ в природе.
С другой стороны, в пищевой промышленности микроорганизмы, окисляющие жиры, приносят вред, вызывая порчу пищевых жиров и жира, содержащихся в различных пищевых продуктах.
Следует учитывать, что многие жирорасщепляющие микроорганизмы являются психрофилами, поэтому способны развиваться при хранении пищевых продуктов в охлажденном состоянии.
11.7 Гнилостные процессы. Понятие об аэробном и анаэробном гниении. Возбудители. Роль гнилостных процессов в природе, в пищевой промышленности
Гниение – процесс глубокого разложения белковых веществ. Одним из конечных продуктов разложения белковых веществ является аммиак, поэтому процесс гниения называют аммонификацией.
Белки – высокомолекулярные соединения, поэтому вначале они подвергаются внеклеточному расщеплению протеолитическими ферментами микроорганизмов, которые являются экзоферментами.
Расщепление белков происходит ступенчато:
белки → пептоны → полипептиды → аминокислоты.
Образовавшиеся аминокислоты диффундируют внутрь клеток и могут быть использованы как в конструктивном, так и в энергетическом обмене.
Расщепление аминокислот начинается путем их дезаминирования и декарбоксилирования. При дезаминировании аминокислот происходит отщепление аминогруппы с образованием аммиака, органических кислот (масляной, уксусной, пропионовой, окси- и кетокислот) и высокомолекулярных спиртов.
В дальнейшем образование конечных продуктов зависит от условий протекания процесса и от вида микроорганизма – возбудителя гниения.
Аэробное гниение. Протекает в присутствии кислорода воздуха. Конечными продуктами аэробного гниения являются, кроме аммиака, диоксид углерода, сероводород и меркаптаны (обладающие запахом тухлых яиц). Сероводород и меркаптаны образуются при разложении серосодержащих аминокислот (цистина, цистеина, метионина).
Анаэробное гниение. Протекает в анаэробных условиях. Конечными продуктами анаэробного гниения являются продукты декарбоксилирования аминокислот (отнятие карбоксильной группы) с образованием дурно пахнущих веществ: индола, акатола, фенола, крезола, диаминов (их производные являются трупными ядами и могут вызывать отравления).
Возбудители гнилостных процессов
Возбудителями аэробного гниения являются спорообразующие бактерии рода Bacillus: Bacillus mycoides (грушевидная бацилла); Bacillus megaterium (капустная бацилла); Bacillus mesentericus (картофельная палочка); Bacillus subtilis (сенная палочка), а также неспорообразующие палочки: Serrate marcencens (чудесная палочка); Proteus vulgaris (палочка протея); Escherichia coli (кишечная палочка) и другие микроорганизмы.
Возбудителями анаэробного гниения являются анаэробные споровые папочки рода Clostridium (протеолитические клостридии): Clostridium sporogenes, Clostridium subterminalis, Clostridium perfringens, Clostridium botulinum.
Практическое значение гнилостных процессов
Гнилостные микроорганизмы нередко наносят большой ущерб народному хозяйству, вызывая порчу богатых белками продуктов питания: мяса и мясопродуктов, яиц, молока, рыбы и рыбопродуктов и др.
В природе (в воде, почве) гнилостные бактерии активно разлагают отмершие животные и растительные ткани, минерализуют белковые вещества и тем самым играют важную роль в круговороте углерода и азота.
Вопросы для самопроверки
1. Каков химизм спиртового брожения?
2. Каковы условия нормального протекания спиртового брожения?
3. Чем отличаются дрожжи верхового брожения от дрожжей низового брожения?
4. При каких условиях дрожжи осуществляют глицериновую форму спиртового брожения?
5. Охарактеризуйте возбудителей молочнокислого брожения.
6. В чем отличие гомоферментативного молочнокислого брожения от гетероферментативного?
Какие гомоферментативные молочнокислые бактерии Вы знаете?
Какие гетероферментативные молочнокислые бактерии Вы знаете?
Где в природе встречаются молочнокислые бактерии?
Охарактеризовать практическое значение молочнокислого брожения в пищевой промышленности, в природе.
11. Каково практическое значение пропионовокислого брожения?
12. Какие микроорганизмы являются возбудителями пропионовокислого брожения?
13. Охарактеризуйте возбудителей маслянокислого брожения.
14. На какие группы делятся маслянокислые бактерии?
15. Охарактеризуйте уксуснокислое брожение.
16. Какие микроорганизмы являются возбудителями уксуснокислого брожения?
17. Каким образом микроорганизмы окисляют жиры и жирные кислоты?
18. В чем сущность гнилостных процессов?
19. Какие продукты образуются при аэробном и гниении?
20. Укажите возбудителей анаэробного гниения.
21. В чем заключается эффект Пастера?
22. Назовите конечные продукты гетероферментативного молочнокислого брожения.
23. Где обитают пропионовокислые бактерии?
24.Какие конечные продукты образуются при анаэробном гниении?
25.Какова роль маслянокислых бактерий в природе, в пищевой промышленности?
26. Назовите конечные продукты пропионовокислого брожения.
27. Что образуется в результате окисления микроорганизмами жиров и высших жирных кислот?
1. Шлегель Г. Общая микробиология. – М.: Мир, 1987. – 500 с.
2. Чурбанова И.Н. Микробиология. – М.: Высшая школа, 1987.
3. Мудрецова-Висс К.А., Кудряшова А.А., Дедюхина В.П. Микробиология, санитария и гигиена – Владивосток: Изд-во ДВГАЭУ, 1997. – 312 с.
4. Асонов Н.Р. Микробиология. 3 изд., перераб. и доп.– М.: Колос, 1997. – 352 с.
5. Вербина Н.М., Каптерева Ю.В. Микробиология пищевых производств. – М.: Агропромиздат, 1988. – 256 с.
Похожие документы:
Основная образовательная программа высшего профессионального образования по направлению подготовки 020400 Биология (3)
Основная образовательная программа высшего профессионального образования Направление подготовки 111900
Первая. Общая микробиология. Глава место микроорганизмов среди
Зрительное восприятие объектов окружающего мира является одним из наиболее важных способов его познания Однако, человеческий глаз видит объекты величиной около 0,1 мм, а различает детали в объектах размером не менее 1 мм В то же
Основная профессиональная образовательная программа (2)
1.1. Специальность утверждена Приказом Министерства образования Российской Федерации от 02.07.2001 № 2572 «Об утверждении Государственного образовательного стандарта среднего профессионального образования - Классификатора специальностей
Урок окружающего мира с применением икт по теме "Почва, её состав и свойства" (3-й класс)
- Прочитайте заголовок. Как вы думаете, о какой кладовой идёт речь? Что означают картинки? Приведите свои примеры из жизни. (Сажаем в землю весной 1 ведро картошки, а собираем 20 вёдер.
Продукты брожения известны человеку с незапамятных времен, хотя истинная причина этого явления была установлена Л. Пастером только в 1861 г. Он открыл три основных типа брожений: спиртовое, молочнокислое и маслянокислое.
Брожение — это анаэробный метаболический процесс, при котором образуется АТФ, а продукты расщепления органического субстрата являются как донорами, так и акцепторами водорода окисляемого субстрата.
При сбраживании углеводов и ряда других веществ могут накапливаться такие продукты метаболизма, как спирт, молочная, пропионовая, муравьиная или масляная кислота и др. В зависимости от того, какие продукты преобладают или являются характерными, различают спиртовое, молочнокислое, пропионовокислое, маслянокислоое, муравьинокислое брожение. Микроорганизмы, осуществляющие брожение, являются либо строгими, либо факультативными анаэробами.
9.5.1. Спиртовое брожение
Сбраживание углеводов микроорганизмами с образованием этилового спирта и диоксида углерода составляет сущность спиртового брожения. Спиртовое брожение осуществляют дрожжи сахаромицеты, мукоровые грибы и некоторые виды бактерий (Zymomonas mobilis, Sarcina ventricula и др.).
Процесс спиртового брожения суммарно можно выразить следующим уравнением:

Спиртовое брожение протекает по фруктозодифосфатному пути (гликолитический путь Эмбдена—Мейергофа—Парнаса) (рис. 28).

Рис. 28. Схема спиртового брожения. Ферменты, участвующие в осуществлении спиртового брожения:
Ф1 — гексокиназа; Ф2 — глюкозофосфатизомераза; Ф3 — фосфофруктокиназа; Ф4 — фруктозо-1,6-дифосфатальдолаза; Ф5 — триозофосфатизомераза; Ф6 — 3-фосфоглицеральдегидцегидрогеназа; Ф7 — фосфоглицераткиназа; Ф8 — фосфоглицеромутаза; Ф9 — енолаза; Ф10 — пируваткиназа; Ф11 — пируватдекарбоксилаза; Ф12 — алкогольдегидрогеназа; Ф13 — глицерол-3-фосфатдегидрогеназа; Ф14 — глицеролфосфатаза
На первой стадии брожения происходит фосфорилирование глюкозы при участии АТФ, изомеризация глюкозо-6-фосфата во фруктозо-6-фосфат, который, в свою очередь, фосфорилируется в положении 1. Затем образовавшийся фруктозо-1,6-дифосфат расщепляется под действием фермента альдолазы (ключевого фермента гликолитического пути) на две триозы: глицеральдегид-3-фосфат и дигидроксиацетонфосфат, которые легко превращаются друг в друга при участии фермента триозофосфатизомеразы. Таким образом, первый этап гликолиза характеризуется активированием одной молекулы глюкозы с затратой энергии в виде 2 молекул АТФ.
На второй стадии брожения глицеральдегид-3-фосфат окисляется до 1,3-дифосфоглицериновой кислоты при участии НАД + и неорганического фосфата. В последующих реакциях превращения 1,3-дифосфоглицериновой кислоты в пируват обе фосфатные группы переносятся на АДФ ( субстратное фосфорилирование), в результате чего образуются 4 молекулы АТФ. Поскольку на начальных этапах активирования глюкозы затрачивается 2 молекулы АТФ, общий выход составляет 2 молекулы АТФ на один моль сброженной глюкозы.
Центральный метаболит гликолитического пути — пируват — подвергается реакции декарбоксилирования под действием пируватдекарбоксилазы — ключевого фермента спиртового брожения. Образовавшийся при этом ацетальдегид становится акцептором водорода окисляемого субстрата и восстанавливается до этанола при помощи фермента алкогольдегидрогеназы. Биологическое значение последней реакции заключается в окислении восстановленного НАДН2, образовавшегося ранее.
Сбраживание глюкозы до этанола и СО, обычно происходит в слабокислой среде при pH 4—5,5 (первая форма брожения по Нойбергу).
К. Нойберг обнаружил, что в зависимости от условий при спиртовом брожении могут образовываться нехарактерные для этого процесса продукты. Так, если к дрожжам, сбраживающим глюкозу, добавить бисульфит (NaHSO3), то последний образует комплекс с ацетальдегидом:

Поскольку ацетальдегид заблокирован, он уже не может выполнять роль акцептора водорода, в результате чего водород от НАДН2 передается на дигидроксиацетонфосфат. Этот метаболит восстанавливается до глицерол-3-фосфата и дефосфорилируется с образованием глицерина, как это показано на схеме (рис. 27). Это вторая (глицериновая) форма спиртового брожения по Нойбергу:

Если спиртовое брожение проводить в щелочной среде (например, в присутствии NaHCO3), то также происходит накопление глицерина. Это объясняется тем, что ацетальдегид в щелочных условиях не может являться акцептором водорода окисляемого субстрата, поскольку участвует в реакции дисмутации с образованием этанола и уксусной кислоты. Поэтому акцептором электронов, как и в предыдущем случае, служит дигидроксиацетонфосфат. Процесс брожения в щелочной среде называют смешанной формой спиртового брожения (третья форма брожения по Нойбергу), которую можно представить в виде уравнения:

Дрожжи относятся к аэробным микроорганизмам, но расщепление глюкозы они осуществляют в анаэробных условиях, при этом спиртовое брожение идет очень интенсивно, хотя роста дрожжей почти не происходит.
Спиртовое брожение лежит в основе таких биотехнологических процессов, как производство этилового спирта и глицерина, виноделие, пивоварение, хлебопечение. В некоторых кисломолочных напитках (кефир, кумыс, курунга, мацони) спиртовое брожение осуществляют дрожжи, способные сбраживать молочный сахар.
Производство этилового спирта. Этанол широко применяется в пищевой промышленности, в медицине, парфюмерии, в химической промышленности в качестве растворителя, антифриза, реагента, как топливо для ракетных двигателей и т. д.
В зависимости от используемого сырья этанол подразделяют на пищевой и технический. Для производства пищевого этилового спирта используют растительное сырье, богатое крахмалом (картофель, зерно, отходы крахмало-паточного производства), инулином (топинамбур, корни цикория), а также отходы сахарного производства (меласса) и виноделия. Технический спирт получают из гидролизатов древесины и отходов сельскохозяйственных растений.
Процесс производства спирта из крахмалсодержащего сырья включает следующие операции:
Очистка сырья → Измельчение и разваривание сырья → Осахаривание → Сбраживание осахаренной массы → Фильтрация и перегонка.
В основе производства этилового спирта из картофеля и зерна злаков лежат два биохимических процесса: гидролиз (осахаривание) крахмала, содержащегося в сырье, с помощью амилолитических ферментов, и сбраживание образующихся сахаров дрожжами до спирта и диоксида углерода. Амилолитические ферменты продуцируют грибы видов Aspergillis awamori, A. orizae, A. niger и др. Основу осахаренной массы (затора) составляют углеводы: мальтоза, глюкоза, декстрины. Кроме того, в ней содержатся продукты распада белка (пептиды, аминокислоты), необходимые для азотного питания дрожжей. В затор вносят и дополнительные источники питания, в результате чего получают питательную среду для осуществления спиртового брожения.
Если в качестве сырья используется меласса, то осахаривание не проводят, так как она содержит углеводы в готовой для брожения форме. Мелассу осветляют, разбавляют водой в необходимом соотношении, чтобы получить оптимальную концентрацию сахара.
В подготовленную среду вносят дрожжи и проводят брожение. Возбудителями брожения являются дрожжи вида Saccharomyces cerevisiae. Спиртовые дрожжи должны обладать высокой бродильной активностью, быть устойчивыми к высокому содержанию спирта в культуральной среде и к инфекции. Они должны также обладать способностью расщеплять некоторые олигосахариды (в частности мальтозу) до глюкозы.
При сбраживании сусла из крахмалсодержащего сырья применяют дрожжи S. cerevisiae штамм XII, выделенные из хлебопекарных прессованных дрожжей в 1902 г. Они хорошо сбраживают мальтозу, сахарозу, но не сбраживают конечные декстрины. Проведена селекция термотолерантных дрожжей, позволяющих ускорить процесс выращивания производственных дрожжей и сбраживания сусла из крахмалсодержащего сырья, частично гидролизовать и сбраживать конечные декстрины, увеличить выход спирта. В результате селекции получены термотолерантные штаммы дрожжей 985-Т и 717. Новый селекционированный штамм дрожжей 985-Т устойчив к повышению температуры до 38 °С и концентрации СВ в питательной среде до 30 %. Получен осмофильный штамм 987-0, устойчивый к высоким концентрациям сусла, но не обладающий термотолерантными свойствами. Его оптимальная температура роста 30—32 °С.
На спиртовых заводах, перерабатывающих мелассу, широко применяются штаммы дрожжей Я, Ял (лохвицкий), В (венгерский). Эти штаммы хорошо сбраживают сахарозу, глюкозу, фруктозу и лишь 1/3 рафинозы. Новый штамм У-2492 сбраживает больший спектр сахаров.
В спиртовом производстве применяют периодическое или непрерывно-проточное культивирование дрожжей, используя для этого батарею ферментеров. Для подавления размножения в ферментерах посторонней микрофлоры затор подкисляют серной кислотой или культуральной средой молочнокислых бактерий. Сбраживание затора проводят в анаэробных условиях при температуре 28—30 °С в течение
5—6 сут. Под действием ферментов дрожжей углеводы сбраживаются и получается зрелая бражка с содержанием спирта 9—11 %. Из бражки спирт выделяют перегонкой.
Виноделие. Вино — алкогольный напиток, получаемый обычно путем сбраживания виноградного сока винными дрожжами. В зависимости от сорта винограда цвет вина считается белым, розовым или красным.
Виноградные вина разделяют на:
✵ столовые (сухие), содержащие от 9 до 14 % спирта и сахара 0,2—0,6%;
✵ десертные или крепкие вина, содержащие до 22 % спирта. Десертные вина могут быть натуральными и креплеными, в которые добавляют виноградный спирт. В полусладких десертных винах содержание сахара составляет 3—7 %, в сладких — около 16 %;
✵ шипучие вина с избытком растворимой в них углекислоты, получаемой при брожении или искусственно введенной (игристые вина).
Технология вина включает дробление винограда, отделение сусла, прессование мезги, сбраживание сусла и снятие с осадка.
С целью подавления развития нежелательной микрофлоры и регулирования окислительно-восстановительных процессов сусло сульфитируют (вводят SO2).
Подготовленное для брожения сусло пастеризуют, охлаждают и перекачивают в бродильные емкости. Для брожения используют культурные дрожжи вида Saccharomyces cerevisiae (синонимы S. ellipsoides, S. vini). Они должны обладать ценными производственными свойствами: сбраживать сусло при низких температурах (13—15 °С) для подавления развития нежелательной микрофлоры; быть устойчивыми к высоким концентрациям спирта (до 18 %) и диоксида углерода, обладать кислототолерантностью, быстро оседать после брожения и давать плотный осадок. Чистые культуры винных дрожжей выделены и селекционированы для определенных типов вин.
В процессе главного брожения, длительность которого составляет 8—10 сут, выделяется тепло. Поэтому брожение следует проводить при постоянной температуре и равномерном отводе тепла с помощью охладительных систем. По окончании брожения проводят отстаивание и снятие сбродившего вина с осадка.
Уксусное скисание — одна из наиболее распространенных и опасных болезней вина, вызываемая развитием уксуснокислых бактерий родов Acetobacter или Gluconobacter. Этому виду порчи более подвержены столовые белые вина, особенно при высокой температуре хранения (28—30 °С). Болезнь развивается при доступе к вину кислорода воздуха, в основном при хранении в незаполненных емкостях. В начале заболевания на поверхности вина появляется тонкая беловатая пленка, которая в дальнейшем опускается на дно. Вино приобретает резкий запах и вкус уксусной кислоты, возникает колющее и царапающее ощущение в горле. Для устранения порока на ранних стадиях рекомендуется пастеризация вина с последующей его оклейкой, фильтрацией, сульфитацией. Если вино в значительной мере подверглось уксусной порче, то его можно использовать только для изготовления винного уксуса. Профилактика этого заболевания состоит в хранении вина в заполненных емкостях при низких температурах, соблюдении режимов сульфитирования, соблюдении санитарно-гигиенического режима производства.
Винная цвель — вид порчи, вызываемой аэробными пленчатыми дрожжами родов Candida, Pichia и так называемыми апикулятными (лимоновидными) дрожжами родов Uansenula и Hanseniaspora. Заболевают чаще молодые вина с невысоким содержанием спирта (до 12 %). При развитии указанных дрожжей на поверхности вина появляется сначала тонкая гладкая пленка, которая впоследствии разрастается, уплотняется, становится морщинистой, поднимается по стенкам сосуда. Вино становится мутным, приобретает неприятный запах и острый вкус за счет образования летучих кислот и эфиров.
Биологическая библиотека - материалы для студентов, учителей, учеников и их родителей.
Наш сайт не претендует на авторство размещенных материалов. Мы только конвертируем в удобный формат материалы, которые находятся в открытом доступе и присланные нашими посетителями.
Если вы являетесь обладателем авторского права на любой размещенный у нас материал и намерены удалить его или получить ссылки на место коммерческого размещения материалов, обратитесь для согласования к администратору сайта.
Разрешается копировать материалы с обязательной гипертекстовой ссылкой на сайт, будьте благодарными мы затратили много усилий чтобы привести информацию в удобный вид.
При спиртовом брожении помимо основных продуктов — спирта и СО2, из сахаров возникает множество других, так называемых вторичных продуктов брожения. Из 100 г С6Н12О6 образуется 48,4 г этилового спирта, 46,6 г диоксида углерода, 3,3 г глицерина, 0,5 г янтарной кислоты и 1,2 г смеси молочной кислоты, ацетальдегида, ацетоина и других органических соединений.
Наряду с этим дрожжевые клетки в период размножения и логарифмического роста потребляют из виноградного сусла аминокислоты, необходимые для построения собственных белков. При этом образуются побочные продукты брожения, главным образом высшие спирты.
В современной схеме спиртового брожения насчитывается 10—12 фаз биохимических превращений гексоз под действием комплекса ферментов дрожжей. В упрощенном виде можно выделить три этапа спиртового брожения.
I этап — фосфорилирование и распад гексоз. На этом этапе протекает несколько реакций, в результате которых гексоза превращается в триозофосфат:
Фосфогексокиназа, изомериаза, альдолаза
Главную роль в передаче энергии в биохимических реакциях играют АТФ (аденозинтрифосфат) и АДФ (аденозиндифосфат). Они входят в состав ферментов, аккумулируют большое количество энергии, необходимой для осуществления жизненных процессов, и представляют собой аденозин — составную часть нуклеиновых кислот — с остатками фосфорной кислоты. Вначале образуется адениловая кислота (монофосфат аденозина, или аденозинмонофосфат — АМФ):

Если обозначить аденозин буквой А, то строение АТФ может быть представлено в следующем виде:
А—О—Р—О ~ Р — О ~ Р— ОН
Значком с ~ обозначены так называемые макроэргические фосфатные связи, чрезвычайно богатые энергией, которая выделяется при отщеплении остатков фосфорной кислоты. Передача энергии с АТФ на АДФ может быть представлена следующей схемой:

Выделяющаяся энергия используется дрожжевыми клетками для обеспечения жизненных функций, в частности их размножения. Первым актом выделения энергии и является образование фосфорных эфиров гексоз — фосфорилирование их. Присоединение к гексозам остатка фосфорной кислоты от АТФ происходит под действием фермента фосфогексокиназы, поставляемого дрожжами (молекулу фосфата обозначим буквой Р):

Глюкоза Глюкозо-6-фосфат фруктозо-1,6-фосфат
Как видно из приведенной схемы, фосфорилирование происходит дважды, причем фосфорный эфир глюкозы под действием фермента изомеразы обратимо превращается в фосфорный эфир фруктозы, имеющий симметричное фурановое кольцо. Симметричное расположение остатков фосфорной кислоты по концам молекулы фруктозы облегчает ее последующий разрыв как раз в середине. Распад гексозы на две триозы катализирует фермент альдолаза; в результате распада образуется неравновесная смесь 3-фосфоглицеринового альдегида и фосфодиоксиацетона:

Фосфоглицери-новый альдегид (3,5 %) Фосфодиокси-ацетон (96,5 %)
В дальнейших реакциях участвует только 3-фосфоглицериновый альдегид, содержание которого постоянно пополняется под действием фермента изомеразы на молекулы фосфодиоксиацетона.
ІІ этап спиртового брожения — образование пировиноградной кислоты. На втором этапе триозофосфат в виде 3-фосфоглицеринового альдегида под действием окислительного фермента дегидрогеназы окисляется в фосфоглицериновую кислоту, а она при участии соответствующих ферментов (фосфоглицеромутазы и энолазы) и системы ЛДФ — АТФ превращается в пировиноградную кислоту:
Дигедрогеназа, фосфотрансфераза, фосфоглицеромутаза, энолаза
Вначале каждая молекула 3-фосфоглицеринового альдегида присоединяет к себе еще один остаток фосфорной кислоты (за счет молекулы неорганического фосфора) и образуется 1,3-дифосфоглицериновый альдегид. Затем в анаэробных условиях происходит его окисление в 1,3-дифосфоглицериновую кислоту:

Активной группой дегидрогеназы является кофермент сложного органического строения НАД (никотинамидадениндинуклеотид), фиксирующий своим никотинамидным ядром два атома водорода:
НАД+ + 2Н+ + НАД • Н2
НАД окисленный НАД восстановленный
Окисляя субстрат, кофермент НАД становится обладателем свободных ионов водорода, что придает ему высокий восстановительный потенциал. Поэтому бродящее сусло всегда характеризуется высокой восстанавливающей способностью, что имеет большое практическое значение в виноделии: понижается рН среды, восстанавливаются временно окисленные вещества, погибают патогенные микроорганизмы.
В заключительной фазе II этапа спиртового брожения фермент фосфотрансфераза дважды катализирует перенос остатка фосфорной кислоты, а фосфоглицеромутаза перемещает его от 3-го углеродного атома ко 2-му, открывая возможность ферменту энолазе образовать пировиноградную кислоту:

1,3-Дифосоглицериновая кислота 2-Фосфогглицериновая кислота Пировиноградная кислота
В связи с тем что из одной молекулы дважды фосфорилированной гексозы (израсходовано 2 АТФ) получаются две молекулы дважды фосфорилированных триоз (образовано 4 АТФ), чистым энергетическим балансом ферментативного распада сахаров является образование 2 АТФ. Эта энергия обеспечивает жизненные функции дрожжей и вызывает повышение температуры бродящей среды.
Все реакции, предшествующие образованию пировиноградной кислоты, присущи как анаэробному сбраживанию сахаров, так и дыханию простейших организмов и растений. III этап имеет отношение только к спиртовому брожению.
III этап спиртового брожения — образование этилового спирта. На заключительном этапе спиртового брожения пировиноградная кислота под действием фермента декарбоксилазы декарбоксилируется с образованием ацетальдегида и диоксида углерода, а с участием фермента алкогольдегидрогеназы и кофермента НАД-Н2 происходит восстановление ацетальдегида в этиловый спирт:

Пировиноградная кислота Ацетилальдегид Этиловый спирт
Если в бродящем сусле есть избыток свободной сернистой кислоты, то часть ацетальдегида связывается в альдегидсернистое соединение: в каждом литре сусла 100 мг Н2SO3 связывают 66 мг СН3СОН.
Впоследствии при наличии кислорода это нестойкое соединение распадается, и в виноматериале обнаруживают свободный ацетальдегид, что особенно нежелательно для шампанских и столовых виноматериалов.
В сжатом виде анаэробное превращение гексозы в этиловый спирт может быть представлено следующей схемой:

Схема спиртового брожения.
Как видно из схемы спиртового брожения, сперва образуются фосфорные эфиры гексоз. При этом молекулы глюкозы и фруктозы под действием фермента гексокеназы присоединяют остаток фосфорной кислоты от аденозиттрифосфата (АТФ), при этом образуется глюкоза-6-фосфат и аденозитдифосфат (АДФ).
Глюкоза-6-фосфат под действием фермента изомеразы превращается в фруктозу-6-фосфат, присоединяющий еще один остаток фосфорной кислоты из АТФ и образующий фруктозу-1,6-дифосфат. Эта реакция катализируется фосфофруктокиназой. Образованием этого химического соединения заканчивается первая подготовительная стадия анаэробного распада сахаров.
В результате этих реакций молекула сахара переходит в оксиформу, приобретает большую лабильность и становится более способной к ферментативным преобразованиям.
Под влиянием фермента альдолазы фруктоза-1, 6-дифосфат расщепляется на глицеринальдегидофосфорную и диоксиацетонофосфорную кислоты, способные превращаться одна в одну под действием фермента триозофосфатизомеразы. Дальнейшему преобразованию подвергается фосфоглицериновый альдегид, которого образуется приблизительно 3 % по сравнению с 97 % фосфодиоксиацетона. Фосфодиоксиацетон, по мере использования фосфоглицеринового альдегида, превращается под действием изомеразы фосфотриоз в 3-фосфоглицериновый альдегид.
На второй стадии 3-фосфоглицериновый альдегид присоединяет еще один остаток фосфорной кислоты (за счет неорганического фосфора) с образованием 1, 3-дифосфоглицеринового альдегида, который дегидруется под действием триозофосфатдегидрогеназы и дает 1, 3-дифосфоглицериновую кислоту. Водород, в этом случае, переносится на окисленную форму кофермента НАД. 1, 3-дифосфоглицериновая кислота, отдавая АДФ (под действием фермента фосфоглицераткеназы) один остаток фосфорной кислоты, превращается в 3-фосфоглицериновую кислоту, которая под действием фермента фосфоглицеромутазы превращается в 2-фосфоглицериновую кислоту. Последняя, под действием фосфопируватгидротазы, превращается в фосфоэнолпировиноградную кислоту. Дальше, при участии фермента пируваткеназы, фосфоэнолпировиноградная кислота передает остаток фосфорной кислоты молекуле АДФ, в результате чего образуется молекула АТФ и молекула энолпировиноградной кислоты переходит в пировиноградную кислоту.
Третья стадия спиртового брожения характеризуется расщеплением пировиноградной кислоты под действием фермента пируватдекарбоксилазы на диоксид углерода и уксусный альдегид, который под действием фермента алкогольдегидрогеназы (коферментом ее является НАД) восстанавливается в этиловый спирт.
Суммарное уравнение спиртового брожения может быть представлено так:
С6Н12О6 + 2Н3РО4 + 2АДФ → 2С2Н5ОН + 2СО2 + 2АТФ + 2Н2О
Таким образом, при брожении происходит преобразование одной молекулы глюкозы в две молекулы этанола и две молекулы диоксида углерода.
Но указанный ход брожения не единственный. Если, например, в субстрате нет фермента пируватдекарбоксилазы, то не происходит расщепление пировиноградной кислоты до уксусного альдегида и восстановлению подвергается непосредственно пировиноградная кислота, превращаясь в молочную кислоту в присутствии лактатдегидрогеназы.
В виноделии брожение глюкозы и фруктозы происходит в присутствии бисульфита натрия. Уксусный альдегид, образующийся при декарбоксилировании пировиноградной кислоты, удаляется в результате связывания бисульфитом. Место уксусного альдегида занимают диоксиацетонфосфат и 3-фосфоглицериновый альдегид, они получают водород от восстановленных химических соединений, образуя глицерофосфат, который превращается в результате дефосфорилирования в глицерин. Это вторая форма брожения по Нейбергу. По этой схеме спиртового брожения происходит накопление глицерина и уксусного альдегида в виде бисульфитной производной.
Вещества, образующиеся при брожении.
В настоящее время в продуктах брожения найдено около 50 высших спиртов, которые обладают разнообразными запахами и существенно влияют на аромат и букет вина. В наибольших количествах при брожении образуются изоамиловый, изобутиловый и N-пропиловый спирты. В мускатных игристых и столовых полусладких винах, получаемых путем так называемого биологического азотопонижения, в большом количестве (до 100 мг/дм3) найдены ароматические высшие спирты β-фенилэтанол (ФЭС), тирозол, терпеновый спирт фарнезол, обладающие ароматом розы, ландыша, цветов липы. Их присутствие в небольшом количестве желательно. Кроме того, при выдержке вина высшие спирты вступают в этерификацию с летучими кислотами и образуют сложные эфиры, придающие вину благоприятные эфирные тона зрелости букета.
Источником высших спиртов являются, прежде всего, аминокислоты, потребляемые дрожжами при размножении на стадии логарифмического роста.
Согласно теории Ф. Эрлиха высшие спирты образуются двумя путями:
І — через декарбоксилирование
R−CH(NH2)COOH → R−CH2NH2 → R−CH2OH
Аминокислота Амин Спирт
R−CH(NH2)COOH → R−CH(OH)COOH → R−CH2OH
Аминокислота Оксикислота Спирт
ІІ — через первоначальное гидролитическое дезаминирование
В дальнейшем было доказано, что основная масса алифатических высших спиртов образуется из пировиноградной кислоты путем переаминирования и непосредственного биосинтеза с участием аминокислот и ацетальдегида. Но наиболее ценные ароматические высшие спирты образуются только из соответствующих аминокислот ароматического ряда, например:

Образование высших спиртов в вине зависит от многих факторов. В нормальных условиях их накапливается в среднем 250 мг/дм3. При медленном длительном брожении количество высших спиртов возрастает, при повышении температуры брожения до 30 °С — уменьшается. В условиях поточного непрерывно брожения размножение дрожжей очень ограничено и высших спиртов образуется меньше, чем при периодическом способе брожения.
При уменьшении количества дрожжевых клеток в результате охлаждения, отстаивания и грубой фильтрации забродившего сусла происходит медленное накопление биомассы дрожжей и одновременно растет количество высших спиртов, прежде всего ароматического ряда.
Повышенное количество высших спиртов нежелательно для столовых белых сухих, шампанских и коньячных виноматериалов, однако придает многообразие оттенков в аромате и вкусе красным столовым, игристым и крепким винам.
Спиртовое брожение виноградного сусла связано также с образованием высокомолекулярных альдегидов и кетонов, летучих и жирных кислот и их эфиров, имеющих значение в формировании букета и вкуса вина.

мастер
винокур
СБОРНИК СТАТЕЙ
19 марта день самогонщика! Поздравляю вас! -->
Моё новое увлечение - солодовые дистилляты.
Желаю удачи всем неравнодушным к этой теме!
Подготовка сырья
Обработка продукта
Теория процесса брожения

Жозеф Луи Гей-Люссак
Еще Гей-Люссак (в 1815 г .) дал уравнение, описывающее превращение глюкозы в этанол в той форме, как это принято и теперь:
Нормальное сбраживание глюкозы дрожжами.
Сбраживание глюкозы до этанола и СО2 дрожжами(Saccharomyces cerevisiae) осуществляется по фруктозодифосфатному пути. Превращение пирувата в этанол происходит в два этапа. Сначала пируват декарбоксилируется пируватдекарбоксилазой (а) при участии тиаминпирофосфата до ацетальдегида, а затем ацетальдегид восстанавливается алкогольдегидрогеназой (б) в этанол при участии NADH2:
Переносится при этом водород, образующийся при дегидрировании триозофосфата; окислительно-восстановительный баланс, таким образом, сохраняется.
В 1896-1897 годах Бухнер и Хан обнаружили, что если к соку, полученному при растирании прессованных пивных дрожжей с кварцевым песком и кизельгуром, добавить сахар, то начинается брожение с образованием пены. Так впервые сложный биохимический процесс удалось осуществить вне клетки. В 1906 году Гарден и Ионг, тоже работавшие с дрожжевым соком, установили, что для сбраживания глюкозы нужен неорганический фосфат, который включается в фруктозо-1,6-дисфосфат. Сбраживание глюкозы дрожжевым соком происходит согласно уравнению Гардена-Йонга:

Формы брожения, открытые Нейбергом.
1877 Карл Александр Нейберг
Открытия Карла Нейберга и разработанные им оригинальные методы имеют не только историческое значение. Этот исследователь показал, что дрожжи способны сбраживать помимо глюкозы также и пируват. В качестве промежуточного продукта при сбраживании пирувата образуется ацетальдегид; это можно доказать, связывая альдегид бисульфитом (который для дрожжей практически нетоксичен). Если к дрожжам, сбраживающим глюкозу, прибавить бисульфит, будет происходить следующая реакция:
При этом появится новый продукт брожения – глицерол - и одновременно снизится выход этанола и СО2.
Брожение в присутствии бисульфита стали использовать в промышленности при производстве глицерола. Эта технология основана на том, что ацетальдегид связывается и поэтому не может служить акцептором водорода. Вместо ацетальдегида роль такого акцептора принимает на себя дигидроксиацетонфосфат; он восстанавливается до глицерол-3-фос-фата и дефосфорилируется с образованием глицерола. Брожение можно представить так:
-> Глицерол + Ацетальдегидсульфит + СО2
Это модифицированное дрожжевое брожение известно как вторая форма брожения по Нейбергу.Принцип перехватывания одного из метаболитов - метод ловушки - стал впоследствии общим биохимическим методом.
При добавлении к бродящему раствору NaHC03 или Na2HP04 то же образуется глицерол, так как ацетальдегид превращается в результате реакции дисмутации в этанол и уксусную кислоту и поэтому не может быть использован в качестве акцептора водорода. Это третья форма брожения по Нейбергу:
-> Этанол + Ацетат + 2 Глицерол + 2СО2
Нормальное дрожжевое брожение Нейберг назвал первой формой брожения. Он считал, что образующийся при небиологическом разложении фруктозы 2-оксопропаноль (метилглиоксаль, СН3-СО-СНО) также является промежуточным продуктом сбраживания глюкозы.

Луи Пастёр
Отношение дрожжей к кислороду.
Сбраживание дрожжами глюкозы - анаэробный процесс, хотя дрожжи - аэробные организмы. В анаэробных условиях брожение идет очень интенсивно, но роста дрожжей почти не происходит. При аэрации брожение ослабевает, уступая место дыханию. У некоторых дрожжей можно почти полностью подавить брожение усиленной аэрацией (эффект Пастера). Пастер открыл этот эффект более ста лет тому назад, исследуя процессы брожения при изготовлении вина. Это явление свойственно не только дрожжам, но и всем другим факультативно-анаэробным клеткам, включая клетки тканей высших животных.
Баланс превращений глюкозы (на примере типичного опыта с дрожжами) представлен в табл. 8.1.

Аэрация уменьшает потребление глюкозы, а также образование этанола и СО2, но делает возможным рост дрожжей. С энергетической точки зрения эти явления понятны; они указывают на существование у дрожжей чрезвычайно полезного регуляторного механизма: в анаэробных условиях образуются только 2 моля АТР на один моль использованной глюкозы, а при дыхании - 38 молей АТР.
Таким образом, клетка, регулируя превращения субстрата, может получать максимум энергии как в тех, так и в других условиях.
В третьем столбце табл. 8.1 приводятся результаты опыта, в котором дрожжи инкубировали в аэробных условиях в присутствии 0,4 мМ 2,4-динитрофенола (ДНФ).
ДНФ разобщает фосфорилирование и окисление в дыхательной цепи: он нарушает сопряжение между переносом электронов и фосфорилированием, после чего дыхание протекает уже без контроля со стороны фосфорилирования.
Добавление ДНФ практически выключает фосфорилирование в дыхательной цепи, и водород, отщепляющийся в цикле трикарбоновых кислот, уже не может использоваться для энергетических целей.
Доступным для использования оказывается только высокоэнергетический фосфат, образующийся при расщеплении сукцинил-СоА. Результаты опыта показывают, что в присутствии ДНФ потребление глюкозы возрастает до величины, наблюдаемой в анаэробных условиях, что связано с его разобщающим действием.
В реакции Пастера участвует, видимо, несколько регуляторных механизмов, действующих в одном направлении. Эффект одного из них проявляется на уровне процессов фосфорилирования.
В основе его лежит конкуренция за аденозиндифосфат (ADP) и неорганический фосфат (Р;). Для дегидрирования при расщеплении глицеральдегидфосфата необходимы ортофосфат и ADP:
Глицеральдегид-3-фосфат + NAD + ADP +
Таким образом, расщепление субстрата (глюкозы) по фруктозодифосфатному пути зависит от наличия ADP и неорганического фосфата. В отсутствие ADP и фосфата дегидрирование глицеральдегидфосфата оказывается невозможным.
Однако в аэробных условиях с этой реакцией конкурирует за ADP и фосфат процесс фосфорилирования в дыхательной цепи, который тоже приводит к образованию АТР.
Вполне вероятно, что расщепление глюкозы, а вместе с тем и образование этанола тормозятся в результате снижения внутриклеточной концентрации ADP и фосфата. Если же под действием ДНФ процессы окисления в дыхательной цепи и фосфорилирование разобщаются, то ADP и фосфат снова могут использоваться для дегидрирования глицеральдегид фосфата, и аэробное потребление глюкозы повышается до уровня, соответствующего анаэробным условиям (см. табл.).
За реакцию Пастера ответствен еще один регуляторный механизм, а именно аллостерический эффект торможения фермента фосфофруктокиназы аденозинтрифосфатом.
Объяснение процесса, описанного Гарденом и Ионгом.
Отжатый дрожжевой сок разлагает глюкозу в соответствии с уравнением Гарде-на-Ионга. Накопление фруктозо-1,6-дисфосфата объясняется в этом случае тем, что АТР в нарушенной ферментной системе (в отличие от живой клетки) не может использоваться для энергетических целей и остается в избытке.
Дрожжевой сок не содержит фосфатаз, поэтому ADP должен непрерывно регенерироваться за счет фосфорилирования лишней глюкозы или фруктозо-6-фосфата.
Пекарские дрожжи(Saccharomyces cerevisiae) должны поднимать тесто в результате образования СО2, т.е. осуществлять интенсивное брожение.
Их выращивают в чанах при сильной аэрации. В качестве побочного продукта при этом всегда образуется этанол. Варьируя степень аэрации и режим добавления сахара, можно изменять относительный выход дрожжей и спирта. При проточном способе, непрерывно прибавляют сахар, но так медленно, чтобы он ограничивал рост дрожжей. Это избавляет от образования продуктов брожения - весь сахар используется для роста.
Источником азота служит аммоний. Необходимые ростовые вещества дрожжи получают из добавляемого пшеничного затора.
Пивные дрожжи по большей части относятся к низовым расам (мюнхенское, пильзенское пиво), реже к верховым (светлое пиво, эль, портер). В Центральной Европе пиво варят в основном из ячменя, выбирая для этой цели ячмень с наименьшим содержанием белка и высоким содержанием крахмала. Поскольку дрожжи не образуют амилаз и могут сбраживать только сахара, но не крахмал, необходимо сначала обеспечить осахаривание крахмала.
Для этого используют специфическую амилазу, образующуюся при прорастании зерен ячменя. Зернам дают набухнуть и прорасти; образовавшийся зеленый солод осторожно сушат при определенной температуре, при которой прерывается только процесс прорастания, а ферменты сохраняются.
Просушенный солод размалывают и погружают в чаны с водой. При умеренной температуре крахмал через некоторое время осахаривается, превращаясь в мальтозу. Полученное сусло освобождается от дробины, к нему добавляют хмель, варят, охлаждают и подвергают брожению в бродильных чанах, прибавляя предварительно выращенные дрожжи.
Для получения спирта (этанола) путем брожения используют отходы производства сахара (мелассу) или картофель. Большие количества дешевого спирта получают также из гидролизатов древесины лиственных пород или из сульфитных щелоков - отходов бумажных фабрик.
В гидролизатах древесины сбраживаются до этанола только гексозы. Остающиеся после этого пентозы используют для выращивания кормовых дрожжей (Endomyces lactis и видов Torula), для которых они служат источником углерода; эти дрожжи, богатые белками, добавляют в корм скоту.
Многие немецкие вина получают в результате спонтанного брожения виноградного сока, вызываемого дрожжами рода Kloeckera.
Для подавления неконтролируемого брожения, вызываемого дикими дрожжами, неоднократно вносят чистые культуры дрожжей или смеси Kloeckera и Saccharomyces, которые подбирают в специальных винодельческих районах.
Еще большее значение для букета вина имеет, однако, сорт винограда (Рислинг, Сильванер, Мюллер-Тургау, Шейребе, Кернер и др.), а также климатические и почвенные факторы, влияющие на рост виноградной лозы.
Во всех жидкостях, полученных путем дрожжевого брожения, содержатся сивушные масла: пропанол, 2-бутанол, 2-метилпропанол, амиловый (пентанол) и изоамиловый (триметилбутанол) спирты.
Они представляют собой продукты нормального бродильного метаболизма дрожжей и обнаруживаются не только при их росте в сложных питательных растворах, содержащих аминокислоты. Основными компонентами сивушного масла являются побочные продукты обмена изолейцина, лейцина и валина.
Химизм спиртового (алкогольного) брожения
В раскрытие химизма спиртового брожения много творческого труда было вложено нашими отечественными учеными, особенно Л. А. Ивановым, С. П. Костычевым, А. Н. Лебедевым, А. Е. Фаворским, а также зарубежными учеными - Нейбергом, Мейергофом и другими, которые с достаточной полнотой и достоверностью установили следующие положения:
1. Брожение является целиком ферментативным процессом. Роль дрожжей при спиртовом брожении заключается в том, что они вырабатывают ферменты, осуществляющие глубокое расщепление такого сложного органического вещества, каким является сахар.
2. Алкогольное брожение не является ступенчатым процессом с последовательной сменой биохимических реакций. В естественных условиях в бродящей среде одновременно совершаются превращения огромного числа молекул сахара, а следовательно, в один и тот же момент можно наблюдать все фазы процесса - параллельное протекание всех реакций. Считают, что фосфорилирование одной молекулы гексозы идет с одновременным сбраживанием второй.
3. В спиртовом брожении обязательное участие принимает фосфорная кислота, перенос которой осуществляется аденозин-трифосфорной кислотой (АТФ). Последовательный ход превращений моносахаридов по современной схеме спиртового брожения. Реакция восстановления уксусного альдегида в этиловый алкоголь является как бы завершающим этапом брожения.
На основе современной схемы спиртового брожения объясняется механизм и многих других видов брожения - молочнокислого, маслянокислого, глицеринового.
Последовательный ход превращений моносахаридов
Наиболее благоприятной концентрацией сахара в бродящей среде является концентрация 10-20%. По мере брожения в среде повышается содержание спирта, который угнетающе действует на дрожжи. При спиртуозности 18% об. (а для некоторых рас дрожжей при 22% об.) брожение останавливается. Такая концентрация спирта для дрожжей является предельной.
Большое значение для брожения имеет и температура среды. Лучше всего брожение протекает при 15-25 °С. При 35 °С наблюдается затормаживание брожения, а при 50 °С оно прекращается совсем, так как происходит инактивирование бродильных ферментов. Минимальная температура, при которой наблюдается еще действие зимазы, 4-5°С. Падение бродильной способности дрожжей с повышением температуры связано с возрастанием ядовитого действия спирта на зимазу.
Применяемая раса дрожжей оказывает большое влияние на результаты спиртового брожения. Одни дрожжи способны накапливать больше спирта, другие больше продуцируют альдегидов, глицерина, обусловливают накопление ароматических веществ, слагающих букет напитка (вина). К настоящему времени выведено большое количество дрожжевых рас (чистых культур), с самыми разнообразными свойствами, необходимыми для соответствующего производства.
Спиртовое брожение нормально протекает в средах с довольно высокой кислотностью (pH 3,5-4,5) и в анаэробных условиях. Если в бродящую среду продувать воздух, то дрожжи переходят к нормальному (аэробному) дыханию, начинают усиленно почковаться, что в конечном итоге приводит к резкому увеличению их живой массы. Это широко используют при получении прессованных дрожжей.
Читайте также:

