Протезирование митрального клапана сердца механическим протезом сколько больничный лист
Обновлено: 18.05.2024
На протяжении многих лет бытует спорный вопрос: Что выгоднее? Что целесообразнее и что предпочтительнее выполнять при врожденной клапанной патологии (МК ) у детей раннего возраста: реконструкцию или протезирование.
Безусловно, предпочтительными являются реконструктивные операции, которые следует рассматривать как процедуру оптимального выбора у детей раннего возраста. Реконструкция у правильно отобранных пациентов дает удовлетворительные отдаленные результаты и меньшее количество осложнений, чем протезирование, а также отсутствует необходимость постоянного применения антикоагулянтов [2, 3, 7, 8]. Однако, грубая сочетанная патология клапанов в этой возрастной группе делает восстановительные операции неэффективными и порой невозможными. Более того, частое сочетание патологии клапанов у детей с другими врожденными пороками сердца вызывает особые технические трудности. Для данной категории больных по мнению большинства кардиохирургов замещение клапана на механический протез является рациональным выбором хирургической тактики [1, 4, 5, 6].
Целью нашего исследования явился анализ 13 летнего опыта по протезированию митрального клапана у детей раннего возраста.
Таблица 1| Пол | Возраст | Количество пациентов | |||
| до 1 года | от 1 до 2 лет | от 2 до 4 лет | n | % | |
| Мужской | 14 | 23 | 7 | 44 | 41,7 |
| Женский | 22 | 27 | 11 | 60 | 58,3 |
| Всего | 36 | 50 | 18 | 104 | 100 |
При физикальном обследовании у всех пациентов выявлялись признаки недостаточности кровообращения той или иной степени выраженности, сопровождавшиеся одышкой, снижением физической активности, а в тяжелых случаях хрипами в легких. Большинство больных отставали в физическом развитии, многие из них имели .
Таблица 2| Группа | Форма порока | Кол-во наблюдений | |
| n | % | ||
| 1. | Врожденная изолированная недостаточность митрального клапана | 38 | 36,5 |
| 2. | Митральная недостаточность после радикальной коррекции ООАВК | 22 | 21,3 |
| 3. | Митральная недостаточность в сочетании с септальными пороками (ДМПП и ДМЖП) | 11 | 10,6 |
| 4. | СБУГ | 12 | 11,6 |
| 5. | Митральная недостаточность в сочетании с коарктацией аорты | 7 | 6,7 |
| 6. | Врожденный комбинированный митральный порок (стеноз+недостаточность) | 7 | 6,7 |
| 7. | Митральная недостаточность в сочетании с клапанным стенозом аорты | 3 | 2,6 |
| 8. | Врожденная недостаточность митрального клапана + трикуспидальная недостаточность | 3 | 2,6 |
| 9. | Бактериальный эндокардит | 1 | 1,0 |
| Всего | 104 | 100 | |
Окончательное решение о протезировании пораженного клапана принимали интраоперационно после оценки анатомических изменений клапанных структур. Основанием для замещения митрального клапана на искусственный механический протез было отсутствие возможности выполнения пластики ввиду грубых морфологических изменений. При ревизии у всех пациентов отмечалась выраженная . У 56% пациентов отмечалось створок клапана (рис. 1), а у остальных больных отмечалось либо грубое утолщение передней створки, либо выраженная с утолщением или спаянием со свободной стенкой левого желудочка (рис. 2). Изменения в хордальном аппарате были представлены либо удлинением, либо укорочением хорд, т.е. нарушением корреляционной связи между длиной хорд и сосочковых мышц. Среди аномалий развития сосочковых мышц отмечалась их гипоплазия, вплоть до , а также . У 16 (15,4%) пациентов с выраженной недостаточностью на митральном клапане присутствовали изменения во всех его структурах.
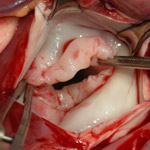
Рис.1. Отмечается соединительнотканная
дисплазия створок митрального клапана с
гипоплазией хорд и сосочковых мышц.
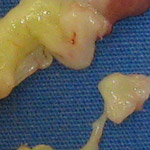
Рис.2. Иссечен миксоматозно измененный
митральный клапан, припаянный к сосочковой
мышце, хорды отсутствуют.
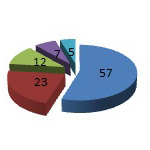
Рис.3. Перечень искусственных
механических клапанов сердца,
имплантированных в митральную
позицию у детей раннего возраста.
В раннем послеоперационном периоде летальность составила 16 (15,4%) пациентов. Основной причиной смерти послужила травматичность операции и острая сердечная недостаточность как пусковой фактор, с развитием в последующем полиорганной недостаточности.
По мере улучшения хирургической техники и усовершенствования дооперационной диагностики в плане четкой дифференцировки клапанов, не пригодных к реконструкции, и установления абсолютных показаний к протезированию в течении последних 2 лет мы добились снижения госпитальной летальности у детей раннего возраста до 6,6%.
Осложненный послеоперационный период наблюдался у 35 (35,6%) пациентов. На первом месте среди осложнений была сердечная недостаточность - у 17 (16,3%) детей ввиду исходно тяжелого состояния миокарда левого желудочка; на втором - осложнения со стороны органов дыхания - 10 (9,6%) малышей, что требовало пролонгированной искусственной вентиляции легких и более длительного пребывания пациентов в отделении реанимации. У 5 (4,8%) пациентов имелись нарушения ритма в виде полной поперечной блокады, что потребовало имплантацию искусственного водителя ритма. У 1 младенца имело место развитие внутренних кровотечений в плевральные и брюшную полость на фоне нарушения свертывающей системы крови в виде гипокоагуляции и гипофибринемии. Среди осложнений, потребовавших хирургического вмешательства (репротезирование МК) в ранние сроки после операции, особо следует отметить развитие парапротезной фистулы (1 ребенок) и ранний тромбоз имплантированного клапана у ребенка с первичным бактериальным эндокардитом.
Таблица 3| Осложнения | Количество случаев | |
| n | % | |
| Острая сердечная недостаточность | 17 | 16,3 |
| Дыхательная недостаточность | 10 | 9,6 |
| Нарушения ритма сердца и проводимости | 5 | 4,8 |
| Кровотечение | 1 | 0,9 |
| Парапротезная фистула | 1 | 0,9 |
| Тромбоз клапана | 1 | 0,9 |
В ряде случаев при развитии тяжелой посткардиотомной сердечной недостаточности в ближайшем послеоперационном периоде были использованы системы вспомогательного кровообращения, такие как внутриаортальная баллонная контрпульсация (у 1 ребенка) и экстракорпоральная мембранная оксигенация- в 2 случаях.
Неосложненный ранний послеоперационный период наблюдался у 69 (66,3%) пациентов. После перевода в отделение интенсивной терапии у них отмечалась стабильная гемодинамика при поддержке терапевтическими дозами кардиотоников: - не более 6 мкг/кг/мин, - не более 8 мкг/кг/мин. Среднее время искусственной вентиляции легких составило 16±3,8 часа. На вторые сутки после операции больных переводили в отделение, где в дальнейшем у них наблюдалось постепенное улучшение состояние с заживлением раны первичным натяжением.
12 (11,5%) больных с осложненным послеоперационным периодом были выписаны из стационара спустя в среднем 22±5,2 дня после операции (от 17 до 26 дней), а те пациенты, послеоперационный период у которых протекал без осложнений,- в среднем на 11±3,2 сутки (от 7 до 14 суток).
Все пациенты в послеоперационном периоде получали антикоагулянтную терапию. Сразу же после операции назначали гепарин (из расчета 200 ЕД/кг/сут каждые 6 часов) с последующим переходом на непрямые антикоагулянты (варфарин) в дозе 0,09 мг/кг/сут. Коррекция антикоагулянтной терапии проводилась под контролем показателей свертывающей системы крови- протромбиновый индекс (ПТИ) и международное нормализованное отношение (МНО). Мы добивались достижения уровня МНО-2-3,5 и протромбинового индекса 35-50%.
Отдаленные результаты оценивались спустя год и более после операции. Однако по независящим от нас причинам с некоторыми больными связь была утрачена. Через год после операции обследовано 81 пациент, через 2 года - 65, через 5 лет - 59 пациентов. Максимальный срок наблюдения за больными, перенесшими протезирование митрального клапана в раннем детском возрасте в настоящее время составляет 10 лет.
Следует отметить, что через 2 года после операции у большинства пациентов отсутствуют жалобы, размеры полостей сердца по данным эхокардиографии соответствуют возрастным нормам. Примечателен тот факт, что более половины детей перенесших протезирование митрального клапана, спустя два года после операции относятся к Iст. недостаточности кровообращения, т.е. считаются практически здоровыми.
В отдаленном послеоперационном периоде у 6 пациентов в связи с перерастанием размера протеза произведено репротезирование митрального клапана.
После протезирования митрального клапана, несмотря на то, что все больные были вынуждены принимать антикоагулянты и регулярно контролировать показатели свертывающей системы крови, отмечено улучшение качества их жизни. Дети стали меньше болеть простудными заболеваниями, сократилось количество принимаемых препаратов, что немаловажно для психологического состояния как для самих пациентов, так и для их родителей.
Протезирование митрального клапана у детей раннего возраста является эффективным методом хирургического лечения выраженной недостаточности левого атриовентрикулярного отверстия. Показанием к протезированию митрального клапана у детей раннего возраста является наличие грубой патологии во всех его структурах (дилатация фиброзного кольца с нарушением развития створок, хорд и сосочковых мышц), приведших к тотальной регургитации. При выборе протеза для имплантации в митральную позицию у детей раннего возраста предпочтение следует отдавать низкопрофильным двустворчатым искусственным клапанам сердца. Вопрос о сроках замены протеза решается строго индивидуально, исходя из данных клинического и инструментального методов обследования совместно с кардиологом и кардиохирургом.
Иллюстрации к статье
1. Бокерия, Л. А. Протезирование митрального клапана у детей раннего возраста при ВПС /Л. А. Бокерия, К. В. Шаталов, А. А. Свободов, Т. И. Мусатова и др. //Грудная и сердечно- сосудистая хирургия. –М.,-2003.-№3.–С.16-19.
2. Бокерия, Л. А. Врожденная недостаточность митрального клапана /Л. А. Бокерия, И. И. Каграманов, Ю. И. Бондарев.–М: Изд-во НЦССХ им А.Н.Бакулева. 2003.–112с.
3. Бокерия, Л. А. Нормативные параметры предсердно- желудочковых клапанов по результатам морфометрических исследований / Л. А. Бокерия, О. А. Махачев, М. С. Панова, Т. Ю. Мосевская //Сердечно- сосудистые заболевания. -2005.–Т.6.-№1.–С.5-25.
4. Дробот, Д. Б. Протезирование клапанов сердца у детей: дисс… д-ра. мед. наук / Д. Б. Дробот. –М., 2004.-248с.
5. Железнев, С.И. Клинико- гемодинамическая оценка результатов операций протезирования митрального клапана с сохранением подклапанных структур при митральной недостаточности /С. И. Железнев. //Патология кровообращения и кардиохирургия. –2007.-№3.–С.20-24.
Что такое механический клапан сердца. Как проводится операция по замене клапана, ее стоимость в Израиле. Каковы риски и жизнь после.
Автор Юлия Дубчак

Протезирование митрального и аортального клапанов – самая распространенная операция на сердце в Израиле. Она выполняется, если пластика клапана в конкретном случае не может быть эффективной.
Замена может проводится искусственным или биологическим протезами, в зависимости от показаний и возраста пациента.
Замена клапанов сердца искусственным протезом в Израиле – миниинвазивные методы операций, лучшие кардиохирурги, реабилитация.
- техника “замочной скважины” – проведение хирургического вмешательства через небольшой боковой разрез грудной клетки
- чрескожная имплантация – внедрение протеза через катетер, размещенный в бедренной артерии (в основном применяется для имплантации биологического клапана)
Решение о методе хирургического вмешательства принимает врач на основании здоровья и возраста пациента, результатов обследования, особенностей патологии сердечного клапана и выбранного протеза.
Самыми востребованными и опытными кардиохирургами Израиля являются:
Послеоперационное нахождение в больнице происходит под наблюдением врачей и занимает, в среднем, до 10 дней. При соблюдении рекомендаций самочувствие полностью нормализуется уже через несколько недель после замены клапана.
Стоимость замены клапана в Израиле
- опыта и уровня квалификации выбранного хирурга,
- метода протезирования,
- типа механического клапана, ( частная или государственная),
- длительности нахождения в стационаре, обусловленной скоростью восстановления после операции.
Как сделать операцию на сердце у одного из лучших кардиохирургов Израиля?
Виды искусственного клапана сердца, срок службы и отличия от биологического.
В медицинской практике для восстановления нормальных функций сердца используют два вида клапанов – биологические и механические. Первые – заменители животного происхождения (обработанные аортальные ткани свиньи, бычьего перикарда), имеющие срок службы до 15 лет. Вторые выполнены из искусственных материалов – металла, силикона.
Стоит отметить, что искусственный клапан сердца имеет неограниченный срок службы и позволяет жить нормальной жизнью минимум 20-30 лет после хирургического вмешательства.
Виды искусственных клапанов сердца, применяемых в Израиле
- Шариковые – состоят из металлического каркаса с силиконовым эластомером
- Наклонные диски – представляют собой кольцо с регулируемой распоркой
- Двустворчатые – два полукружных клапана, вращающиеся вокруг распорки, прикрепленной к основанию.
Процент износа механического клапана ничтожно мал, а необходимость проведения повторной операции по его замене сводится к нулю. По этой причине в Израиле проводят имплантацию искусственных аортальных и митральных клапанов чаще молодым людям.
Единственным минусом любого вида механического имплантата является необходимость регулярного наблюдения за функциями свертываемости крови – приема препаратов для ее разжижения.
Диагностика, показания к операции по замене клапана и возможные риски.
- Выраженного разрастания соединительной ткани митрального или аортального клапана (фиброз)
- Невозможности произвести разделение спаек при стенозе клапанного отверстия сердца (комиссуротомия)
- Образований отложений кальция на створках клапана
- Патологических изменений структуры
- ЭКГ – процедура дает возможность определить нарушения работы сердечного ритма
- УЗИ сердца – эхографическое исследование, включая чреспищеводное, нужно для составления полной картины заболевания
- Ряд анализов для оценки общего состояния здоровья – рентгенография, анализы крови, включая развернутое биохимическое исследование
- Коронарографию сердца и сосудов – актуальна для людей с ишемической болезнью
Как живет человек с искусственным митральным клапаном? Есть ли ограничения?
В целом жизнь человека любого возраста после установки механического клапана мало чем отличается от прежней: рекомендуется соблюдение базовых правил правильного питания, прогулок на свежем воздухе, отказа от вредных привычек и контроля над эмоциональным состоянием. Единственным исключением, особенно среди молодых пациентов, следует считать запрет на занятие профессиональным спортом “высоких достижений”, поскольку такие виды физических нагрузок априори подразумевают перегрузку сердечно-сосудистой системы.
Срок жизни с искусственным клапаном сердца приравнивается к средним показателям жизни человека, не перенесшего подобную процедуру. Возможный износ или необходимость повторной операции связываются преимущественно с усталостью металла либо несоблюдением предписаний врача, особенно у молодых активных людей.
Искусственный клапан сердца требует регулярного, но не утомительного наблюдения за состоянием здоровья. Так, первый год посещать лечащего врача необходимо ежемесячно, далее – каждые полгода при отсутствии других показаний.

Замена сердечного клапана – в настоящее время это очень эффективная процедура с малым риском осложнений. Она показана больным с симптомами стеноза аортального клапана. Отказ от этой передовой хирургической технологии для некоторых больных означает существенное сокращение продолжительности жизни или опасность внезапной смерти. Если нет явных противопоказаний к операции (например, ишемическая болезнь сердца, перенесённый инфаркт), то обычно эта операция назначается и рекомендуется всем больным со степенью стеноза выше средней. При тяжёлых симптомах (боль в груди, обмороки, проблемы с дыханием) продолжительность жизни многих больных без операции на сердце не превышает 5 лет, поскольку заболевание со временем прогрессирует.
Операция по замене сердечного клапана может производиться открытым способом или малоинвазивно. Хотя это довольно сложная процедура, огромный опыт такого хирургического лечения в настоящее время значительно снизил возможные риски. Все этапы отработаны до мелочей. Во время замены клапана учитывается возможность осложнений и внештатных ситуаций, поэтому операционная и медицинский состав подготавливаются с учётом разного развития ситуации в ходе операции.
Замена сердечного клапана проходит в восемь этапов. Перед этим больной проходит подготовку к операции (амбулаторно или в условиях стационара), соблюдая определённые назначения и принимая ряд препаратов. В некоторых случаях необходима, наоборот, отмена регулярно принимаемых лекарств.
2. Этапы операции
На первом этапе больного подключают к кардиомониторам, обрабатывается грудная клетка, подводятся дыхательные трубки от аппарата искусственного дыхания, который подключается только после того, как начнет действовать наркоз (т.е. единственным дискомфортом для больного может стать некоторое першение и саднение в горле после операции).
Анестезиолог вводит пациента в состояние общего наркоза. С этого момента оперируемый не ощущает ничего.
Через пищевод в область сердца помещается ультразвуковое устройство, транслирующее изображение сердца на монитор в течение всей операции.
Второй этап – это открытие грудной клетки. После разметки кардиохирург делает разрез на груди от вершины грудной клетки до пупка. При малоинвазивном методе длина разреза меньше на две трети.
Целью третьего этапа является подключение к аппарату, обеспечивающему искусственное кровообращение. Во время операции обогащение крови кислородом происходит вне лёгких, затем она возвращается в аорту и движется по большому кругу кровообращения.
На этом этапе хирург останавливает сердце, промывает его и помещает в специальный раствор, поддерживающий его жизнеспособность вне кровообращения.
Четвёртый и пятый этапы – это собственно замена клапана. Аорта разрезается, удаляется больной клапан. Если поражена и часть аорты, она тоже удаляется и ставится трансплантат. Отверстие клапана замеряется для подбора нового клапана нужного размера. Новый клапан пришивается, затем необходимо проконтролировать отсутствие истечений через него.
Шестой этап – это отключение от аппарата искусственного кровообращения. Зашивается аорта, из полости сердца удаляется попавший в него воздух. Сердце начитает биться под током собственной крови. Если наблюдается неровный ритм, применяется электрошок, который восстанавливает ровный пульс.
Седьмой этап – закрытие грудной клетки. Кости и ткани сшиваются, грудина закрывается швом, которые остаётся видимым на всю жизнь.
Вся операция обычно длится от 2 до 5 часов.
Немаловажным для исхода лечения является восьмой этап. Начинается он в палате интенсивной терапии. Выписка из стационара происходит на 5-9 день после операции. Послеоперационная реабилитация продолжается амбулаторно.
3. Эффективность операции протезирования аортального клапана
Эффективность операции по замене сердечного клапана во многом зависит от состояния больного на момент операции и некоторых факторов:
- наличие сердечной недостаточности;
- причины сердечной недостаточности;
- серьезные нарушения сердечной деятельности;
- другие серьезные заболевания.
4. Срок функционирования сердечных клапанов
На сегодняшний день в хирургии сердца применяют два вида имплантатов сердечных клапанов: искусственные и биологические. Первые — долговечные, но их установка связана с пожизненным приёмом ряда препаратов для устранения риска тромбообразования. Биологические клапаны наиболее близки живым тканям, но быстрее изнашиваются. Кардиологи постоянно ведут работу по разработке и внедрению в медицинскую практику новых типов клапанов, сочетающих в себе лучшие свойства обоих видов — долговечность и максимальную приемлемость для организма. Срок службы искусственных клапанов 10-15 лет. Более новые материалы пока только проходят изучение. Широкая практика их применения в ближайшем будущем даст кардиологам более точную информацию о сроке их службы.
Заболевания ![частые заболевания]()
Жалобы и симптомы ![Жалобы и симптомы]()
Если вы обнаружили у себя подобные симптомы, возможно, это сигнал заболевания, поэтому рекомендуем проконсультироваться с нашим специалистом.
Диагностика ![Диагностика]()
Наши цены ![Типичные жалобы]()
- Консультация врача кардиолога, кмн - от 3000 р.
- Биохимический анализ крови (стандартная, 10 показателей) - 2470 р.
- Биохимический анализ крови (расширенаяая, 14 показателей) - 3565 р.
- Общий анализ крови - 675 р.
- Электрокардиограмма (ЭКГ) - 900 р.
- Электрокардиограмма (ЭКГ) с расшифровкой - 1500 р.
- ЭхоКГ (эхокардиография, УЗИ сердца) - 4500 р.
- Нагрузочный тест (велоэргометрия) - 5000 р.
- Холтеровское (суточное) мониторирование ЭКГ - 4000 р.
- СМАД (суточное мониторирование АД) - 4000 р.
Мы стараемся оперативно обновлять данные по ценам, но, во избежание недоразумений, просьба уточнять цены в клинике.
Данный прайс-лист не является офертой. Медицинские услуги предоставляются на основании договора.
• Виды механических протезов •• Шаровые (в настоящее время не применяют): Magovern-Cromie, Smeloff-Cutter, Cross-Jones, АКЧ, МКЧ •• Дисковые: Bjork-Shiley, Sorin Monocast, Medtronic-Hall, Lillehei-Kaster, Omniscience, Bicer, МИКС, ЛИКС •• Двустворчатые: St. Jude Medical, Sorin Bi Carbon, Carbomedics, ATS, Duromedics, MedEng.
• Преимущество •• Долговечность — в среднем более 30 лет (не принимая во внимание случаи протезного инфекционного эндокардита [ИЭ]) •• Исключение составляют поломки стойки запирательного элемента в некоторых моделях клапана Bjork–Shiley.
• Недостатки •• Тромбогенность (наименьшая у клапана St. Jude Medical) •• Необходимость постоянной антикоагулянтной терапии •• Относительное стенозирование у дисковых и шаровых протезов •• Постпротезные аневризмы у дисковых протезов с небольшим углом открытия запирательного элемента.
• Антикоагулянтная терапия •• Начинают через 2 сут после операции, несмотря на терапию непрямыми антикоагулянтами (МНО на уровне 3,0–4,5) •• Риск тромбоэмболий высок (0,2% летальных и 2% нелетальных осложнений в год) •• Тромбозы после протезирования митрального клапана возникают значительно чаще, вследствие протезирования аортального клапана •• Неоднозначное отношение к механическим клапанам в трикуспидальной позиции (как правило, используют протезы St. Jude Medical) вызвано частым тромбообразованием в правых отделах сердца ••• Такое тромбообразование обусловлено, по-видимому, низкой концентрацией ПгI2, обладающего антитромботическим действием. Этот Пг синтезируется в лёгких и поступает с током крови в левые отделы сердца •• Если хотя бы один раз возникла тромбоэмболия, вызванная наличием протеза, то риск повторных эмболий повышен •• Постоянная антикоагулянтная терапия, даже при умеренном увеличении МНО (до 3,0), значительно увеличивает риск кровотечений.
БИОЛОГИЧЕСКИЕ КСЕНОПРОТЕЗЫ (Hancock, Carpentier-Edwards, КемКор) и аллотрансплантаты. По гемодинамическим характеристикам оба клапана сопоставимы с низкопрофильными механическими протезами (двустворчатым и дисковым).
• Преимущества •• Тромбогенность существенно ниже, чем у механических протезов •• Антикоагулянтная терапия необходима только в течение 2–3 мес после операции (пока не произойдёт эндотелизация пришивного кольца).
• Недостатки •• Недолговечность вследствие дегенеративных изменений и ИЭ, обычно проявляющихся через 4–5 лет после операции и в дальнейшем прогрессирующих •• Вероятность дисфункции через 10 лет после операции — 20%, через 15 лет — 50% •• Долговечность аллотрансплантатов незначительно выше, чем других биологических протезов.
• Факторы, влияющие на долговечность •• Возраст пациента — вероятность дисфункции протеза обратно пропорциональна возрасту на момент операции •• Позиция — вероятность дисфункции протеза в митральной позиции ниже, чем в аортальной •• ХПН и гиперкальциемия при гиперпаратиреозе — увеличение риска дисфункции и скорости её прогрессирования •• Беременность — укорочение срока службы вследствие большей гемодинамической нагрузки (объёмом).
Выбор протеза • Механические протезы •• Аортальная позиция или необходимость одновременного протезирования митрального и аортального клапанов •• ИЭ или реимплантация протеза в связи с ИЭ •• Гиперкальциемия •• Почечная недостаточность • Биологические протезы •• Высокий риск тромбозов (см. ниже) •• Противопоказания к антикоагулянтной терапии (геморрагические диатезы, повторные желудочно-кишечные кровотечения, алкоголизм, нежелание или неспособность следовать схеме лечения), планируемая беременность, возраст старше 65-70 лет, протезирование ТК (даже при одновременной имплантации механического протеза в митральной или аортальной позиции).
Осложнения • Относительный стеноз протеза (допустимые показатели градиентов давления на протезах указаны в технической документации к ним) • Обструкция протеза при тромбозе, фиброзе, разрастании вегетаций • Клапанная (тромбоз протеза или вегетации) или околоклапанная (абсцесс кольца, отрыв протеза) регургитация • ИЭ •• Протезный ИЭ ••• Распространённость — 1–4% в год ••• Ранний (раньше чем через 90 сут после операции) и поздний инфекционный эндокардит бывает вызван разными возбудителями ••• ИЭ различают по клиническому течению и осложнениям ••• При инфекции механического протеза поражение самого клапана возникает редко, но существует тенденция к вовлечению в процесс биологического материала, покрывающего пришивное кольцо ••• При инфицировании биологического протеза возникает поражение как створок, так и клапанного кольца. Вегетации могут не визуализироваться при ЭхоКГ ••• Регургитация возникает вследствие разрушения или перфорации створок биологического протеза, механического препятствия нормальному движению шарика или диска, создаваемого вегетациями •••• Околоклапанная регургитация возникает вследствие абсцесса клапанного кольца и несостоятельности швов ••• Обструкция клапана чаще возникает в связи с массивными вегетациями (причины — грибы, Haemophilus parainfluenzae) •••• Обструкция биологического протеза вегетациями чаще происходит в митральной, чем в аортальной позиции ••• Инфекция протезов сравнительно плохо поддаётся антибиотикотерапии, чаще всего необходимо репротезирование ••• Лечение ИЭ — см. Эндокардит инфекционный.
Оценка состояния протезов • При аускультации слышны щелчки открытия (обычно более тихие) и закрытия (как правило, более громкие) механических протезов; их исчезновение или уменьшение интенсивности — признак тромбоза • Над дисковыми протезами может выслушиваться нежный мезосистолический шум • Биологические протезы не дают специфической аускультативной картины • Рентгенологическое исследование в настоящее время практически не применяют специально для исследования состояния протезов • При ЭхоКГ выясняют тип протеза, измеряют диаметр и амплитуду открытия запирательного элемента механического протеза, измеряют градиент давления на протезе и диагностируют наличие патологических потоков, вегетаций, тромбоза, фиброза • Чреспищеводную ЭхоКГ для визуализации тромбов и вегетаций проводят при подозрении на дисфункцию протеза или при фибрилляции/трепетании предсердий • Инвазивные методы диагностики показаны только при затруднениях в диагностике.
Антикоагулянтная терапия • При внесердечных операциях, чреватых большой кровопотерей, за 2–4 сут до вмешательства отменяют антикоагулянты, 1 раз в 2 сут определяют МНО • За сутки до операции (или раньше, если МНО снижается значительно) начинают вводить гепарин в/в • За несколько часов до операции отменяют гепарин • После отмены гепарина назначают низкомолекулярный декстран, его инфузию продолжают и в послеоперационном периоде до возобновления терапии гепарином и варфарином • Терапию гепарином и непрямыми антикоагулянтами возобновляют через 1–2 сут после операции.
РЕКОМЕНДАЦИИ ПО ДОЗИРОВКЕ НЕПРЯМЫХ АНТИКОАГУЛЯНТОВ АНТИТРОМБОТИЧЕСКОЙ ТЕРАПИИ у пациентов с протезированными клапанами сердца.
• Показания •• Первые 3 мес после имплантации — варфарин, МHO=2,5–3,5 •• Более 3 мес после имплантации ••• Механические клапаны •••• Аортальная имплантация без факторов риска: двустворчатые клапаны (варфарин, МHO=2,0–3,0); дисковые клапаны (варфарин, МHO=2,5–3,5); аортальная имплантация в сочетании с факторами риска (варфарин, МHO=2,5–3,5) •••• Митральная имплантация (варфарин, MHO=2,5–3,5) ••• Биологические клапаны •••• Аортальная имплантация без факторов риска (ацетилсалициловая кислота по 80–100 мг/день) •••• Аортальная имплантация в сочетании с факторами риска (варфарин, MHO=2,0–3,0) •••• Митральная имплантация без факторов риска (ацетилсалициловая кислота по 80–100 мг/день) •••• Митральная имплантация в сочетании с факторами риска (варфарин, MHO=2,5–3,5) ••• Одномоментное коронарное шунтирование — добавление ацетилсалициловой кислоты 80–100 мг/день ••• Варфарин, MHO=3,5-4,5 у пациентов с высоким риском, когда ацетилсалициловая кислота не может быть назначена.
• Если у пациента на адекватной антикоагулянтной терапии произошёл тромбоэмболический эпизод, дозировку препаратов следует откорректировать по следующей схеме •• Варфарин, MHO=2,0–3,0 — дозу варфарина увеличивают до достижения MHO=2,5–3,5 •• Варфарин, MHO=2,5-3,5 — доза может быть увеличена до достижения MHO=3,5-4,5.
• Доказанные лекарственные взаимодействия с варфарином •• Препараты, усиливающие эффект варфарина: амиодарон, ципрофлоксацин, ко-тримоксазол, дисульфирам, флуконазол, циметидин, клофибрат, эритромицин, метронидазол, сульфинпиразон •• Препараты, уменьшающие эффект варфарина: барбитураты, карбамазепин, гризеофульвин, рифампицин, менадиона натрия бисульфит.
Осложнения • Эмболии артерий большого круга • Тромбоз протеза •• При тромбозе механического протеза применение тромболитиков и гепарина в большинстве случаев позволяет устранить обструкцию, по крайней мере, частично •• Эффективность тромболизиса контролируют с помощью ЭхоКГ •• При высоком риске кровотечений и выраженных нарушениях гемодинамики предпочтительнее хирургическое лечение (тромбэктомия или репротезирование клапана) •• Если тромб образуется на вегетациях или разросшейся соединительной ткани, тромболизис малоэффективен или не эффективен совсем •• Окончательные рекомендации по применению тромболизиса как альтернативы хирургическому лечению ещё не разработаны • Тяжёлые кровотечения •• Возникают часто, даже при тщательно контролируемом, терапевтическом уровне гипокоагуляции •• При длительной антикоагулянтной терапии временное уменьшение дозы или полное устранение гипокоагуляции больные обычно переносят хорошо •• Для активного устранения гипокоагуляции вводят менадиона натрия бисульфит (5–10 мг в/в), свежезамороженную плазму (1–2 дозы), устраняют причину кровотечения (с помощью эндоскопического, эндоваскулярного или хирургического вмешательства) и возобновляют антикоагулянтную терапию.
Сокращения • ИЭ — инфекционный эндокардит
Код вставки на сайт
МЕХАНИЧЕСКИЕ ПРОТЕЗЫ
• Виды механических протезов •• Шаровые (в настоящее время не применяют): Magovern-Cromie, Smeloff-Cutter, Cross-Jones, АКЧ, МКЧ •• Дисковые: Bjork-Shiley, Sorin Monocast, Medtronic-Hall, Lillehei-Kaster, Omniscience, Bicer, МИКС, ЛИКС •• Двустворчатые: St. Jude Medical, Sorin Bi Carbon, Carbomedics, ATS, Duromedics, MedEng.
• Преимущество •• Долговечность — в среднем более 30 лет (не принимая во внимание случаи протезного инфекционного эндокардита [ИЭ]) •• Исключение составляют поломки стойки запирательного элемента в некоторых моделях клапана Bjork–Shiley.
• Недостатки •• Тромбогенность (наименьшая у клапана St. Jude Medical) •• Необходимость постоянной антикоагулянтной терапии •• Относительное стенозирование у дисковых и шаровых протезов •• Постпротезные аневризмы у дисковых протезов с небольшим углом открытия запирательного элемента.
• Антикоагулянтная терапия •• Начинают через 2 сут после операции, несмотря на терапию непрямыми антикоагулянтами (МНО на уровне 3,0–4,5) •• Риск тромбоэмболий высок (0,2% летальных и 2% нелетальных осложнений в год) •• Тромбозы после протезирования митрального клапана возникают значительно чаще, вследствие протезирования аортального клапана •• Неоднозначное отношение к механическим клапанам в трикуспидальной позиции (как правило, используют протезы St. Jude Medical) вызвано частым тромбообразованием в правых отделах сердца ••• Такое тромбообразование обусловлено, по-видимому, низкой концентрацией ПгI2, обладающего антитромботическим действием. Этот Пг синтезируется в лёгких и поступает с током крови в левые отделы сердца •• Если хотя бы один раз возникла тромбоэмболия, вызванная наличием протеза, то риск повторных эмболий повышен •• Постоянная антикоагулянтная терапия, даже при умеренном увеличении МНО (до 3,0), значительно увеличивает риск кровотечений.
БИОЛОГИЧЕСКИЕ КСЕНОПРОТЕЗЫ (Hancock, Carpentier-Edwards, КемКор) и аллотрансплантаты. По гемодинамическим характеристикам оба клапана сопоставимы с низкопрофильными механическими протезами (двустворчатым и дисковым).
• Преимущества •• Тромбогенность существенно ниже, чем у механических протезов •• Антикоагулянтная терапия необходима только в течение 2–3 мес после операции (пока не произойдёт эндотелизация пришивного кольца).
• Недостатки •• Недолговечность вследствие дегенеративных изменений и ИЭ, обычно проявляющихся через 4–5 лет после операции и в дальнейшем прогрессирующих •• Вероятность дисфункции через 10 лет после операции — 20%, через 15 лет — 50% •• Долговечность аллотрансплантатов незначительно выше, чем других биологических протезов.
• Факторы, влияющие на долговечность •• Возраст пациента — вероятность дисфункции протеза обратно пропорциональна возрасту на момент операции •• Позиция — вероятность дисфункции протеза в митральной позиции ниже, чем в аортальной •• ХПН и гиперкальциемия при гиперпаратиреозе — увеличение риска дисфункции и скорости её прогрессирования •• Беременность — укорочение срока службы вследствие большей гемодинамической нагрузки (объёмом).
Выбор протеза • Механические протезы •• Аортальная позиция или необходимость одновременного протезирования митрального и аортального клапанов •• ИЭ или реимплантация протеза в связи с ИЭ •• Гиперкальциемия •• Почечная недостаточность • Биологические протезы •• Высокий риск тромбозов (см. ниже) •• Противопоказания к антикоагулянтной терапии (геморрагические диатезы, повторные желудочно-кишечные кровотечения, алкоголизм, нежелание или неспособность следовать схеме лечения), планируемая беременность, возраст старше 65-70 лет, протезирование ТК (даже при одновременной имплантации механического протеза в митральной или аортальной позиции).
Осложнения • Относительный стеноз протеза (допустимые показатели градиентов давления на протезах указаны в технической документации к ним) • Обструкция протеза при тромбозе, фиброзе, разрастании вегетаций • Клапанная (тромбоз протеза или вегетации) или околоклапанная (абсцесс кольца, отрыв протеза) регургитация • ИЭ •• Протезный ИЭ ••• Распространённость — 1–4% в год ••• Ранний (раньше чем через 90 сут после операции) и поздний инфекционный эндокардит бывает вызван разными возбудителями ••• ИЭ различают по клиническому течению и осложнениям ••• При инфекции механического протеза поражение самого клапана возникает редко, но существует тенденция к вовлечению в процесс биологического материала, покрывающего пришивное кольцо ••• При инфицировании биологического протеза возникает поражение как створок, так и клапанного кольца. Вегетации могут не визуализироваться при ЭхоКГ ••• Регургитация возникает вследствие разрушения или перфорации створок биологического протеза, механического препятствия нормальному движению шарика или диска, создаваемого вегетациями •••• Околоклапанная регургитация возникает вследствие абсцесса клапанного кольца и несостоятельности швов ••• Обструкция клапана чаще возникает в связи с массивными вегетациями (причины — грибы, Haemophilus parainfluenzae) •••• Обструкция биологического протеза вегетациями чаще происходит в митральной, чем в аортальной позиции ••• Инфекция протезов сравнительно плохо поддаётся антибиотикотерапии, чаще всего необходимо репротезирование ••• Лечение ИЭ — см. Эндокардит инфекционный.
Оценка состояния протезов • При аускультации слышны щелчки открытия (обычно более тихие) и закрытия (как правило, более громкие) механических протезов; их исчезновение или уменьшение интенсивности — признак тромбоза • Над дисковыми протезами может выслушиваться нежный мезосистолический шум • Биологические протезы не дают специфической аускультативной картины • Рентгенологическое исследование в настоящее время практически не применяют специально для исследования состояния протезов • При ЭхоКГ выясняют тип протеза, измеряют диаметр и амплитуду открытия запирательного элемента механического протеза, измеряют градиент давления на протезе и диагностируют наличие патологических потоков, вегетаций, тромбоза, фиброза • Чреспищеводную ЭхоКГ для визуализации тромбов и вегетаций проводят при подозрении на дисфункцию протеза или при фибрилляции/трепетании предсердий • Инвазивные методы диагностики показаны только при затруднениях в диагностике.
Антикоагулянтная терапия • При внесердечных операциях, чреватых большой кровопотерей, за 2–4 сут до вмешательства отменяют антикоагулянты, 1 раз в 2 сут определяют МНО • За сутки до операции (или раньше, если МНО снижается значительно) начинают вводить гепарин в/в • За несколько часов до операции отменяют гепарин • После отмены гепарина назначают низкомолекулярный декстран, его инфузию продолжают и в послеоперационном периоде до возобновления терапии гепарином и варфарином • Терапию гепарином и непрямыми антикоагулянтами возобновляют через 1–2 сут после операции.
РЕКОМЕНДАЦИИ ПО ДОЗИРОВКЕ НЕПРЯМЫХ АНТИКОАГУЛЯНТОВ АНТИТРОМБОТИЧЕСКОЙ ТЕРАПИИ у пациентов с протезированными клапанами сердца.
• Показания •• Первые 3 мес после имплантации — варфарин, МHO=2,5–3,5 •• Более 3 мес после имплантации ••• Механические клапаны •••• Аортальная имплантация без факторов риска: двустворчатые клапаны (варфарин, МHO=2,0–3,0); дисковые клапаны (варфарин, МHO=2,5–3,5); аортальная имплантация в сочетании с факторами риска (варфарин, МHO=2,5–3,5) •••• Митральная имплантация (варфарин, MHO=2,5–3,5) ••• Биологические клапаны •••• Аортальная имплантация без факторов риска (ацетилсалициловая кислота по 80–100 мг/день) •••• Аортальная имплантация в сочетании с факторами риска (варфарин, MHO=2,0–3,0) •••• Митральная имплантация без факторов риска (ацетилсалициловая кислота по 80–100 мг/день) •••• Митральная имплантация в сочетании с факторами риска (варфарин, MHO=2,5–3,5) ••• Одномоментное коронарное шунтирование — добавление ацетилсалициловой кислоты 80–100 мг/день ••• Варфарин, MHO=3,5-4,5 у пациентов с высоким риском, когда ацетилсалициловая кислота не может быть назначена.
• Если у пациента на адекватной антикоагулянтной терапии произошёл тромбоэмболический эпизод, дозировку препаратов следует откорректировать по следующей схеме •• Варфарин, MHO=2,0–3,0 — дозу варфарина увеличивают до достижения MHO=2,5–3,5 •• Варфарин, MHO=2,5-3,5 — доза может быть увеличена до достижения MHO=3,5-4,5.
• Доказанные лекарственные взаимодействия с варфарином •• Препараты, усиливающие эффект варфарина: амиодарон, ципрофлоксацин, ко-тримоксазол, дисульфирам, флуконазол, циметидин, клофибрат, эритромицин, метронидазол, сульфинпиразон •• Препараты, уменьшающие эффект варфарина: барбитураты, карбамазепин, гризеофульвин, рифампицин, менадиона натрия бисульфит.
Осложнения • Эмболии артерий большого круга • Тромбоз протеза •• При тромбозе механического протеза применение тромболитиков и гепарина в большинстве случаев позволяет устранить обструкцию, по крайней мере, частично •• Эффективность тромболизиса контролируют с помощью ЭхоКГ •• При высоком риске кровотечений и выраженных нарушениях гемодинамики предпочтительнее хирургическое лечение (тромбэктомия или репротезирование клапана) •• Если тромб образуется на вегетациях или разросшейся соединительной ткани, тромболизис малоэффективен или не эффективен совсем •• Окончательные рекомендации по применению тромболизиса как альтернативы хирургическому лечению ещё не разработаны • Тяжёлые кровотечения •• Возникают часто, даже при тщательно контролируемом, терапевтическом уровне гипокоагуляции •• При длительной антикоагулянтной терапии временное уменьшение дозы или полное устранение гипокоагуляции больные обычно переносят хорошо •• Для активного устранения гипокоагуляции вводят менадиона натрия бисульфит (5–10 мг в/в), свежезамороженную плазму (1–2 дозы), устраняют причину кровотечения (с помощью эндоскопического, эндоваскулярного или хирургического вмешательства) и возобновляют антикоагулянтную терапию.
У пациентов, которые перенесли операцию аорто-коронарного или маммаро-коронарного шунтирования, то есть операцию на открытом сердце, всегда много вопросов. Постараемся ответить на самые часто задаваемые.

Можно ли пить после шунтирования?
Сколько живут после шунтирования?
Диета после шунтирования/питание после шунтирования
По поводу диеты можно выделить два основных направления: во-первых, это ограничение животных жиров. К животным жирам относятся продукты, изготавливаемые из мяса, молока, мясных субпродуктов. Также холестерина слищком много в яичном желтке и икре. Самая правильная диета для кардиологического пациента – это средиземноморская. Она богата овощами (кроме картофеля), зеленью, рыбой, морепродуктами, зерновыми. Употребление мяса должно свестись к 1-2 разам в неделю. Предпочтение следует отдавать нежирным сортам мяса – индейке, куриной грудке, дичи. Рыба может использоваться и речная, и морская. Морская рыба богата полиненасыщенными жирными кислотами, которые борются с процессом атеросклероза.

Реабилитация после шунтирования
Этап реабилитации после шунтирования очень важен. В общем от того насколько правильно будет проведен этот этап лечения зависит и дальнейшее выздоровление. Реабилитацию после шунтирования следует разделить на три этапа. Первый этап начинается еще в стационаре, когда пациент начинает делать под контролем врача по лечебной физкультуре дыхательные упражнения и начинает ходить. Второй продолжается в санатории, где постепенно увеличивают нагрузку в виде ходьбы под контролем специалистов и адаптируют пациента к повседневной жизни. Если операция шунтирования была плановая и послеоперационный период протекал спокойно, то переносимость нагрузки у пациента постепенно возрастает и становиться лучше, чем до операции. Собственно, для этого операция и делалась. Несмотря на то, что часто грудину во время операции открывают, а потом соединяют металлическими скобками, бояться, что она разойдется, не нужно. С другой стороны, нужно знать, что грудина срастается в течение 3-х месяцев и в течение этого времени надо ограничивать ассиметричные движения в верхнем плечевом поясе, отказаться от привычки закладывать руки за спину или носить что-то тяжелое в одной руке или на одном плече. У пациентов, которым делали операцию из миниинвазивного доступа очень повезло – с этими вопросами они не столкнуться. Третий этап- амбулаторный. Это самостоятельные тренировки в домашних условиях под четким руководством лечащего кардиолога, который с помощью нагрузочных проб может оценит в правильном ли режиме Вы тренируетесь.
Упражнения после шунтирования/Тренировки после шунтирования
В обычном случае физические нагрузки не противопоказаны и полезны. Для лечащего врача и пациента важно убедиться в их безопасности. Главным методом для этого является проведение стресс-теста - пробы с физической нагрузкой (чаще всего стресс-эхокардиография). Эту пробу стоит провести по совету кардиолога через 3-4 недели после операции. Проба позволяет оценить реакцию организма на нагрузку, выявить нарушения ритма, признаки ишемии миокарда (нехватки крови сердцу). Если тест отрицательный (то есть не выявляет ишемии), а изменения давления и пульса на фоне физической нагрузки оцениваются врачом как адекватные, то такому пациенту мы рекомендуем регулярные кардио- нагрузки.
- Важно помнить, что тренирует сердце только непрерывная нагрузка не менее 30 минут. Работа по дому, прогулки с ребенком сердце не тренируют.
Боли после шунтирования/Осложнения после шунтирования
- Если боль трудно переносимая, принимать обезболивающие (как правило, через 7-10 дней все пациенты уже отказываются от приема обезболивающих препаратов)
- Поднять сниженный гемоглобин. Для этого бывает часто нужен длительный прием препаратов железа.
- Убедиться в отсутствии признаков ишемии миокарда (с помощью нагрузочной пробы) и возобновить физическую активность.
- Быть в контакте с кардиологом для того, чтобы вовремя получить ответы на возникающие вопросы.
Секс после шунтирования. Половая жизнь после шунтирования
Не противопоказан. Скорее наоборот. Для сердца секс является одним из видов кардио-нагрузки. Если результат нагрузочной пробы хороший, то не должно быть никаких опасений. Некоторые исследования показали, что секс именно с женой наиболее безопасен для пациентов после перенесенного инфаркта миокарда.
Эректильная дисфункция частая проблема для наших пациентов, ведь по механизму возникновения она схожа с ишемической болезнью сердца, так как связана с недостаточным расширением артерий. Для большинства мужчин выходом из этой ситуации является прием ингибиторов фосфодиэстеразы 5 типа, то есть Виагры, Сиалиса и так далее. Сами эти препараты никакой дополнительной нагрузки на сердце не вызывают. Есть только одно важное правило – их ни в коем случае нельзя сочетать с нитропрепаратами (нитроглицерин, нитроспрей, нитросорбид, моночинкве, кардикет и так далее) из-за риска резкого снижения артериального давления. Если наши пациенты вынуждены принимать нитраты, то основные препараты для лечения эректильной дисфункции им противопоказаны.
Перелеты после шунтирования. Можно ли летать после шунтирования?
После шунтирования летать можно, если нет каких-либо других ограничений и послеоперационный период прошел спокойно. Первый перелет возможен через 10 дней. Об этом мы можем говорить с уверенностью, так как все наши пациенты, прооперированные в Германии возвращались на самолете домой именно в этот период. Все пациенты после шунтирования принимаю пожизненно малые дозы аспирина. А это хорошая профилактика артериальных тромбозов в том числе во время перелетов.
Одними из факторов риска длительных перелетов являются обезвоживание организма и застой крови в венах ног. Важно пить достаточно жидкости и, при длительных перелетах, не забывать вставать и разминаться.
Ключевую роль в жизни пациента после операции на открытом сердце играет врач-кардиолог. Поэтому принципиально важно найти врача, которому пациент доверил бы свое здоровье. Правильнее всего в этой ситуации ориентироваться на имидж клиники и на опыт конкретного доктора. Ошибкой будет надеяться на кардиохирурга, который проводил операцию. У сердечно-сосудистых хирургов совершенно другая специализация.
-
Контроль артериального давления.
Чем чаще пульс, тем выше потребность мышцы сердца в кислороде и тем больше крови требуется сердцу для нормальной работы. Одна из важных задач кардиолога – обеспечить пациенту достаточно редкий пульс для уменьшения потребности сердца в крови, но и не слишком редкий, чтобы в головном мозге кровоток сохранялся на достаточном уровне. Обычно идеальный пульс для пациента после шунтирования- 55-60 уд/мин. Основные препараты, которые мы используем для урежения пульса это бета- адреноблокаторы (бисопролол, метопролол, небиволол и др). Они не только урежают пульс в покое, но и уменьшают реакцию пульса на физические и эмоциональные нагрузки.
Причина ишемической болезни сердца - атеросклероз коронарных артерий. В основе формирования атеросклеротических бляшек лежит нарушение обмена холестерина. Таким образом, прием лекарств, влияющих на обмен холестерина - это единственный способ воздействовать на причину болезни, которая привела пациента на операционный стол.
После коронарного шунтирования 99% пациентов нуждаются в приеме статинов. Никакие побочные эффекты от приема статинов (по большому счету это только возможные боли в мышцах) не могут сравниться с той пользой, которую дает замедление процесса атеросклероза у наших пациентов.
К сожалению, нередко наши пациенты слышат информацию о вреде сатинов. Это в корне неверно! Статины - единственная группа препаратов, позволяющая остановить процесс атеросклероза. Печальная статистика это только подтверждает. Если проводиться правильный регулярный контроль показателей холестеринового обмена и ферментов (АСТ, АЛТ, КФК), то прием статинов абсолютно безопасен!
Пациентам, перенесшим операцию на сердце следует незамедлительно обратиться к врачу при проявления первых признаков стенокардии. Боли, жжение или тяжесть за грудиной, которые возникают при физической нагрузке, прекращаются при ее остановке и реагируют на прием нитроглицерина – это повод срочно обратиться к врачу, в т.ч. вызвав скорую помощь. Внезапно возникшие или прогрессирующие симптомы стенокардии часто являются предвестником скорого инфаркта.
Читайте также:




