Какая норма сатурации кислорода у пенсионеров
Обновлено: 15.05.2024
Если респираторный дистресс синдром достиг такой стадии, когда требуется более высокая концентрация кислорода для поддержания минимально приемлемой (не менее 80-85%, сатурации кислорода), то такие больные должны быть переведены на ИВЛ через интубационную трубку. Показаниями для интубации трахеи являются показатели газового состава артериальной крови и КОС, хотя следует принимать во внимание скорость нарастания гипоксемии, ацидоза, а также общее состояние больного pi рентгенологическую картону в легких.
Показания к интубации и ИВЛ при респираторном дистресс-синдроме.
1. Артериальная гипоксемия (РаО2 менее 60 мм рт. ст. при использовании высоких концентраций кислорода через плотно прилегающую маску).
2. Неадекватная альвеолярная вентиляция (РаСС>2 более 50 мм рт. ст.).
3. Метаболический и дыхательный ацидоз (рН менее 7,3).
4. Критическая артериальная птотензия.
5. Терминальное состояние (остановка дыхания и сердца).
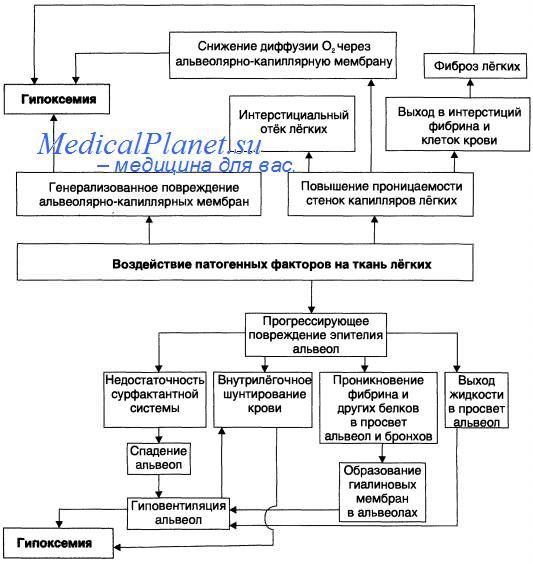
Патогенез респираторного дистресс синдрома взрослых (РДСВ)
Искусственная вентиляция легких при респираторном дистресс-синдроме.
Перевод больного на ИВЛ осуществляется по общим для анестезиологии правилам. После внутривенной премедикации диазепамом, фентанилом и атропином в терапевтических дозах, через маску подается 100% кислород и проводится ручная вспомогательная ИВЛ. Для индукции в наркоз целесообразно использовать оксибутират натрия, являющийся антапшоксантом и благоприятно влияющим на функции ЦНС, сердечно-сосудистой системы, печени и почек. Выключение сознания создает необходимый покой, ликвидирует психо-эмоциональное напряжение, страх и снижает метаболическую потребность в кислороде. Следует подчеркнуть, что интубация должна быть своевременной, не ожидая развития терминального состояния на фоне истощенных резервов дыхательной и сердечно-сосудистой систем.
Важно, чтобы желудок больного был пустой во избежание регургитации и аспирации желудочного содержимого. Если состояние больного или неотложность ситуации не позволяют опорожнить желудок через толстый зонд, то во время индукции и интубации непременно используют прием Селлика. В этих случаях желудок зондируется после интубации и раздувания трахеальной манжетки.
ИВЛ, регулируемая по объему с частотой 12-18 в минуту и относительно большим дыхательным объемом (12-15 мл/кг), проводится для расправления ателектазов и улучшения оксигенации. Концентрация кислорода в дыхательной смеси подбирается такой, чтобы сатурация крови была не менее 85-90%. При этом следует иметь в виду, что при РДС значительно снижается растяжимость легких, поэтому для обеспечения адекватного раздувания требуется значительно большее давление на вдохе - до 30 и даже 40 см вод. ст.
Некоторые авторы считают необходимым проводить ИВЛ в режиме "защиты легких": Vt - 4-6 мл/кг, ПДКВ - 10-13 см ШО, Ppeak - менее 35 см, F1O2 - менее 0,5, f - 18 в минуту для обеспечения Ра02 на уровне не менее 80 мм рт. ст.
Гипервентиляция легких, рекомендуемая некоторыми для компенсации метаболического ацидоза, нежелательна, так как она может вызвать спазм сосудов и нарушения микроциркуляции, способствующие тканевой гипоксии.
Метаболический ацидоз следует устранять растворами бикарбоната натрия или трис-буфером (ТНАМ).
Если на фоне ИВЛ не удается обеспечить минимально необходимый уровень оксигенации крови при концентрации кислорода в «дыхательной смеси до 60% (FiO2 = 0,6), следует использовать повышенное давление в конце выдоха (ПДКВ). Такой режим вентиляции повышает артериальную оксигенацию благодаря лучшему расправлению легких, ликвидации участков ателектаза и снижению шунтирования венозной крови в легких.
Следует учитывать, что режим ПДКВ может уменьшать сердечный выброс за счет нарушения венозного возврата крови, что усугубляется дефицитом ОЦК. Эти два фактора (улучшение оксигенации и снижение сердечного выброса) имеют противоположно направленньш эффект на доставку кислорода (DO2) кровью органам и тканям.
Доставка кислорода рассчитывается по формуле:
D02 (мл/мин) = CaО2 x Q = (1,36 х Hb x Sa02) x Q x 10,
где Са02 - содержание 02 в артериальной крори (мл/100 мл); НЬ -концентрация гемоглобина в артериальной крови (г/100мл); 1,36 х НЬ -кислородная емкость крови при полном насыщении; Sa02 - насыщение артериальной крови кислородом (%); Q - сердечный выброс (л/мин).
Поэтому уровень ПДКВ должен быть отрегулирован таким образом, чтобы получить наилучший результат: оказать минимальное влияние на сердечный выброс при максимальном улучшении оксигенации.
В начале устанавливают ПДКВ на уровне +5 см Н20 и следят за показаниями пульсоксиметра. Такая величина ПДКВ обычно не снижает сердечный выброс, но оксигенация повышается. При недостаточном эффекте постепенно повышают ПДКВ на +2 - +3 см Н20. Для контроля за сердечным выбросом рекомендуют использовать метод термодилюции, катетеризируя легочную артерию катетером Swan-Ganz. Однако этот метод, довольно трудоемкий и к тому же не везде доступен. Практичнее пользоваться неинвазивным методом, основанным на интегральной реографии тела (ИРГТ) по М.ИТищенко или отечественным компьютеризированным комплексом "Diamant" (СПб), применение которого значительно упростило контроль за показателями гемодинамики у тяжелых больных.
Оптимальной величиной ПДКВ является такая, которая обеспечивает адекватную доставку кислорода артериальной кровью при Н02 до 0,6 Обычный уровень ПДКВ от +5 до +15 см Н20 достаточен для насыщения крови кислородом. Если при этом нарушаются показатели гемодинамики, то необходима коррекция ОЦК и использование инотропных препаратов (допамина или добутамина).
Адекватность доставки кислорода тканям можно контролировать по напряжению кислорода в смешанной венозной крови (PvО2). Этот показатель зависит как от содержания кислорода в артериальной крови, так и от сердечного выброса, т. е. является интегральным. При относительно стабильном уровне метаболизма (температура не повышена) снижение Pv02 ниже 40 мм рт. ст. указывает на недостаточную доставку кислорода к органам и тканям. Если при этом оксигенация (SpО2) не уменьшилась, то это свидетельствует о снижении сердечного выброса.
Так как методика измерения Pv02 намного проще, чем измерение сердечного выброса, то этим показателем можно руководствоваться при выборе параметров ИВЛ, ПДКВ и дозировки кардиотропных средств.
Следует согласиться, что поддержание ПДКВ (PEEP) на уровне 5-10 см вод. ст. на какой-то момент способно улучшить газообмен за счет перераздувания еще не полностью заполненных выпотом альвеол. Однако специальные физиологические исследования показали, что объем ВСЖЛ при этом не только не уменьшается, но даже возрастает .из-за большей порозности перерастянутой альвеолокапиллярной мембраны, увеличенной площади фильтрации и затруднения лимфоотока из легочной паренхимы при возрастании внугригрудного давления. Кроме того, при ПДКВ уменьшается и сердечный выброс за счет нарушения венозного возврата крови. Поэтому не следует на длительный период использовать ПДКВ свыше 5 см вод. ст.
Здоровый взрослый человек делает от 12 до 20 вдохов в минуту, хотя насытить кровь кислородом может и гораздо меньшее количество вдохов – около 6 - 8 в минуту. Несмотря на то, что мы делаем большое количество вдохов, большинство из нас не осознает, что мы дышим не оптимально. Оптимальное дыхание оказывает большое влияние на наше здоровье и хорошее самочувствие, поскольку оно напрямую связано с уровнем кислорода в нашем организме. Мы расскажем, почему кислород так важен для нас, а также озвучим 5 простых способов получить больше кислорода.
Целых 90% нашей энергии поступает из кислорода. Дыхание использует химические и механические процессы, чтобы доставить кислород к каждой клетке тела и избавиться от углекислого газа. Нашему телу нужен кислород, чтобы получать энергию для всех наших жизненных процессов. Двуокись углерода является побочным продуктом этого процесса. Дыхательная система с ее проводящей и дыхательной зонами, доставляет воздух из окружающей среды в легкие и способствует газообмену как в легких, так и внутри клеток.
Затем клеткам необходим кислород, чтобы иметь возможность разорвать химические связи молекул пищи, таких как сахара, углеводы и белки, чтобы высвободить содержащуюся в них энергию. Доставка кислорода к нашим клеткам и мышцам делает нас способными выполнять физические упражнения и вести привычную жизнь.
Что такое уровень кислорода в крови
Концентрация кислорода (SpO2) – это термин, используемый при оценке уровня кислорода в кровотоке человека, который является стандартной частью диагностики состояния пациентов во всем мире.
SpO2 означает насыщение кислородом периферических капилляров. Число SpO2 измеряется пульсоксиметром. Он позволяет оценить, сколько кислорода переносит ваша кровь по сравнению с ее максимальной емкостью.
Почему важен кислород и его оптимальный уровень в крови? Дыхание через легкие обеспечивает наши клетки кислородом, заставляет наш мозг работать, а непрерывное сердцебиение обеспечивает доставку кислорода в ткани.
Выполняя тренировку инспираторных мышц (дыхательных, межреберных, мышц грудной клетки), вы можете значительно увеличить количество кислорода.
Норма уровня кислорода в крови у взрослого
Мы вдыхаем кислород через нашу дыхательную систему, в дальнейшем кислород поступает непосредственно в нашу кровь и далее перекачивается в наше тело через кровеносные сосуды. Перенос кислорода происходит за счет наших красных кровяных телец (эритроцитов), которые отвечают за транспорт газов в крови.
Когда мы дышим, мы поглощаем кислород и выводим углекислый газ. Этот газообмен наиболее эффективно происходит в конечной части наших легких, то есть в альвеолах. Поэтому важны глубокие вдохи, они гарантируют, что воздух достигает альвеол, где происходит газообмен, и делает кровь более насыщенной кислородом, что увеличивает уровень кислорода в вашей крови.
Повышенный уровень кислорода помогает нам работать лучше, давая энергию как нашему разуму, так и телу. Если нам не хватает кислорода (состояние гипоксии), мы не можем работать физически, и мы будем чувствовать усталость и переутомление.
Уровень кислорода может сильно различаться у разных людей и зависит от факторов окружающей среды.
Нормальный уровень SpO2составляет от 94% до 99%. У людей с заболеваниями легких уровень SpO2обычно ниже нормы. SpO2ниже 90% очень опасен, и может вызвать нагрузку на сердце, легкие и печень.
Как определить уровень кислорода в крови у взрослого
Тесты для проверки уровня кислорода в крови могут быть полезны при диагностике или мониторинге заболеваний легких. Используемые тесты включают:
- пульсоксиметрию;
- анализ газов крови;
- оценка долгосрочной кислородной терапии;
- тест на гипоксическую нагрузку (пригодность к полетам).
Изучаем лучшие медицинские пульсоксиметры и рассказываем, как выбрать прибор, на что обратить внимание, а также приводим мнение специалистов
Пульсоксиметрия
Кислород переносится в красных кровяных тельцах молекулой, называемой гемоглобином. Пульсоксиметрия измеряет количество кислорода, переносимого гемоглобином в крови, то есть насыщение кислородом и выражается оно в процентах (оценивается по 100-балльной шкале). Это простой безболезненный тест, в котором датчик помещается на кончик пальца или мочку уха. У людей с заболеваниями легких уровень кислорода в крови может быть ниже нормы, поэтому пульсоксиметрия может помочь диагностировать проблему. Чем сильнее повреждены легкие, тем больше вероятность проблемы с потреблением кислорода.
Пульсоксиметрию также можно использовать для определения степени поражения легких.
Тест может быть проведен как разовое измерение при диагностике. Его также можно использовать для измерения уровня кислорода в течение определенного периода времени, например, во время физических упражнений, таких как ходьба, или когда вы спите.
Лак для ногтей или накладные ногти могут блокировать свет и влиять на результаты. Поэтому вам будет предложено удалить покрытие только на одном пальце. Это поможет получить точный результат. На результаты пульсоксиметрии могут влиять болезни, включая анемию и синдром Рейно.
Пульсоксиметрию проводят следующим образом. К пальцу или мочке уха прикрепят небольшое устройство, называемое оксиметром. Он пропускает через кончик пальца или мочку уха 2 световых индикатора: один красный и один инфракрасный. Кровь, содержащая много кислорода, поглощает больше инфракрасного света и пропускает через себя больше красного света. Кровь без достаточного количества кислорода поглощает больше красного света и пропускает больше инфракрасного света. Если вашим клеткам крови не хватает кислорода, они будут казаться более синими.
На дисплее оксиметра отображается процентное содержание кислорода в крови. Для здорового человека нормальный уровень насыщения крови кислородом составляет около 95–100%. Если уровень кислорода ниже, это может быть признаком проблемы с легкими. Людям с низким уровнем кислорода может потребоваться дополнительный кислород или другое лечение.

Оксигенотерапия — лечение кислородом людей, страдающих от его нехватки (гипоксии).
Однако, этот метод часто применяется и здоровыми людьми – жителям крупных городов часто не хватает в атмосфере кислорода и это начинает сказываться на комфорте жизни. Часто этот способ называют просто — оксигенация. Это самый простой способ. Следующий по сложности, но более эффективный — баротерапия (барокамера).

Оксигенотерапия показания
Оксигенотерапия появилась около 200 лет назад, и считается одним из способов повышения оксигенации крови. Частично повышается и содержание кислорода в тканях человеческого организма.
- адаптация людей к условиям, имеющимся на высоте от 4000 м над уровнем моря
- гипоксия, возникшая вследствие развития заболеваний сердечно-сосудистой и дыхательной систем
- реабилитация после химиотерапии
- кислородное голодание, появившееся из-за острого отравления окисью углерода
- метеоризм, возникший после хирургических манипуляций на кишечнике
- профилактика гипоксии у лиц, проживающих в густонаселённых регионах.
Оксигенотерапия противопоказания
Выполнение процедуры запрещено при наличии у пациента гиповентиляции и гиперкапнии. Данные состояния развиваются вследствие нарушений в работе лёгких, за счёт чего показатель углекислого газа в крови стремительно возрастает. Если в данной ситуации применить оксигенотерапию, может развиться отёк мозга, что увеличивает вероятность летального исхода. Часто пациенты путают ощущение насыщения кислородом с кислородным голоданием. Поэтому процедуры надо проводить под контролем специалистов.
Методы оксигенотерапии
На сегодняшний день существуют следующие способы введения кислорода в организм:
- Ингаляционный. Данный метод подразумевает использование кислородных масок, носовых катетеров, специальных трубок. Таким образом кислород поступает в организм пациента через дыхательные пути.
- Неингаляционный. Метод объединяет все остальные пути введения: энтеральный, внутривенный, подкожный и пр.
В ходе процедуры, как правило, используется не чистый кислород (он весьма токсичен), а газовые смеси, в которых его содержание может достигать 90%.
Процесс выполнения оксигенотерапии
В зависимости от используемых инструментов и приспособлений применяются разные техники. Алгоритм действий в любом случае включает в себя следующие мероприятия:
- Подготовка пациента и оборудования
- Подача кислорода, постоянный контроль за состоянием больного
- Уход за пациентом после процедуры
Врач отвечает за качественное проведение оксигенотерапии. Алгоритм выполнения должен быть соблюдён, т.к. игнорирование подготовительного и/или завершающего этапа может негативно сказаться на здоровье пациента.
Наиболее распространённым ингаляционным путём введения является носовой катетер. Следующие по популярности способы – через кислородную маску и с помощью кислородной подушки.
Алгоритм выполнения оксигенотерапии через носовой катетер:
- Пациент принимает удобную позу.
- Врач проверяет исправность оборудования, т.к. утечка кислорода может создать пожароопасную ситуацию.
- Стерилизованный и смазанный вазелином катетер вводится так, чтобы он визуализировался в зёве. Наружный его конец закрепляется на щеке и виске пациента.
- Осуществляется пальпация катетера с целью проверки правильности его установки.
- Запускается подача кислорода.
- По мере необходимости производится замена катетера (с чередованием ноздрей).
- Врач наблюдает за пациентом после процедуры и оказывает помощь при ухудшении его состояния.

Алгоритм оксигенотерапии через кислородную маску
- Маска подсоединяется к оборудованию, проверяется герметичность.
- Прибор включается.
- Маска накладывается на лицо пациента и закрепляется фиксаторами на затылке.
- Проверяется степень прилегания к коже пациента.
Алгоритм выполнения оксигенотерапии через кислородную подушку:
Алгоритм выполнения оксигенотерапии в барокамере:
- Пациент располагается в барокамере. В барокамере он может принимать любую удобную позу и даже спать во время сеанса.
- Пациент надевает кислородную маски или назальные канюли.
- Запускается процесс подачи кислорода, имеющего повышенное давление.
Алгоритм выполнения оксигенотерапии внутривенно (самый популярный неингаляционный метод):
- Пациент укладывается на кушетку.
- С помощью капельницы через вену в организм поступает физраствор, обогащённый смесью озона и перекиси водорода.
Данный способ чаще всего применяется в качестве лечения и профилактики большинства существующих заболеваний. Он показан даже беременным женщинам с целью предотвращения появления гипоксии у плода.

Оксигенотерапия дома
С появлением современных концентраторов кислорода, стало возможным проводить процедуры дома. Для этого необходим концентратор кислорода (кислород отфильтровывается из обычного воздуха) и кислородная маска или назальные канюли. В большинстве случаев достаточно производительности оборудования до 5 л/минуту. Длительность процедуры обычно 10-30 минут.
Применение концентраторов кислорода очень безопасно, по сравнению с баллонами кислорода. И часто достаточно брать в аренду концентратор кислорода, т.к. это будет выгоднее покупки, а курс процедур надо делать периодически.
Заключение
Процедура оксигенотерапии носит как лечебный, так и профилактический характер. Основным показанием к проведению служит гипоксия, появившаяся вследствие различных причин. Тем не менее всё больше людей проходят профилактический курс лечения кислородом, т.к. доказано, что процедура помогает бороться примерно с 200 известными заболеваниями. Врачи тщательно соблюдают алгоритм выполнения оксигенотерапии во избежание появление негативных последствий для здоровья пациента.
Следующим шагом к повышению эффективности является баротерапия — это оксигенотерапия в барокамере под давлением. Это в несколько раз более эффективно!
Известно, что значительный избыток веса может стать причиной хронической дыхательной недостаточности – так называемого синдрома ожирения-гиповентиляции, исторически также упоминающегося в литературе как синдром Пиквика (1). Под этим термином понимается патологическое состояние, при котором у больного с морбидным ожирением развивается хроническая альвеолярная гиповентиляция – гиперкапническая дыхательная недостаточность (РаСО2> 45 мм рт. ст.), которую нельзя объяснить никакими другими причинами, кроме значительного избытка веса (2). Кроме того, у большинства таких пациентов одновременно наблюдаются тяжелые нарушения дыхания во время сна (3), что позволяет ряду авторов рассматривать обструктивное апноэ сна в качестве одной из важных составляющих Пиквикского синдрома (4). При этом хроническая дыхательная недостаточность, как исход выраженного ожирения не является чем-то редким и по данным D. D. Sin et al. (2000) развивается у трети таких больных (5). Патофизиологические механизмы, приводящие к возникновению синдрома ожирения-гиповентиляции, все еще дискутируются в литературе и по всей видимости представляют собой сочетание рестриктивных нарушений легочной вентиляции, хронического утомления дыхательной мускулатуры и нарушения центральных механизмов регуляции дыхания (6). При этом наиболее выраженными дыхательные нарушения оказываются во время сна. Это объясняется дальнейшим ухудшением механики дыхания в положении лежа за счет давления абдоминального жира на диафрагму, а также естественным снижением тонуса дыхательных мышц и понижением центрального респираторного ответа на гипоксемию и гиперкапнию в состоянии сна (7). Присоединение обструктивного апноэ сна еще больше усугубляет тяжесть наблюдающихся у таких пациентов дыхательных расстройств.
До сегодняшнего пациент с синдромом ожирения-гиповентиляции представляет для отечественных практических врачей определенную проблему. Дело в том, что эффективной и безопасной медикаментозной терапии этого состояния не найдено, снижение веса может привести к положительным сдвигам лишь в долгосрочной перспективе, а необдуманное назначение малопоточной кислородотерапии для коррекции гипоксемии, обычно наблюдающейся у таких больных, может привести к еще большему угнетению дыхания и нарастанию гиперкапнии (8). Однако на сегодняшний день мы имеем возможность эффективно лечить таких больных, что наглядно иллюстрирует следующее клиническое наблюдение.
Рис. 1. Пациентка С., 52 лет, индекс массы тела 58 кг/м 2 .
Пациентка С, 52 лет (рис. 1.), бухгалтер, была госпитализирована в кардиологическое отделение Университетской клинической больницы №1 Первого МГМУ им. И.М. Сеченова в феврале 2016 г. При поступлении предъявляла жалобы на одышку при небольших физических нагрузках, таких как спокойная ходьба на расстояние 100-200 м., выраженную дневную сонливость, слабость, быструю утомляемость, беспокойный прерывистый сон, головные боли – преимущественно утром после пробуждения. Из анамнеза известно, что с детства была предрасположена к избыточному весу. В возрасте 20 лет во время первой беременности впервые стала отмечать умеренное повышение артериального давления. После вторых родов в возрасте 37 лет за короткое время прибавила в весе около 40 кг, тогда же стала отмечать беспокоящий окружающих громкий храп, появилась дневная сонливость, начала беспокоить одышка при повседневных физических нагрузках, таких как работа по дому.
Приблизительно в это же время отмечено прогрессирование артериальной гипертонии с максимальными цифрами артериального давления до 220/110 мм рт. ст., несмотря на регулярный прием гипотензивных препаратов. В 2010 г. у пациентки диагностирован синдром обструктивного апноэ сна (СОАС), но на тот момент от рекомендованной СиПАП-терапии она отказалась. Ухудшение состояния с лета 2015 г., когда больная отметила прогрессирующее снижение толерантности к физическим нагрузкам и нарастание сонливости – стали возникать эпизоды приступообразного засыпания, что периодически приводило к падениям и ушибам.
При поступлении в клинику состояние средней тяжести. Питание значительно повышено – индекс массы тела 58 кг/м 2 . Цианоз губ. Частота дыхания 20-22 в минуту. Измеренная с помощью пульсоксиметра сатурация кислорода в покое – 92%, при ходьбе снижается до 88%. Над легкими дыхание ослаблено, хрипы не выслушиваются. Из-за выраженного ожирения границы сердечной тупости не определяются. Тоны сердца приглушены, ритм правильный с частотой сердечных сокращений 90 в мин., патологические шумы не выслушиваются. Артериальное давление 210/100 мм рт. ст. на фоне терапии тремя гипотензивными препаратами в адекватных дозах. Живот значительно увеличен в объеме за счет жировой клетчатки, при пальпации мягкий, безболезненный. Печень и селезенка не пальпируются. Симптом поколачивания по поясничной области отрицательный, дизурии нет. Голени отечны. Грубой неврологической симптоматики нет.
Результаты лабораторного и инструментального обследования:
В общем анализе крови: гемоглобин 136 г/л, эритроциты 4.9 х 10 12 /л, цветовой показатель 0.82, тромбоциты 149 х 10 9 /л; лейкоциты 7.4х10 9 /л, лейкоцитарная формула без особенностей, СОЭ 14 мм/ч. В биохимическом анализе крови отмечена тенденция к незначительному повышению уровня глюкозы натощак, а в остальном также без существенных патологических отклонений. Гормоны щитовидной железы в норме. При исследовании КЩС и газового состава крови: PaО2 – 61 мм рт. ст., PaСО2 – 52 мм рт. ст., компенсированный дыхательный ацидоз.
На ЭКГ синусовый ритм с частотой сердечных сокращений 83 в минуту, признаки гипертрофии левого желудочка. Отрицательные зубцы Т в III и AVF отведениях, возвращающиеся к изолинии при повторной регистрации ЭКГ на вдохе.
Эхокардиографическое исследование выявило дилатацию левого и правого предсердий, умеренную гипертрофию миокарда левого желудочка, а также незначительную регургитацию на митральном и трехстворчатом клапанах. Показатели систолической функции левого желудочка оставались в пределах нормы. Диастолическая функция также существенно не нарушена. Вызывало определенные вопросы отсутствие гипертрофии миокарда правого желудочка и признаков легочной гипертензии у пациентки с хронической дыхательной недостаточностью. Однако, с учетом объективной трудности выполнения ультразвукового исследования сердца при морбидном ожирении полученные результаты вполне могут быть ложно отрицательными.
Суточное мониторирование ЭКГ не выявило клинически значимых нарушений сердечного ритма и проводимости, а также признаков ишемии миокарда.
При рентгеновском исследовании органов грудной клетки очаговые и инфильтративные изменения не выявлены, признаков венозного застоя в малом круге кровообращения нет. Обращает на себя внимание увеличение тени сердца преимущественно за счет его левых отделов.
По данным ультразвукового исследования органов брюшной полости печень нормальных размеров, без признаков венозного застоя. Почки не изменены.
Исследование функции внешнего дыхания показало наличие умеренных вентиляционных нарушений по рестриктивному типу.
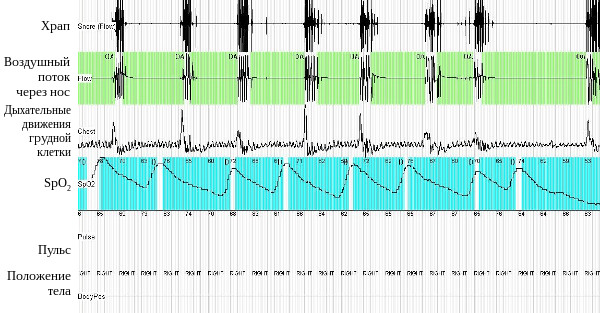
Рис. 2. Респираторное мониторирование во время сна у больной С. (фрагмент записи). Регистрируются множественные эпизоды обструктивного апноэ. Исчезновение дыхательного потока происходит на фоне сохраняющихся дыхательных усилий и сопровождается значительным снижением SрO2. При возобновлении легочной вентиляции возникает храп.
Больной было проведено респираторное мониторирование во время сна, выявлены множественные эпизоды апноэ и гипопноэ обструктивного характера (рис. 2). Индекс апноэ-гипопноэ – 93 события в час. Минимальная сатурация во время сна 50% при средней сатурации 66%. Обращало на себя внимание, что даже при отсутствии эпизодов апноэ и гипопноэ сатурация кислорода во время сна оставалась крайне низкой – порядка 86-87% (рис. 3.). Сделано заключение о наличии у пациентки синдрома обструктивного апноэ сна тяжелого течения и синдрома ожирения-гиповентиляции.
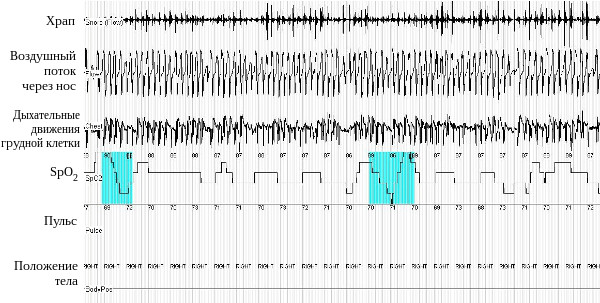
Рис. 3. Респираторное мониторирование во время сна у больной С. (фрагмент записи). Даже при отсутствии эпизодов апноэ наблюдается стойкая гипоксемия со снижением SрO2 до 86-87%. Наличие регулярного храпа косвенно подтверждает, что пациентка в этот момент спит.
Консультация сосудистого хирурга: Хроническая венозная недостаточность.
Консультация эндокринолога: Нарушение толерантности к глюкозе.
Анализ результатов проведенного обследования позволил исключить кардиогенную природу одышки. Было сделано заключение о том, что пациентка с тяжелой артериальной гипертонией и с морбидным ожирением, также страдает синдромом обструктивного апноэ сна тяжелого течения и синдромом ожирения-гиповентиляции (Пиквикский синдром) с формированием хронической дыхательной недостаточности. С учетом того, что нарушения газообмена были в значительной мере ассоциированы со сном и в меньшей степени проявлялись во время бодрствования, наряду с коррекцией гипотензивной терапии пациентке был начат подбор режима вспомогательной вентиляции во время ночного сна. На фоне начатой СиПАП-терапии удалось устранить эпизоды обструкции верхних дыхательных путей, но явления альвеолярной гиповентиляции при этом сохранялись – средняя сатурация кислорода во время сна составила 87%. Соответственно следующим этапом стало начало неинвазивной вспомогательной вентиляции легких с двумя уровнями положительного давления – БиПАП, также только во время ночного сна. При этом величина давления выдоха была установлена согласно оттитрованной раньше величине СиПАП, что гарантировало пациентке беспрепятственную вентиляцию верхних дыхательных путей. Давление вдоха увеличивалось постепенно вплоть до достижения целевой сатурации кислорода более 90%, что в итоге позволило полностью компенсировать имевшие место дыхательные нарушения во время сна.
В результате проводимого лечения состояние пациентки значительно улучшилось: нормализовался сон, перестали беспокоить головные боли по утрам, исчезла дневная сонливость, ощутимо повысилась переносимость физических нагрузок – больная смогла без одышки ходить в пределах отделения. На фоне неинвазивной респираторной поддержки средняя сатурация кислорода во время сна составила 92%. Спустя 1 неделю от начала лечения частота дыхания днем в покое – 18 в минуту, а SpO2 при пульсоксиметрии – 94% и не снижается ниже 90% при спокойной ходьбе. Одновременно было отмечено восстановление чувствительности к гипотензивным препаратам – на фоне терапии эналаприлом, амлодипином и индапамидом достигнута стойкая стабилизация артериального давления на уровне 140/80 мм рт. ст. При контрольном исследовании газового состава артериальной крови в бодрствовании гиперкапния полностью купирована: РаО2 – 66 мм рт. ст. и РаСО2 – 43 мм рт. ст.
В результате больной был поставлен следующий клинический диагноз:
Основное заболевание: Артериальная гипертония 2 стадии, 3 степени, риск IV.
Сочетанные заболевание: Синдром ожирения-гиповентиляции. Синдром обструктивного апноэ сна тяжелого течения.
Фоновые заболевания: Ожирение 3 ст. Нарушение толерантности к глюкозе.
Осложнения: Вентиляционные нарушения 1 ст. по рестриктивному типу. Хроническая дыхательная недостаточность 2 ст.
Выписана через 2 недели пребывания в стационаре в удовлетворительном состоянии с рекомендациями продолжить неинвазивную вспомогательную вентиляцию легких в режиме БиПАП во время ночного сна, прием гипотензивных препаратов в подобранных дозах, а также низкокалорийную диету для снижение веса.
Таким образом, на сегодняшний день применение неинвазивной вспомогательной вентиляции легких является методом выбора при лечении больных с синдромом ожирения-гиповентиляции (рис. 4) и полностью соответствует патофизиологической логике гиперкапнической дыхательной недостаточности, позволяя снизить нагрузку на дыхательную мускулатуру, оптимизировать механику дыхания и восстановить чувствительность дыхательного центра к СО2 (9), одновременно обеспечивая проходимость верхних дыхательных путей во время сна. Благодаря создаваемому резерву это в целом ряде случаев позволяет задействовать вспомогательную вентиляцию прерывисто – только во время ночного сна, в то время как в бодрствовании пациент оказывается способен самостоятельно поддерживать адекватный уровень газообмена.
У пациентов с тяжелым СОАС и умеренными нарушениями газообмена в течении дня лечение следует начинать с СиПАП-терапии – дыхания с постоянным положительным давлением воздуха, что позволяет устранить обструкцию верхних дыхательных путей во время сна. Однако резвившаяся на фоне обструктивного апноэ сна хроническая дыхательная недостаточность по всей видимости отличается по своей природе у разных пациентов. В пользу этого свидетельствует тот факт, что коррекция СОАС приводит к улучшению альвеолярной вентиляции и нормализации показателей газообмена в состоянии бодрствования лишь у части пациентов, в то время как у других положительная динамика показателей газообмена не отмечается (10). Это позволяет клинически разделять пациентов с СОАС и хронической гиперкапнией на подгруппы с апноэ-зависимым и апноэ-независимым и механизмами развития альвеолярной гиповентиляции. И если в первом случае коррекции СОАС бывает достаточно для нормализации показателей газообмена и в бодрствовании, то во втором требуются дополнительные терапевтические опции. Однако так как предсказать заранее к какой из перечисленных групп относится тот или иной пациент до начала лечения затруднительно, то терапия синдрома ожирения-гиповентиляции должна начинаться с устранения обструктивных нарушений дыхания во время сна.
Если СиПАП-терапия не привела к нормализации РаСО2 и устранению гипоксемии во время сна, когда исходная тяжесть дыхательной недостаточности велика или СОАС изначально отсутствует, то пациенту показана классическая неинвазивная вентиляция. Вспомогательная вентиляция подразумевает, что подача аппаратных вдохов производится с учетом самостоятельных дыхательных попыток пациента и синхронизирована с ними. Наибольшее распространение для использования вне палат интенсивной терапии в нашей стране получили портативные аппараты для неинвазивной респираторной поддержки в режиме контроля по давлению – БиПАП. При этом давление выдоха устанавливается на уровне, позволяющем поддерживать верхние дыхательные пути в открытом состоянии, т.е. по сути соответствует величине давления СиПАП, после чего постепенно повышается давление вдоха до величины, позволяющей устранить гиповентиляцию и добиться сатурации кислорода более 90%. Если целевой величины SpO2 достигнуть не удается, то на следующем этапе к лечению следует добавить кислород (6).
![Алгоритм подбора респитаторной терапии при синдроме ожирения-гиповентиляции [по Al Dabal L. et al. (2009) с изменениями] (12).](https://somnolog-pulmonolog.ru/images/algoritm-podbora-respiratornoj-terapii.jpg)
Рис. 4. Алгоритм подбора респитаторной терапии при синдроме ожирения-гиповентиляции [по Al Dabal L. et al. (2009) с изменениями] (12).
При острой гиперкапнической дыхательной недостаточности неинвазивная вентиляция является общепризнанным методом терапии, эффективность которого не вызывает сомнений. У пациентов с хронической гиповентиляцией респираторная поддержка, напротив, используется неоправданно редко, так как все еще рассматриваются многими клиницистами исключительно в качестве составляющей терапии критических и терминальных состояний (11). Наш опыт показывает, что у больных с хронической дыхательной недостаточностью, развившейся в итоге морбидного ожирения, вовремя и по показаниям начатая неинвазивная вспомогательная вентиляция легких позволяет эффективно реабилитировать таких больных и вернуть их к активной жизни.
Профилактические меры, диагностика и лечение CoViD-19
Данные рекомендации предназначены для врачей и иных специалистов, оказывающих медицинские услуги пациентам с диагностированным CoViD-19. Рекомендации созданы на основе Временных методических рекомендаций Минздрава России по профилактике, диагностике и лечению новой коронавирусной инфекции в версии 6 от 28.04.2020.
Характеристики возбудителя заболевания CoViD-19
Новый штамм коронавируса SARS-CoV-2 является одноцепочечным РНК-содержащим вирусом, относящимся ко второй группе патогенности. Официально пандемия CoViD-19 была объявлена ВОЗ 11 марта 2020 года. Основным источником инфекции является больной человек, в том числе в инкубационном периоде.
Стандартный случай заболевания CoViD-19
Для инфекции характерны клинические проявления ОРВИ – температура более 37,5 градусов, кашель (сухой или с небольшим количеством мокроты), одышка, заложенность и сжатость в грудной клетке, насморк и боли в горле, а также другие катаральные симптомы, такие как слабость, головные боли, диарея, отсутствие обоняния. Также для заболевания характерна сниженная сатурация кислорода в крови – равная или менее 95%.
При отсутствии других известных причин, объясняющих клиническую картину, важно учитывать в анамнезе:
- Возвращался ли пациент в течение последних 14 дней из-за рубежа;
- Были ли за последние 14 дней тесные контакты с людьми, которые находятся под наблюдением по CoViD-19;
- Наличие в последние 14 дней контактов с лицами, у которых подтвержден диагноз CoViD-19;
- Работа с пациентами, у которых подтвержден диагноз CoViD-19.
Если у пациента есть характерные клинические проявления в сочетании с выраженными изменениями в легких по результатам КТ или обзорной рентгенографии ОГК вне зависимости от результатов однократного лабораторного исследования на РНК SARS-CoV-2, а также при невозможности проведения исследования на РНК SARS-CoV-2, на основании общего анамнеза его принято считать инфицированным CoViD-19. Также пациент признается инфицированным поле положительного результата лабораторного анализа вне зависимости от клинических проявлений.
Рекомендации по использованию методик лучевой диагностики
- Выбирайте методы исследования дифференцированно, учитывайте имеющееся оборудование и кадровые ресурсы;
- В качестве методов визуализации рекомендован РГ, УЗИ и КТ при необходимости госпитализации и тяжело клинической картине респираторной инфекции, особенно при признаках дыхательной недостаточности;
- При отсутствии у пациента с подтвержденным CoViD-19 симптомов респираторной инфекции КТ, РГ и УЗИ проводить не требуется;
- При амбулаторном лечении пациентов с CoViD-19 при стабильном состоянии и отсутствии признаков ДН проводить КТ, РГ и УЗИ не требуется;
- Проведение оценки динамики течения выявленной пневмонии на фоне CoViD-19 выполняется по клиническим показателям с применением КТ;
- Признаки и изменения, выявленные на КТ, не являются специфичными для определенной инфекции и не дают достаточное основание для постановки этиологического диагноза.
Рекомендации по формулировке заключения после КТ-исследования и вероятность взаимосвязи изменений в легких с CoViD-19-пневмонией
Лечение коронавирусной инфекции CoViD-19
Основным подходом к терапии CoViD-19 являет упреждающее назначение препаратов для предотвращения развития комплекса симптомов и угрожающих жизни состояний, таких как ОРДС, пневмония, сепсис, тромбоз, тромбэмболия. Лечение в соответствии с действующим протоколом рекомендаций применяется в вероятных и подтвержденных случаях заболевания.
Патогенез ОРДС вследствие CoViD-19 имеет в основе избыточный иммунный ответ организма со стремительным и угрожающим жизни высвобождением цитокинов. В таком случае важно назначить упреждающую терапию ИИЛ-6-блокаторами (тоцилизумаб и сарилумаб). При их отсутствии по жизненным показателям необходимо назначь ГКС-терапию. При пневмонии средней тяжести можно рассмотреть терапию таблетированным препаратом барицитиниб в качестве дополнительной терапии.
Какие условия подразумевают назначение упреждающей противовоспалительной терапии
КТ3 по результатам КТ ОГК в сочетании с двумя и более признаками:
Оценка динамки пневмонии CoViD-19 проводится по клиническим показателям в сочетании с применением КТ.
Терапия неотложных состояний и показания к переводу в ОРИТ
- ЧДД более 30;
- Сатурация кислорода менее 93%;
- PaO2/FiO2 менее или равно 300 мм рт. ст.;
- Прогрессирующая пневмония с нарастанием площади инфильтративных изменений более чем на 50% за 24-48 часов;
- Снижение уровня сознания;
- Необходимость внешней респираторной поддержки с помощью ИВЛ и НИВЛ;
- Нестабильная гемодинамика;
- Лактат артериальной крови более 2 ммоль/л.
Прональная позиция для неинтубированных пациентов
В прональной позиции пациент располагается на животе для повышения оксигенации и возможного снижения риска летального исхода. Разумно использовать прональную позицию заранее в сочетании с кислородотерапией и НИВЛ у пациентов с ОРДС легкой степени тяжести – это позволяет снизить потребность в интубации пациентов почти в половину.
Пошаговая стратегия в выборе респираторно терапии коронавирусной инфекции
Пациенты с острой дыхательной недостаточностью вследствие CoViD-19 нуждаются в пошаговом выборе методик респираторной терапии ля повышения результативности лечения.
При ОРДС в легкой форме (сатурация кислорода 80-90%) рекомендуется оксигенотерапия с помощью лицевой маски или назальных канюль, высокопоточная оксигенация или НИВЛ совместно с прональной позицией.
При ОРДС в среднем и тяжелом течении (сатурация кислорода менее 75%) показана интубация трахеи и инвазивная искусственная вентиляция легких в сочетании с прональной позицией.
Показания к интубации трахеи (для процедуры остаточно одного показателя)
- Гипоксемия (сатурация кислорода менее 92%) при высокопоточной оксигенотерапии ли НИВЛ в прон-позиции;
- ЧДД более 35;
- Нарастание видимой экскурсии грудной клетки;
- Состояния измененного или нарушенного сознания;
- Ухудшение визуально картины легких на КТ;
- Остановка дыхания;
- Нестабильная гемодинамика.
Показания к прекращению респираторной поддержки
Для пациентов с ОРДС на фоне CoViD-19 рекомендуется продолжать респираторную поддержку до 14 суток и более. Даже если наблюдается положительная динамика оксигенирующей функции легких, так как при коронавирусной инфекции возможно повторное ухудшение течения ОРДС. Среди выживших средняя продолжительность ИВЛ составляет 14-21 день.
Критерии, по которым определяется готовность к прекращению респираторной поддержки пациента:
- PaO2/FiO2 более 300 мм. рт. ст.;
- Сатурация при вдыхании воздуха более 90%;
- Восстановление кашлевого рефлекса и толчка;
- Отсутствие бронхореи;
- Индекс Тобина менее 105.
Экстракорпоральная мембранная оксигенация (ЭКМО)
На сегодняшний день имеется достаточно данных о возможной перспективности данного метода. Скорость прогрессирования ОДН у пациентов с тяжелой внебольничной пневмонией требует заблаговременно выйти на контакт с центром, располагающим возможностью проведения ЭКМО.
Потенциальными показаниями для ЭКМО являются:
- Индекс Мюррея более 3 или PaO2/FiO2;
- Давление плато более или равно 5 см Н2О несмотря на снижение РЕЕР до 5 см Н2О и снижение Vt до минимума.
Потивопоказания для проведения ЭКМО
- Тяжелые сопутствующие заболевания и ожидаемая продолжительность жизни менее 5 лет;
- Полиорганная недостаточность или SOFA более 15 баллов;
- Немедикаментозная кома вследствие инсульта;
- Невозможность артериального или венозного доступа;
- ИМТ более 40 кг на метр квадратный.
Порядок выписки пациентов из медицинских учреждений
Выписка пациентов с подтвержденным CoViD-19 осуществляется при регрессе клинических проявлений заболевания. Решение о выписке может быть принято до получения двух отрицательных лабораторных РНК-тестов.
Клиническими показаниями к выписке являются:
- Температура тела менее 37,2 градусов Цельсия;
- Отсутствие признаков дыхательной недостаточности, сатурация кислорода при дыхании воздухом составляет более 96%;
- Снижение СРБ до уровня менее двух норм, уровень лейкоцитов более 1*109/л.
Рентгенологические показания к выписке
Проведение КТ или РГ перед выпиской для оценки динамики не является обязательным условием, но может быть назначено лечащим врачом по другим показаниям. В остальных случаях рентгенограмма или КТ могут проводиться амбулаторно через 1-2 месяца после выписки.
Коронавирусная инфекция COVID-19
Нарушение микробной экологии кишечника: взгляды на проблему и пути решения
Читайте также:
- Решение об отказе назначения пенсии отдельным категориям граждан
- Что делают порнозвезды на пенсии
- Является ли повышение пенсионного возраста нарушением стандарта международного права
- Засчитывается ли в стаж учеба в училище до 1990 года при назначении пенсии
- Есть ли льгота военным пенсионерам на проезд в поездах

